2. 南京理工大学化工学院, 江苏 南京 210094
2. School of Chemical Engineering, Nanjing University of Science & Technology, Nanjing 210094, China
离子液体存在下芳香化合物的硝化反应人们已进行了许多研究[1-8]。但离子液体存在下稀硝酸硝化反应的结果仍难令人满意,主要表现为硝化产物得率较低、副反应多。在所采用的离子液体中,阳离子的类型变化较多,阴离子则主要来自于几种常见酸如三氟甲磺酸、硫酸、对甲苯磺酸、氟硼酸等。因此作者试图改变阴离子的构型以提高离子液体的催化活性。
杂多酸是一类含有氧桥的多核配合物,具有类似于分子筛的笼型结构特征[9]。杂多酸组成简单、组分易调,同时具有酸性和氧化性,并可以通过改变组成元素调控其酸性;由于杂多酸阴离子体积大、对称性高及电荷密度低,杂多酸无论是处于固态还是液态,都是强的质子酸,而且所有质子均具有酸性,其酸强度要比由相应中心原子或配位原子组成的无机酸强得多;另外杂多酸表现出的准液相行为赋予了它独特的催化行为。这些特点使杂多酸在很多反应中表现出很高的催化活性,因此在催化研究领域受到重视[10-13]。
在杂多酸结构中,缩合比为1:12的Keggin结构是最具代表性的杂多酸阴离子结构。根据杂多酸的性质,推想由含有Brϕnsted酸性取代基的阳离子与Keggin杂多阴离子构成的离子盐可能会具有与普通酸阴离子构成的离子液体盐不同的催化活性。Keggin型杂多酸H3PMo12O40在甲苯的硝酸硝化(Menke条件下)中表现出了良好的催化活性[14]。本文中,以两性离子[SO3(CH2)4Mim]为阳离子源、Keggin型杂多酸H3PMo12O40为阴离子源,合成了Keggin杂多阴离子基型Brϕnsted酸性离子盐,并考察了其在甲苯的硝酸(67%)硝化反应中的催化作用。
2 实验部分 2.1 试剂与仪器所用试剂均为分析纯。1-甲基咪唑和1, 4-丁磺内酯购自美国百灵威。
Bruker EQUINOX55型红外光谱仪(瑞士)。Agilent Technologies 6820气相色谱仪(美国),OV-101石英毛细管柱(0.25 mm×30 m),FID检测器。硝化产物的气相色谱(GC)测试条件:气化温度250 ℃;柱箱温度,初始温度100 ℃,升温速率10 ℃·min-1,终止温度130 ℃,保持时间2 min;检测器温度250 ℃。
2.2 实验过程 2.2.1 N-丁磺酸根甲基咪唑两性离子的制备[15]将1-甲基咪唑(10 mmol)和1, 4-丁磺内酯(10 mmol)于25 mL茄形瓶中40 ℃充分搅拌反应至完全固化(约24 h),用乙醚反复洗涤至乙醚洗涤液中不含反应物(可用薄层分析,紫外光下不显示荧光即说明乙醚洗涤液中不含1-甲基咪唑),真空干燥,得白色固体即为N-丁磺酸根甲基咪唑两性离子,得率92%。
2.2.2 Keggin型杂多酸H3PMo12O40的制备[14]按P/Mo物质的量之比为1:12称取一定量的Na2HPO4·12H2O和Na2MoO4·2H2O,分别溶于去离子水(5 mL·g-1溶质)中制成溶液,于65 ℃恒温水浴中搅拌混合后,在搅拌的条件下向混合液中缓慢加入一定量的浓盐酸(36.5%,1.4 eqv),冷却至室温下过夜,将酸化后的混合液过滤除去不溶物,再加入乙醚,充分摇匀后静置,混合液分为三层,上层是含有少量杂多酸的乙醚层,中间层是水层,下层为H3PMo12O40与乙醚形成的黄色透明油状物层,分离出底层油状物层,旋转蒸发除去乙醚并真空干燥,得到黄色H3PMo12O40固体,得率87%。
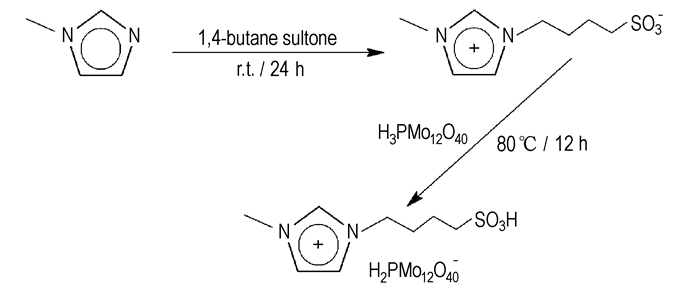
2.2.3 杂多酸根阴离子基型Brϕnsted酸性离子盐的制备将N-丁磺酸根甲基咪唑两性离子与H3PMo12O40按物质的量之比为1:1溶于少量去离子水(5 mL·g-1溶质)中,80 ℃回流12 h,旋转蒸发除水并真空干燥,得到绿色固体,得率99%。反应过程见Scheme 1。
|
Scheme1 Synthesis of Brϕnsted acidic ionic salt based on Keggin heteropolyoxotungstate anion |
称取一定量的催化剂于25 mL茄形瓶中,依次加入设定量的甲苯和硝酸,磁力搅拌,在设定温度下反应一定时间后,停止加热和搅拌,加入0.2 mL硝基苯(内标),正己烷萃取(5 mL×3),简单倾析法分离有机相,有机相合并后依次用饱和NaHCO3(适量)、水(5 mL×3)、饱和NaCl (5 mL×2)洗涤,GC测试。无机相回收离子液体。
3 结果与讨论 3.1 杂多酸及其固体离子盐的表征N-丁磺酸根甲基咪唑两性离子与H3PMo12O40按物质的量之比1:1反应得到固体离子盐,其化学式为:[(CH2)4SO3HMim]H2PMo12O40,这种固体离子盐在丙酮中部分溶解,溶于水和甲醇,微溶于甲苯。
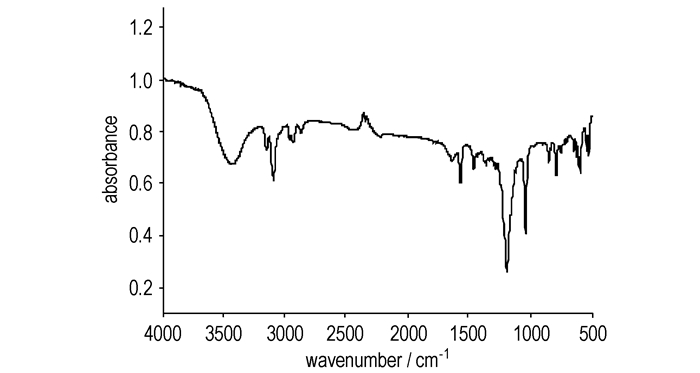
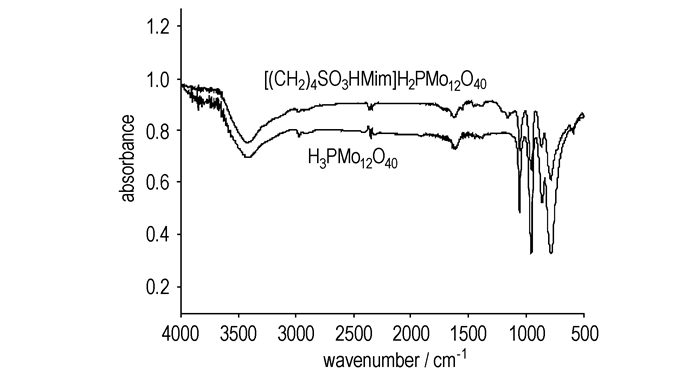
红外光谱分析(图 1和图 2):红外谱图中3400~3500 cm-1附近的吸收峰为H2O分子的伸缩振动。图 2中,H3PMo12O40的红外特征吸收峰波数分别为:1064, 963, 869, 790和594 cm-1;1064 cm-1处的吸收峰是由中心的PO4四面体对称伸缩振动引起的;963 cm-1处的吸收峰归属为MoO6八面体中Mo与端氧的伸缩振动;869 cm-1处的吸收峰为Mo-Ob-Mo伸缩振动;790 cm-1处的吸收峰为Mo-Oc-Mo的伸缩振动;594 cm-1处的特征振动吸收峰是由P-O键的弯曲振动引起的。离子盐[(CH2)4SO3HMim]H2PMo12O40阴离子部分的红外特征吸收峰与H3PMo12O40的相似。两性离子的红外谱图如图 1所示,特征吸收峰波数分别为:3093 cm-1,咪唑环上C-H伸缩振动;1637 cm-1,咪唑环上C=N伸缩振动;1573, 1457, 1390 cm-1,咪唑环上C=C伸缩振动;2940, 2973 cm-1,脂肪族—CH2—的C—H伸缩振动;1463 cm-1,C—N键的特征吸收峰;1041, 1193, 1157 cm-1,—SO3H中S=O的对称伸缩和不对称伸缩振动。由图 1和图 2可看出,两性离子与杂多酸结合后,阳离子的特征吸收要比杂多阴离子的特征吸收弱很多。
|
图 1 Mim(CH2)4SO3的红外谱图 Fig.1 IR spectra of Mim(CH2)4SO3 |
|
图 2 催化剂的红外谱图 Fig.2 IR spectra of the catalysts |
分别考察了催化剂用量、硝酸(67%)用量、反应温度、催化剂的重复使用等几个因素对杂多酸根阴离子基型Brϕnsted酸性离子盐[(CH2)4SO3HMim]H2PMo12O40催化下甲苯的硝酸(67%)硝化反应的影响。
3.2.1 催化剂的用量对硝化反应的影响在催化剂的用量摩尔分数为甲苯的1.0%~10.0%的范围内考察了催化剂的用量对该离子盐催化下甲苯的硝酸(67%)硝化反应的影响。实验结果列于表 1。由表 1可看出,在催化剂用量摩尔分数为甲苯的1.0%~10.0%的范围内,随催化剂用量的增加,一硝基甲苯的收率增加,邻/对硝基甲苯的比例减小,对位产物增加。当催化剂的用量摩尔分数为10%时,硝酸(67%)与甲苯的摩尔比为3:1,50 ℃反应10 h,一硝基甲苯的收率为84.9%,邻/对硝基甲苯的比例为1.21。在一定的用量范围内,催化剂的用量增加,一方面提供了更多的质子酸量,另一方面离子液体对反应物的相转移作用增强,从而提高了硝化反应速率,使一硝基甲苯的收率提高。另外一个可能性是催化剂在体系中起到了干燥和脱水的作用。对位选择性随催化剂离子盐的增多有所改善,可能是由于体系中离子的增多对芳环上电子自旋密度的影响增加,对位C原子上电子自旋密度略有增加所致。
| 表 1 催化剂的用量对硝化反应的影响1) Tab.1 Effect of the catalyst amount on the nitration |
以催化剂[(CH2)4SO3HMim]H2PMo12O40的用量摩尔分数为甲苯的1.0%,50 ℃反应10 h,考察了硝酸(67%)的用量对该离子盐催化下甲苯的硝酸(67%)硝化反应的影响。实验结果列于表 2。
| 表 2 硝酸(67%)的用量对硝化反应的影响1) Tab.2 Effect of the nitric acid (67%) amount on the nitration |
从表 2可看出,随硝酸用量增加,硝化产物收率增加,邻/对硝基甲苯的比例变化不明显。当硝酸(67%)与甲苯的摩尔比为4:1时,50 ℃反应10 h,一硝基甲苯的收率为74.6%。随硝酸用量的增加,硝酸的浓度受反应产生水的影响减小,转化为活性硝化剂的硝酸的量增加,因此硝化产物收率增加;但并不影响活性硝化剂对硝化底物邻、对位的选择性,所以,邻/对硝基甲苯的比例变化不明显。
3.2.3 反应温度对硝化反应的影响以[(CH2)4SO3HMim]H2PMo12O40为例,催化剂的用量摩尔分数为甲苯的1.0%,硝酸与甲苯的摩尔比为3:1,考察了反应温度对该催化剂催化下甲苯的硝酸(67%)硝化反应的影响。实验结果列于表 3。从表 3可看出,随反应温度升高,一硝基甲苯的收率增加,邻/对硝基甲苯的比例略有减小。70 ℃反应10 h,一硝基甲苯的收率为73.3%,邻/对硝基甲苯的比例为1.24。
| 表 3 反应温度对硝化反应的影响1) Tab.3 Effect of the reaction temperature on the nitration |
催化剂[(CH2)4SO3HMim]H2PMo12O40的重复使用实验结果列于表 4。
| 表 4 催化剂的重复使用对硝化反应的影响 Tab.4 Effect of the catalyst reused on the nitration |
由表 4可知,催化剂的用量摩尔分数为甲苯的5.0%,硝酸(67%)与甲苯的摩尔数分别为5.0 mmol,75 ℃反应16 h,一硝化产物得率为52.4%。催化剂回收真空干燥后再次用于甲苯的硝酸(67%)硝化反应,硝酸(67%)与甲苯的摩尔数分别为10.0 mmol,催化剂的摩尔分数变为2.5%,70 ℃反应16 h,一硝化产物得率为39.5%,与不加催化剂的反应体系(一硝化产物得率为27%)相比,具有催化活性。催化剂再次回收干燥后未进行纯化处理直接用于硝化反应,反应条件与第二次相同。催化剂第三次使用的反应结果较第二次变化较大,一硝基甲苯的得率下降了7.5%,这可能是由于硝化反应副产物滞留于催化剂中,对催化剂起了包裹作用,使催化剂不能与反应物充分接触,从而降低了催化剂的催化活性。
4 结论Keggin杂多酸阴离子基型Brϕnsted酸性离子盐[(CH2)4SO3HMim]H2PMo12O40对甲苯的硝酸(67%)硝化具有良好的催化作用。在催化剂用量摩尔分数为甲苯的1.0~10.0%的范围内,随催化剂用量的增加,一硝基甲苯的收率增加,邻/对硝基甲苯的比例减小,对位产物增加。当催化剂[(CH2)4SO3HMim]H2PMo12O40的用量摩尔分数为甲苯的10%时,硝酸(67%)与甲苯的摩尔比为3:1,50 ℃反应10 h,一硝基甲苯的收率为84.9%,邻/对硝基甲苯的比例为1.21。
| [1] |
Earl M J, Katdare S P, Seddon K R. Paradigm confirmed: The first use of ionic liquids to dramatically influence the outcome of chemical reactions[J].
Org Lett, 2004, 6(5): 707-710. DOI:10.1021/ol036310e |
| [2] |
Smith K, Liu S, EL-Hiti G A. Regioselective mononitration of simple aromatic compounds under mild conditions in ionic liquids[J].
Ind Eng Chem Res, 2005, 44: 8611-8615. DOI:10.1021/ie050047z |
| [3] |
Lancaster N L, Verónica L M. Aromatic nitrations in ionic liquids: The importance of cation choice[J].
Chem Commun, 2003: 2812-2813. |
| [4] |
Qiao K, Yokoyama C. Nitration of aromatic compounds with nitric acid catalyzed by ionic liquids[J].
Chem Lett, 2004, 33(7): 808-809. DOI:10.1246/cl.2004.808 |
| [5] |
Qiao K, Hagiwara H, Yokoyama C. Acidic ionic liquid modified silica gel as novel solid catalysts for esterification and nitration reactions[J].
J Mol Catal A: Chem, 2006, 246: 65-69. DOI:10.1016/j.molcata.2005.07.031 |
| [6] |
Fang Dong, Shi Qun-Rong, Cheng Jian, et al. Regioselective mononitration of aromatic compounds using Brønsted acidic ionic liquids as recoverable catalysts[J].
Appl Catal A: General, 2008, 345: 158-163. DOI:10.1016/j.apcata.2008.04.037 |
| [7] |
齐秀芳, 程广斌, 吕春绪. 酸性离子液体存在下甲苯的硝化反应[J].
含能材料, 2008, 16(4): 398-400. QI Xiu-fang, CHENG Guang-bin, Lü Chun-xu. Nitration of toluene with nitric acid in the presence of acidic ionic liquids(Ⅱ)[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2008, 16(4): 398-400. |
| [8] |
方东, 施群荣, 巩凯, 等. 离子液体催化甲苯绿色硝化反应研究[J].
含能材料, 2007, 15(2): 122-124. FANG Dong, SHI Qun-rong, GONG Kai, et al. Green nitration of toluene in ionic liquids[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2007, 15(2): 122-124. |
| [9] |
王恩波, 胡长文, 许林.
多酸化学导论[M]. 北京: 化学工业出版社, 1998.
|
| [10] |
Nisikin M, Nakamura R, Niiyama H. An unusual suppression of trimethlyamine formation in the high temperature alkylation of ammonia with methanol over (NH4)3PW12O40[J].
Chem Lett, 1993: 209-212. |
| [11] |
Nishimura T, Okuhara T, Misono M. High catalytic activities of pseudoliquid phase of dodecatungstophosphoric acid for reaction of polar molecules[J].
Chem Lett, 1991: 1695-1698. |
| [12] |
Sato H, Nagai K, Yoshioka H, et al. Vapor-phase nitration of benzene over silid acid catalysts (3): Nitration with nitric acid; mixed metal oxide treated with sulfuric acid and heteropolyacid partially neutralized[J].
Appl Catal A: General, 1998, 175: 209-213. DOI:10.1016/S0926-860X(98)00217-8 |
| [13] |
陈霄榕, 李永丹, 康慧敏, 等. SiO2与Keggin杂多酸相互作用的研究[J].
分子催化, 2002, 16(1): 60-64. CHEN Xiao-rong, LI Yong-dan, KANG Hui-min, et al. Investigation of Inter action between SiO2[J]. Journal of Molecular Catalysis(China), 2002, 16(1): 60-64. |
| [14] |
程广斌, 吕春绪, 彭新华. 钼磷酸催化下甲苯的选择性硝化[J].
含能材料, 2004, 12(2): 110-112. CHENG Guang-bin, Lü Chun-xu, PENG Xin-hua, et al. Selective nitration of toluene with nitric acid in the presence of phosphomolybdic acid catalysts[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2004, 12(2): 110-112. |
| [15] |
Ntai I, Tran K L T, Weaver K J. Novel Brønsted acidic ionic liquids and their use as dual solvent-catalysts[J].
J Am Chem Soc, 2002, 124: 5962-5963. DOI:10.1021/ja026290w |
A novel Keggin heteropolyacid anionic Brϕnsted acid salt [(CH2)4SO3HMim]H2PMo12O40 was synthesized and used as efficient catalyst in toluene nitration in HNO3(67%).



