熔铸炸药是指能以熔融态进行铸装的混合炸药,是当前应用最广泛的一类军用混合炸药,约占军用混合炸药的90%以上。它们能适应各种形状药室的装药,综合性能较好,多用于迫击炮、手榴弹、炮弹、导弹弹头和地雷装药,在军用混合炸药中占有重要的地位。其载体可通过硝硫混酸、发烟硝酸和硝酸-乙酸酐等硝化剂硝化合成。理想的熔铸炸药[1]应该具有以下性质:(1)熔点为70~120 ℃;(2)低蒸汽压(较低的毒气吸入量);(3)在熔点和化学分解开始之前有足够的电荷分离;(4)冷却时没有收缩和扩张;(5)弹药和弹壳间没有间隙;(6)高密度和优良的爆炸性能;(7)不过早爆炸;(8)绿色合成。但这些性能之间存在着矛盾,如良好表现性能的熔铸炸药载体及其配方在冷却时易于收缩和扩张。早期使用的2, 4, 6-三硝基苯酚(TNP)的爆轰性能虽然较TNT好,但机械感度比TNT高,热感度也较高且酸性很强,腐蚀金属,安全性低。因此,TNP逐渐被TNT取代,淡出市场[2]。
现阶段熔铸炸药主要采用TNT作为液相载体炸药,TNT为基的熔铸炸药在20世纪发挥了巨大的作用,得到了世界范围的认可,广泛应用于工业炸药和军用炸药中。然而TNT不仅生产过程中排放的废物对工人健康和环境都有危害,而且TNT类炸药存在渗油、收缩、空洞、发脆和膨胀现象,对弹药的感度、易损性和运输都会产生影响,随着现代武器的发展,TNT不再能满足当前钝感弹药标准(IM)的要求。国内外都在大力寻找可替代TNT的高能钝感含能材料。本研究结合课题组多年的成果[2-21],参考国内外相关文献,对现阶段使用的TNT和有望替代TNT熔铸炸药载体的研究现状进行了综述,为熔铸炸药配方载体的选择提供参考。
2 熔铸炸药载体的研究现状 2.1 苯环类熔铸炸药载体(1) 2, 4, 6-三硝基甲苯(TNT)
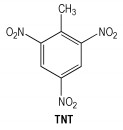
TNT是一种十分成熟的载体炸药(见Scheme 1),其密度1.64 g·cm-3,熔点80.8 ℃,爆速6940 m·s-1,爆压29.0 GPa[22]。合成工艺成熟、三废处理比较完善、制造成本很低,具有优良的热稳定性和塑性,爆发点较高而机械感度较低,爆炸能量适中。TNT为基的熔铸炸药得到了世界范围的认可,广泛应用于工业炸药和军用炸药中,然而TNT生产中含有红色的硫酸酯化硝基甲苯的废物流对工人健康和环境都有危害[23-25],并且TNT为基熔铸炸药,很难除去的同分异构体、三硝基苯、一、二硝基化合物会使TNT的凝固点降低而使其铸件渗油。而且TNT形体稳定性较差,热循环后能产生不可逆膨胀,悬浮的TNT还有过冷现象,过冷度较大,自发晶核出现较慢;针状晶形,铸件时易形成粗结晶结构,凝固过程中会发生明显的体积收缩,由此形成的铸件在结晶-收缩-熔化-再结晶-收缩的反复循环过程中,在晶粒间产生微观裂纹,形成大气孔。TNT从液态凝固后要产生11.6%的体积收缩,对弹药发射安全不利,TNT还有与生俱有的脆性而影响铸件的力学性能[26]。因此,不久的将来会逐渐被新型的熔铸炸药载体所取代。
|
Scheme 1 |
(2) 2, 4-二硝基苯甲醚(DNAN)
DNAN分子结构式如Scheme 2所示,熔点95 ℃,氧平衡-97%,密度1.34 g·cm-3,爆速5600 m·s-1,爆压7.02 GPa[27]。在DNAN作为熔铸介质时,考虑到其密度、能量比TNT低,通常在配方中加入高氯酸按(AP),使其混合密度、能量接近TNT。1849年首次合成,在二战中首次被应用到弹药中,装填德国的V-1火箭,Amatol-40(50% DNAN,35% AN,15% RDX)。2000年美国Picatinny Arsenal的研究者们研制出了PAX-21炸药。2004年美国已建立了采用连续法工艺生产DNAN的工厂,设备采用的是已经闲置的TNT设备。北京理工大学也在开展这方面的应用研究。由于DNAN能量比较低,二战后很长一段时间无人问津,但随着对不敏感弹药要求的提高,DNAN优良的钝感性引起了各国的广泛关注。

|
Scheme 2 |
DNAN合成得率较高方法有以下几种:(1)在甲醇中加入二硝基氯苯,再少量多次加入碳酸钾,回流反应一段时间,冷却加入冰水析出产物,得率在97%~99%;(2)一锅法合成DNAN,在烧瓶中加入碳酸钾、2, 4-二硝基酚、溴化甲烷和甲基异丁酮,密封加压反应,冷却,去溶剂,得率在91%~93%;(3)用甲醇溶解二硝基氯苯,把氢氧化钠溶液滴入混合液中,回流1h,冰水析出产物,得率90%左右;(4)用氯苯在硝硫混酸作用下,制取二硝基氯苯,再在甲醇和氢氧化钠混合液中制取DNAN[28]。为了降低DNAN的熔点,通常加入N-甲基-对硝基苯胺(MNA) [29],但MNA的量不能超过DNAN量的1.5%。作为载体同时也要必须考虑其与其他固相炸药的相容性,通过真空安定性实验表明DNAN与现阶段大量应用的高能炸药如HMX、RDX等有很好的相容性。DNAN单独作为熔铸介质,表现出的缺点是熔点略微偏高(需要加入降低熔点的物质)而能量密度偏低。
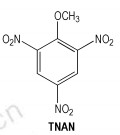
此外,三硝基苯甲醚(TNAN)也是一种低感炸药,结构式见Scheme 3,它的性能介于TNT与苦味酸之间[30],其熔点较低(68 ℃),在使用中受到限制。缺点是它会造成皮肤湿疹,生理学上不安全。
|
Scheme 3 |
(1)3, 4-二氰基氧化呋咱(DFCO)
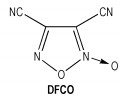
Homewood等人[31]通过以三氟乙酸或者三氯乙酸为溶剂,在温度为40 ℃下硝酸与氰乙酸反应2 h制得DFCO,其结构式如Scheme 4所示。它也可通过氨基氧化呋咱的重氮化作用制备,一份3-氨基-4-硝基氧化呋咱与3~6份NaNO2在H2SO4/乙酸中于35 ℃反应可以生成3, 4-二氰基氧化呋咱,得率小于8%[32]。DFCO已经被用作TNT、硝化甘油等类似炸药的替代品,它具有相当大的能量,极其稳定,对热和冲击钝感。其较低的熔点与感度,较高的爆速和稳定性使其成为具有良好应用前景的熔铸炸药载体。
|
Scheme 4 |
(2) 4, 4′-二硝基-3, 3′-呋咱(DNBF)
DNBF可通过氧化4, 4′-二氨基-3, 3′-呋咱制得[33-34],结构式见Scheme 5。其爆轰参数分别为:熔点85 ℃,密度1.85 g·cm-3,爆速8800 m·s-1,爆压35.6 GPa。DNBF较低的熔点与较好的爆轰性能使其成为很有吸引力的熔铸炸药载体,但其特性落高H50=12 cm,与太安(PETN)接近,因此,在合成与使用过程中需要严格的安全措施。

|
Scheme 5 |
(3) 3, 4-二硝基呋咱基氧化呋咱(DNTF)
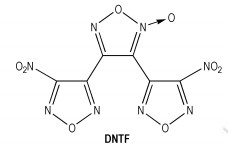
DNTF是一种新型的含能氧化剂,结构式见Scheme 6,它具有较高的能量与较好的热稳定性[35]。20世纪80年代首次由俄罗斯合成,我国于上世纪90年代合成成功。它的制备方法是以3, 4-二氨基呋咱基氧化呋咱(BAFF)为原料,用96%的H2O2与三氟乙酸酐(TFAA)为氧化剂氧化BAFF,得率50%。熔点107~110 ℃,密度1.937 g·cm-3,爆速9250 m·s-1。DNTF具有能量高、密度大、安定性好、感度比较高、综合性能优于HMX[36-38]。DNTF被认为极具潜力的熔铸炸药配方组分[39-40]。DNTF在110 ℃以下可长时间受热不分解,仅有微量挥发性。DNTF的熔点已经达到了熔铸炸药载体炸药的上限,这给熔铸工艺带来了困难,但DNTF能与其他化合物形成低共熔物,更有可能与其生成络合物。因此要寻找能与其形成低共熔物的炸药,这样既降低熔铸温度,改善熔铸工艺,又可以提高组分能量利用率。已见报道的DNTF低共熔体有DNTF/PETN、DNTF/TNT。
|
Scheme 6 |
氮杂环硝基化合物由于结构中含有大量的N—N、C=N、N=N和N—O键等高生成热基团,因而具有很高的生成焓,其独特的性能在含能材料的研究中备受重视。它们的爆轰性能大都优于TNT。
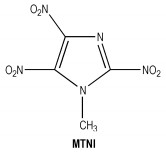
(1) 1-甲基-2, 4, 5-三硝基咪唑(MTNI)
MTNI,结构式见Scheme 7,熔点82℃,氧平衡-25.79%,密度1.8 g·cm-3,性能(爆速8800 m·s-1,爆压35.58 GPa)与RDX相当,感度(H50=100 cm,F=252 N)介于TNT与RDX之间。2001年首次报道Jin Rai Cho等人合成了MTNI [40],到目前为止MTNI的合成路线有四条[28]:(1)由咪唑制备,用硝硫混酸硝化咪唑,得到4-硝基咪唑,4-硝基咪唑在冰乙酸、发烟硝酸和乙酸酐的作用下反应,通过加入氯苯重排得到2, 4-二硝基咪唑,再通过混酸和氯化钾、碳酸钾作用下制得三硝基咪唑盐,最后甲基化得产物,得率23%;(2)由2, 4-二硝基咪唑制备,经过硝化、甲基化制得产物;(3)由4-硝基咪唑制备,经硝化、重排、甲基化制得产物,得率20%;(4)由甲基咪唑制备,在硝基甲烷中溶解甲基咪唑,冷却搅拌,加入四氟硼酸硝鎓盐反应,加热蒸馏,同时回收硝基甲烷,反应一段时间,倒入冰水,用二氯甲烷萃取,洗涤干燥得产物,得率13%。由于MTNI的熔点低,并且其能量比TNT高,它可以替代TNT,用作熔铸炸药。2006年《世界兵器发展年度报告》介绍了美国匹克尼丁兵工厂通过六步法合成MTNI,提出它是更好的TNT替代品。但MTNI合成路线较长不易工业化生产。本课题组[12-15]在它的合成工艺方面进行了研究。以咪唑为原料,常温下在碘的碱性溶液中碘化,然后甲基化、硝化得到1-甲基-2, 4, 5-三硝基咪唑, 最终得率达到到23%。优化了1, 4-二硝基咪唑重排合成2, 4-二硝基咪唑的工艺条件,其收率达到92%。
|
Scheme 7 |
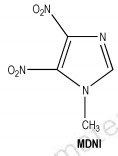
(2) 1-甲基-4, 5-二硝基咪唑(MDNI)
MDNI(Scheme 8)是在1-甲基-2, 4, 5-三硝基咪唑(MTNI)的合成过程中得到一种新型的低熔点炸药,其熔点为77~78 ℃,密度为1.64 g·cm-3[3],撞击感度为87 cm(5 kg wt),爆速实测值[3]7093 m·s-1 (密度1.542 g·cm-3),收缩率为4.05%~4.30%(TNT的收缩率8.50%~9.50%)。近年来,重点对1-甲基-4, 5-二硝基咪唑的合成工艺进行了优化,并对其爆炸性能也进行了初步研究。结果表明,MDNI是一种优良的钝感、低熔点炸药,是以甲基咪唑为原料一步硝化合成而得[11, 16]。本课题组[3, 11, 16]通过几年的努力,以甲基咪唑为原料一步硝化的制备工艺得率由20%提高到40%,可提供公斤级制备工艺。目前与某厂联合开发其应用。
|
Scheme 8 |
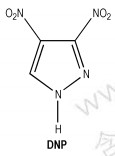
(3) 3, 4-二硝基吡唑(DNP)
DNP[4]熔点86 ℃,密度1.81 g·cm-3,爆速8240 m·s-1,爆压28.80 GPa,撞击感度适中,摩擦感度较低,热稳定性也较好[41-42]。DNP(Scheme 9)最初的制备方法是,从吡唑硝化获得N-硝基吡唑,然后重排制得3-硝基吡唑,得率可达67%,3-硝基吡唑进一步硝化可得3, 4-二硝基吡唑,得率为65%[43-44]。Latpov等人[45],通过3-氨基-4-硝基吡唑与过量的NO2反应制得,提高了DNP的得率。Katrizky[46]等人通过以硝酸-三氟乙酸酐在室温下硝化吡唑反应12 h制得DNP,得率42%。此外,RAvi[47]通过硝化3, 4-二碘吡唑制备获得DNP,其中3, 4-二碘吡唑是由吡唑的碘化反应(吡唑在氨水中与I 2/K I反应)制备而得[48],DNP作为载体炸药具有较好的应用前景。本课题组[2, 4, 6]在它的合成工艺方面进行了研究,目前可提供公斤级的样品。
|
Scheme 9 |
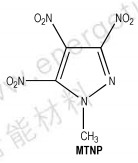
(4) 1-甲基-3, 4, 5-三硝基吡唑(MTNP)
MTNP的熔点89 ℃,分解温度256 ℃,密度1.83 g·cm-3,爆速8960 m·s-1,爆压33.54 GPa[49],其结构式如Scheme 10所示。它是3, 4, 5-三硝基吡唑(TNP)的一种新型衍生物,Herve等人[49-50]报道了在乙腈中通过三硝基吡唑钠盐与碘甲烷的甲基化反应制得MTNP的合成方法。TNP的制备有三种方法:(1)以4-氨基-3, 5-二硝基吡唑为原料,以二苯氧基硫酸为氧化剂氧化制得,得率93%;(2)以5-氨基-3, 4-二硝基为原料,二苯氧基硫酸氧化制备,得率37%;(3)用硝酸与20%~30%的发烟硫酸的混酸在100 ℃硝化吡唑反应1 h制备,得率94%。此外,TNP和MTNP也可通过3, 4, 5-三碘吡唑与1-甲基-3, 4, 5-三碘吡唑分别硝化制备,得率较高[47]。本课题组在它的合成工艺方面采用硝酸盐的催化硝化取得了较大进展。
|
Scheme 10 |
(5) 1-甲基-3, 5-二硝基-1, 2, 4-三唑(MDNT)
MDNT是一种典型的三唑类硝基化合物,结构式见Scheme 11,熔点98 ℃,晶体密度1.676 g·cm-3,实验测试密度1.63 g·cm-3,能量输出415 J·cm-3,爆速7659 m·s-1。其制备方法为:3, 5-二氨基-1, 2, 4-三唑(DAT)与亚硝酸钠-硫酸经硝化反应制得3, 5-二硝基-1, 2, 4-三唑(DNT),DNT再通过与硫酸二甲酯或者碘甲烷甲基化反应制备[51]。MDNT的安定性和TATB相当,性能与B炸药接近,撞击感度与摩擦感度分别为大于100 cm和252 N。它具有优异的综合性能,可用蒸汽熔化加工,替代TNT用于熔铸炸药,并可广泛用于高能钝感炸药和推进剂中。文献报道得率不到10%,本课题组[8-10]采用新工艺,以双氰胺与二盐酸肼为起始原料,在水中缩合环化得到3, 5-二氨基-1, 2, 4-三唑(DAT),DAT再经重氮化、硝基取代得到3, 5-二硝基-1, 2, 4-三唑(DNT),最后以乙腈作溶剂甲基化得到DNMT,最终将得率提高到32%。

|
Scheme 11 |
(1)2, 4, 6-三叠氮基-1, 3, 5-三嗪(TTA)
TTA是在1921年合成的一个富氮化合物,分子中只含有碳元素与氮元素,其结构式如Scheme 12所示。它可以很容易的由2, 4, 6-三氯-1, 3, 5-三嗪(TCT)和叠氮化钠(SDA)反应制得[52]。其密度为1.54 g·cm-3,熔点94 ℃,分解温度为187 ℃,爆速5680 m·s-1。它具有较高的撞击感度与摩擦感度,性能与叠氮化铅、三硝基间苯二酚铅相当[1]。尽管TTA拥有至少相当于雷酸汞两倍的爆炸威力,却由于挥发性和对火花、摩擦、撞击等极其敏感而限制了它的实际应用。

|
Scheme 12 |
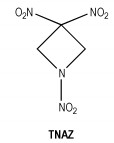
(1) 1, 3, 3-三硝基氮杂环丁烷(TNAZ)
TNAZ氧平衡OB=-16.70%,熔点101 ℃,密度1.84 g·cm-3,爆速8730 m·s-1,爆压37.2 GPa,特性落高H50%=21cm,性能优于RDX [53-54],分子结构式见Scheme 13。它于1984年首次合成,至今已报道的合成路线超过了20种,但真正应用于一定规模的工业合成的路线就两条[55-56]:(1)硝基甲烷法; (2)氯代环氧丙烷法。由于其熔点低、分解点高、密度高、液相稳定性良好、与其它炸药有良好的相容性等优点,因此TNAZ可用于熔铸炸药。但TNAZ制造成本高,制约了TNAZ的应用。
|
Scheme 13 |
在TNAZ的应用研究方面,美国一直处于领先地位,德国在1997年也成立了专门的研究室,以期望在TNAZ的工业化方面取得突破。西安近代化学研究所以美国中试合成路线(硝基甲烷法)为基础进行了研究,并对关键步骤进行了改进,收率达到40%以上,目前已达百克量合成规模。
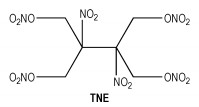
(2)二硝基四硝酸酯(TNE)
Chavez等人[57]报道了二硝基四硝酸酯(TNE)的合成方法,赤藓糖醇与硝酸乙酰酯在乙酸中硝化可制得TNE,其结构式如Scheme 14所示,得率85%。熔点86 ℃,分解温度141 ℃,生成热和分解热分别为-371 kJ·mol-1与818 J·g-1。TNE密度1.92 g·cm-3,爆速9100 m·s-1,爆压40 GPa,能量高于HMX。由于它熔点较低,可以熔化并倒入特定模具中,更易制备炸药配方。它也可作为高能增塑剂和双基药组分使用。其对冲击,摩擦和火花的感度与太安相当,可以充当其他炸药的高能塑化剂。
|
Scheme 14 |
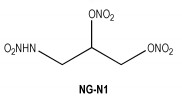
(3) 1-硝氨基-2, 3-二硝酸酯基丙烷(NG-N1)
Altenburg[58]报道了1-硝氨基-2, 3-二硝酸酯基丙烷(NG-N1)的合成方法,它是一种新型的硝胺炸药,结构式见Scheme 15。它可通过硝化1-氨基-2, 3-丙二醇制备,得率和纯度很高。NG-N1熔点66 ℃,分解温度173 ℃,密度1.80 g·cm-3,爆速8840 m·s-1,爆压32.60 GPa。它是迄今为止唯一的一种在熔化时不发生分解现象的硝胺。由于分子的氢键作用,NG-N1的感度(14 J)与硝化甘油(0.2 J)相比显著降低。
|
Scheme 15 |
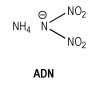
(1)二硝酰胺铵(ADN)
ADN结构式见Scheme 16,是一种对环境友好的高能氧化剂,为燃烧提供大量的氧元素,可作为高氯酸按(AP)的替代物。在火药配方中,ADN代替AP后能够提高能量和火药的燃速,具有潜在的应用,如作为火箭推进剂配方组分,水下熔铸炸药,阳离子相转移试剂等。ADN分子结构中C和Cl的缺失会降低火箭和导弹中以ADN为基推进剂的尾焰雷达信号[59-61]。ADN熔点为92 ℃,密度1.82 g·cm-3,与烷基二硝酰胺相比,它的稳定性较高,感度较低[62-63]。已报道多条二硝酰胺阳离子的合成路线,但大部分不适合放大合成。Hatano与合作者[64]报道了一种清洁安全的通过尿素制备ADN的方法,以Ac2O/HNO3为硝化剂在0 ℃硝化双(二氰乙基)胺,然后经碱性脱氰和进一步硝化(硝化剂NO2BF4)制得ADN,得率60%。由于ADN过度的产气速率,未添加稳定剂时不可熔融铸造。因此,当加入1%稳定剂MgO时,ADN较易熔铸[65]。固化成型时,体积收缩(体积的14%)大于TNT,在铸造时极易出现空隙与裂纹,但铸装ADN密度大于压装ADN和以TNT为基炸药密度。
|
Scheme 16 |
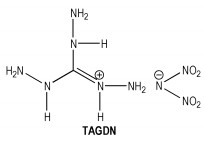
(2)三氨基胍二硝酰胺盐(TAGDN)
2003年,Niklas等人合成了TAGDN,结构式见Scheme 17。他们首先合成出二硝酰胺胍(GUDN),然后溶于二氧杂环已烷中,加热至回流,滴加水合肼制得目标产物。TAGDN密度为1.57 g·cm-3,生成焓184 kJ·mol-1,熔点85 ℃,分解温度150~160 ℃ (10 ℃·min-1)。由于其较低的火焰温度,TAGDN作为枪炮发射药比较合适。TAGDN的摩擦与撞击感度高,对摩擦作用极其敏感,所以在使用过程中需要严格的安全措施,它作为熔铸炸药载体的趋势较小[66-67]。
|
Scheme 17 |
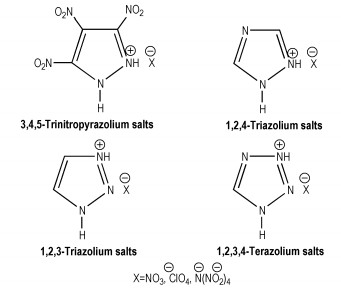
硝基唑类化合物可以和阴离子(例如,硝酸盐,高氯酸盐,二硝基胺等)生成低熔点熔铸含能盐材料。含能盐比非离子物质在物理性质上有许多优势,这些盐类物质比他们的非离子类似物蒸汽压低,密度高[68-70]。1, 2-二唑盐、1, 3-二唑盐、1, 2, 4-三唑盐、1, 2, 3-三唑盐、1-氨基-1, 2, 4-三唑盐、4-氨基-1, 2, 4-三唑盐、4-甲基-1-氨基-1,2, 4-三唑盐、1, 2, 3, 4-四唑盐这八种盐类化合物(部分结构式见Scheme 18)可以通过相似的反应条件得到,均可采用等量的唑类和强酸阴离子反应。硝酸盐、高氯酸盐、二硝基铵盐的熔程在70~110 ℃之间。1-甲基-4-氨基-1, 2, 4-三唑高氯酸盐(MATP)熔点和TNT接近,生成热也较高并且有好的氧平衡,这些性质可以提高熔铸炸药的性能。
|
Scheme 18 |
分子间炸药是由各为单独分子的氧化剂组分和可燃剂组分均匀混合组成的一类低共熔点的混合炸药。
近十多年来, 国内外研究的分子间炸药大致有以下几种类型:(1) EA系列分子间炸药(EA=乙二胺二硝酸盐/硝酸铵);(2)含NQ及MeNQ的分子间炸药;(3)含唑类硝基化合物的分子间炸药;(4)其他类型分子间炸药。
西安近代化学研究所在20世纪90年代初也首先研制出了代号分别为X-185和XR-185的非TNT基熔铸型分子间炸药。之后,对EA、EAK、NEAK等分子间炸药的配方、制备方法及各项性能指标进行了系统的研究[71-73],据报道该类炸药的能量密度较低。
4 其他的熔铸炸药载体2-甲基-4, 5-二硝基-1, 2, 3-三唑-3-氧化物(MDNTO),其熔点131~132 ℃,密度1.73 g·cm-3,分解温度256 ℃。
5 各种熔铸炸药载体性能对比对以上详述的16种熔铸炸药载体的部分性能进行了比较,结果见表 1,综合考虑表 1中所列熔铸炸药载体的爆轰性能,可以看出它们各有其优势,但也各有缺陷。在氮杂环唑类的炸药中DNP,MTNI,MTNP和TNAZ性能优良,是作为熔铸炸药载体替代TNT的较具潜力的候选物质。
| 表 1 各种熔铸炸药载体的性能 Tab.1 Performance for various of melt-cast explosive carriers |
(1) 由于感度较高,有毒性以及TNT类熔铸弹药存在的收缩、发脆等缺点,TNT已经不能满足现代军事对弹药的要求。
(2) 上述的四大类熔铸炸药载体是近20年来研究比较多的低熔点炸药,综合各类铸炸药载体的爆轰性能以及感度,可以看出DNP,MTNI,MTNP,TNAZ性能优良,是作为熔铸炸药载体替代TNT的较具潜力的候选物质。
(3) 进一步研究DNP,MTNI,MTNP,TNAZ等这些新型低熔点、高能钝感、相容性较好的熔铸炸药载体;开发新型复合型熔铸炸药载体,包括现有两种或多种熔铸炸药载体形成共熔物。
| [1] |
Ravi Pasupala, Dilip Badgujar M, Gore Girish M, et al. Review on melt cast explosives[J].
Propellants Explos Pyrotech, 2011, 36(5): 393-403. DOI:10.1002/prep.201100047 |
| [2] |
杜闪, 赵家乐, 李永祥, 等. 熔铸炸药载体的研究进展及其性能比较[J].
化工中间体, 2011, 08(6): 32-35. DU Shan, ZHAO Jia-le, LI Yong-xiang, et al. Study progress on melt-cast explosives carriers and comparition of their performance[J]. Chemical Intermediates, 2011, 08(6): 32-35. |
| [3] |
LI Yong-xiang, WANG Xiao-jun, WANG Jian-long. 1-Methyl-4, 5-dinitro-1H-imidazole[J].
Crystallography Journals, 2009, 65: o3073 |
| [4] |
LI Yong-xiang, DU Shan, WANG Jian-long. 3, 4-Dinitro-1H-pyrazole benzene 0.25-solvate[J].
Acta Cryst, 2011, 67(6): o1369 |
| [5] |
CAO Duan-lin, REN Fu-de, WANG Jian-long. Theoretical study on intermolecular interactions of 2, 4-dinitroimidazole with methanol[J].
Journal of Molecular Structure: THEOCHEM, 2007, 805(1-3): 53-60. DOI:10.1016/j.theochem.2006.09.024 |
| [6] |
ZHANG Qiao-ling, LI Yong-xiang. Characterization and thermolysis studies on novel compound: 3, 4-dinitropyrazole[J].
Journal of Beijing Institute of Technology, 2012, 21(1): 140-142. |
| [7] |
李永祥, 王建龙, 曹端林, 等. 4, 5-二硝基咪唑有机铵盐的制备[J].
火炸药学报, 2011, 34(3): 35-37. LI Yong-xiang, WANG Jian-long, CAO Duan-lin, et al. Synthesis of ammonium salt of 4, 5-dinitroimidazole[J]. Chinese Journal of Explosives & Propellants, 2011, 34(3): 35-37. |
| [8] |
杨克明, 曹端林, 李永祥, 等. 1-甲基-3, 5-二硝基-1, 2, 4-三唑的合成及表征[J].
含能材料, 2011, 19(5): 501-504. YANG Ke-ming, CAO Duan-lin, LI Yong-xiang, et al. Synthesis and characterization of 1 -methyl-3, 5-dininitro-1, 2, 4-triazole[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2011, 19(5): 501-504. |
| [9] |
杨克明, 曹端林, 李永祥, 等. 不敏感炸药1-甲基-3, 5-二硝基-1, 2, 4-三唑的研究进展[J].
化工中间体, 2010, 6(10): 15-18. YANG Ke-ming, CAO Duan-lin, LI Yong-xiang, et al. Progress in the Low Insensitive Explosive of 1-Methyl 3, 5-dininitro-1, 2, 4-triazole[J]. Chemical Intermediate, 2010, 6(10): 15-18. DOI:10.3969/j.issn.1672-8114.2010.10.008 |
| [10] |
杨克明, 曹端林, 李永祥, 等. 3, 5-二硝基-1, 2, 4-三唑盐的制备[J].
天津化工, 2011, 25(1): 18-20. YANG Ke-ming, CAO Duan-lin, LI Yong-xiang, et al. Preparation of 3, 5-dinitro-1, 2, 4-triazole salt[J]. TianJin Chemical Industry, 2011, 25(1): 18-20. |
| [11] |
宋磊, 王建龙, 李永祥, 等. 1-甲基-4, 5-二硝基咪唑的合成及表征[J].
含能材料, 2009, 17(5): 531-533. SONG Lei, WANG Jian-long, LI Yong-xiang, et al. Synthesis and characterization of 1-methy-4, 5-dinitroimidazole[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2009, 17(5): 531-533. |
| [12] |
宋磊, 王小军, 李永祥, 等. 不敏感炸药1-甲基-2, 4, 5-三硝基咪唑的合成[J].
天津化工, 2009, 23(4): 20-22. SONG Lei, WANG Xiao-jun, LI Yong-xiang, et al. Synthesis and characterizeation of 1-methyl-2, 4, 5-trinitroimidazole[J]. TianJin Chemical Industry, 2009, 23(4): 20-22. |
| [13] |
李永祥, 宋磊, 冉军鹏, 等. 1-甲基-2, 4, 5-三硝基咪唑合成工艺优化[J].
精细化工中间体, 2009, 39(3): 65-67. LI Yong-xiang, SONG Lei, RAN Jun-peng, et al. Optumization of synthesis of 1-methyl-2, 4, 5-trinitroimidazole[J]. Fine Chemical Intermediate, 2009, 39(3): 65-67. |
| [14] |
王小军, 曹端林, 李永祥, 等. 1-甲基-2, 4, 5-三硝基咪唑的合成新工艺[J].
火炸药学报, 2009, 32(3): 16-18. WANG Xiao-jun, CAO Duan-lin, LI Yong-xiang, et al. New technology for synthesis of 1-methyl-2, 4, 5-trinitroimidazoles[J]. Chinese Journal of Explosives & Propellants, 2009, 32(3): 16-18. |
| [15] |
王小军, 曹端林, 李永祥, 等. 不敏感炸药1-甲基-2, 4, 5-三硝基咪唑研究进展[J].
化工中间体, 2009, 10(3): 10-13. WANG Xiao-jun, CAO Duan-lin, LI Yong-xiang, et al. Progress in the low insensitive explosive of 1-methyl-2, 4, 5-trinitroimidazoles[J]. Chemical Intermediate, 2009, 10(3): 10-13. |
| [16] |
宋磊, 王建龙, 李永祥, 等. 1-甲基-4, 5-二硝基咪唑的合成及表征[J].
含能材料, 2009, 17(6): 678-680. SONG Lei, WANG Jian-long, LI Yong-xiang, et al. Synthesis and characterization of 1-methyl-4, 5-dinitroimidazole[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2009, 17(6): 678-680. |
| [17] |
杨国臣, 刘慧君, 曹端林. 4, 5-二硝基咪唑的制备[J].
含能材料, 2006, 14(5): 349-351. YANG Guo-chen, LIU Hui-jun, CAO Duan-Lin. Preprationof 4, 5-nitroimidazole[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2006, 14(5): 349-351. |
| [18] |
刘慧君, 杨林, 曹端林. 4-硝基咪唑的合成工艺及其热安定性[J].
中北大学学报, 2006, 27(4): 331-334. LIU Hui-jun, YANG Lin, CAO Duan-lin. Production of 4-nitroimidazole and its thermal stability[J]. Journal of North University of China (Natural Science Edition), 2006, 27(4): 331-334. |
| [19] |
曹端林, 刘慧君, 李永祥. 1, 4-二硝基咪唑的合成及其热分解[J].
火炸药学报, 2005, 28(3): 60-62. CAO Duan-lin, LIU Hui-jun, LI Yong-xiang. Synthesis and thermal decomposition of 1, 4-dinitromidazole[J]. Chinese Journal of Explosives & Propellants, 2005, 28(3): 60-62. |
| [20] |
刘慧君, 曹端林, 李永祥, 等. 2, 4-DNI的研究进展[J].
含能材料, 2005, 13(4): 269-272. LIU Hui-jun, CAO Duan-lin, LI Yong-xiang, et al. Progress in 2, 4-dinitroimidazole[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2005, 13(4): 269-272. |
| [21] |
刘慧君, 杨林, 曹端林. 由1, 4-DNI热重排制备2, 4-DNI的研究[J].
含能材料, 2005, 13(3): 141-143. LIU Hui-jun, ANG Lin, CAO Duan-lin. Preparation of 2, 4-dinitroimidazole by thermal rearrangement of 1, 4-DNI[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2005, 13(3): 141-143. |
| [22] |
Beanard P W, Fouche F C, Bezuidenhout H C. Less Sensitive TNT-based Formulations[C]//Australian Explosive Ordance Symposium (Parari′ 1997), Canberra, Australia, 1997: 12-14.
|
| [23] |
Doll Daniel W, Hanks Jami M, Allred Alan G, et al. Reduced sensitivity melt-pourable TNT replacements: US2003/0005988[P]. 2003.
|
| [24] |
Doll Daniel W, Hanks Jami M, Allred Alan G, et al. Reduced sensitivity melt-pourable Tritonal replacements: US2003/0140993[P]. 2003.
|
| [25] |
Doll Daniel W, Hanks Jami M, Highsmith Thomas K, et al. Reduced sensitivity melt-cast explosives: World: 01 /46092[P]. 2001.
|
| [26] |
王亲会. 熔铸混合炸药用载体炸药评述[J].
火炸药学报, 2011, 34(5): 25-28. WANG Qin-hui. Over view of carrier explosive for melt-cast composite explosive[J]. Chinese Journal of Explosives & Propellants, 2011, 34(5): 25-28. |
| [27] |
Agrawal J P, Hodgson R D.
Organic Chemistry of Explosives[M]. John Wiley & Sons, Chichester: 2007 |
| [28] |
谭彦威, 刘玉存, 杨宗伟, 等. 熔铸炸药的研究进展[J].
山东化工, 2011, 40(5): 22-24. TAN Yan-wei, LIU Yu-cun, YANG Zong-wei, et al. The current research of the melt-cast explosive[J]. Shandong Chemical Industry, 2011, 40(5): 22-24. |
| [29] |
Nicolich S, Niles J, Ferlazzo P, et al. Recent developments in reduced sensitivity melt pour explosives[C]//34th Int. Annual Con. ference of ICT, Karlsruhe, Germany, 2003: 24-27.
|
| [30] |
Fedorff B T.
Encyclopedia of Explosives and Related Items[M]. Picatany Arsenal, Dover, New Jersey, USA: 1960 |
| [31] |
Homewood R H, Krukonis V J, Loszewski R C, et al. Safe Explosive Containing Dicyanofuraxane and method: US Patent, 3832249[P]. 1974.
|
| [32] |
Mel′nikova T M, Novikova T S, Khmel′nitskii L I. Novel Synthesis of 3, 4-Dicyanofuroxan[J].
Mendeleev Commun, 2001, 11: 30-31. DOI:10.1070/MC2001v011n01ABEH001369 |
| [33] |
Coburn M D. Picrylamino-substituted Heterocycles. Ⅱ. Furazans[J].
J Heterocycl Chem, 1968, 5: 83-87. DOI:10.1002/jhet.v5:1 |
| [34] |
Coburn M D. N2, N4, N6-Tripicrylmelamine: US Patent 3414570[P], 1968.
|
| [35] |
Sheremetev A B, Ivanova E A, Spiridonova N P, et al. Desilylative nitration of C, N-disilylated 3-amino-4-methylfurazan[J].
Heterocycl Chem, 2005, 42: 1237-1242. DOI:10.1002/jhet.v42:6 |
| [36] |
Zheng W, Wang J N. Review of 3, 4-Bisnitrofuazanfuroxan[J].
Chin J Energ Mater, 2006, 6: 463-466. |
| [37] |
Zhou Y S, Zhang Z Z, Li J K, et al. Crystal structure of 3, 4-dinitrofurazanfuroxan[J].
Chin J Explos Propellants, 2005, 2: 43-46. |
| [38] |
Hu H, Zhang Z, Zhao F, et al. A Study on the properties and applications of high energy density material DNTF[J].
Acta Armamentarii, 2004, 2: 155-158. |
| [39] |
Wang Q. DNTF-based melt cast explosives[J].
Chin J Explos Propellants, 2003, 3: 57-59. |
| [40] |
Jin Rai Cho, Soo Gyeong Cho, Kwang Joo Kim, et al. A candidate of new insensitive high explosive MTNI [C]//Insensitive Munitions & Engergetic Materials Technology Symposium. Enschede, 2000: 393-400.
|
| [41] |
Shevelev S A, Dalinger I. Advances in nitropyrazole cherrustry[J].
Russ J Org Chem, 1998, 34: 1127-1136. |
| [42] |
Vingradov V M, Cherkasova T I, Dalinger I L, et al. Nitropyrazoles[J].
Russ Chem Bull, 1993, 42: 1552-1554. |
| [43] |
Jansse A M, Habraken C L. Pyrazoles.Ⅷ. Rearrangement of N-nitropyrazoles. Formation of 3-nitropyrazoles Ⅷ. Rearrangement of N-nitropyrazoles. Formation of 3-nitropyrazoles[J].
J Org Chem, 1971, 36: 3081-3084. DOI:10.1021/jo00820a004 |
| [44] |
Janssen A M, Koeners H J, Kruse C G, et al. Pyrazoles. XII. Preparation of 3(5)-nitropyrazoles by thermal rearrangement of N-nitropyrazoles[J].
J Org Chem, 1973, 38: 1777-1782. DOI:10.1021/jo00950a001 |
| [45] |
Latypov N V, Silevich V A, Ivanov P A, et al. Diazotization of aminonitro pyrazoles[J].
Chem Heterocycl Compd, 1976(2): 1355-1359. |
| [46] |
Katritzky A R, Scriven E F V, Majundar S, et al. Direct nitration of five-membered heterocycles[J].
A RKIVOC, 2005(3): 179-191. |
| [47] |
Ravi P, Reddy C K, Saikia A, et al. Nitrodeiodination of polyiodopyrazoles[J].
Propellants, Explos, Pyrotech, 2012, 37(2): 167-171. DOI:10.1002/prep.v37.2 |
| [48] |
Giles D, Parnell E W, Renwick J D. Some iodinated pyrazole derivatives[J].
J Chem Soc C, 1966: 1179-1184. DOI:10.1039/j39660001179 |
| [49] |
Herve G, Roussel C, Graindorg H. Selective preparation of 3, 4, 5-trinitro-lH-pyrazole: A stable all-carbon-nitrated arene[J].
An gew Chem Int Ed, 2010, 49: 3177-3181. DOI:10.1002/anie.v49:18 |
| [50] |
Herve G. Dinitropyrazole Derivatives. Their Preparation and Energetic Compositions Comprising Them: US Patent 200901016931[P], 2009.
|
| [51] |
Surapaneni R. Insensitive High Energy Materials[C]//7th High Energy Materials Conference and Exhibit (HEMCE-2007). 2009: 7-9.
|
| [52] |
Pepekin V I. Limiting detonation velocities and limiting propelling powers of organic explosives[J].
Doklady Physical Chemistry, 2007, 414(2): 159-161. DOI:10.1134/S0012501607060103 |
| [53] |
Simpson R L, Garza R G, Foltz M F, et al. Characterization of TNAZ, Report UCRL-ID-119572[R]. Lawrence Livermore National Laboratory, Livermore, CA, USA, 1994.
|
| [54] |
Doali J O, Fifer R A, Kruezynski D I, et al. Technical Report No. BRL-MR-378/5[R]. US Ballistic Research Laboratory, Aberdeen Proving Ground, MD, USA, 1989.
|
| [55] |
Chung Kyoo-Hyun, Pyun Doo-Hyuk, Chu-Kook. A study on the synthesis of a key intermediate for TNAZ[J].
Kongop Hwahak, 2001, 12(2): 224-228. |
| [56] |
Sikder N, Sikder A K, Bulakh N R, et al. 1, 3, 3-Trini-troazetidine(TNAZ), a melt-cast explosive: synthesis, characterization and thermal behavior[J].
Hazardous Materials, 2004, 113(1-3): 35-43. DOI:10.1016/j.jhazmat.2004.06.002 |
| [57] |
Chavez D E, Hiskey M A, Naud D L, et al. Synthesis of an energetic nitrate ester[J].
Angew Chem, 2008, 120(43): 8431-8433. DOI:10.1002/ange.v120:43 |
| [58] |
Altenburg T, Klapotke T M, Penger A. Primary nitramines related to nitroglycerine: l-Nitramino-2, 3-dinitroxypropane and 1, 2, 3-trinitraminopropane[J].
Eur J Energ Mater, 2010, 6: 255-276. |
| [59] |
Rossi M J, Bottaro J C, McMillen D F. The Thermal decomposition of the new energetic material ammoniumdinitramide (NH4N(NO2)2) in relation to nitramide (NH2NO2) and NH4NO3[J].
Int J Chem Kinet, 1993, 25(7): 549-570. DOI:10.1002/(ISSN)1097-4601 |
| [60] |
Brill T B, Brush P J, Patil D G. Thermal decomposition of energetic materials 58. chemistry of ammonium nitrate and ammonium dinitramide near the burning surface temperature[J].
Combust Flame, 1993, 92(1-3): 178-186. |
| [61] |
Medel A M, Lin M C, K Melius Morokuma C F. Theoretical study of the gas-phase structure, thermochemistry and decomposition mechanisms of NH4NO2 and NH4N(NO2)2[J].
J Phys Chem, 1995, 99(18): 6842-6848. DOI:10.1021/j100018a015 |
| [62] |
Martin A, Pinkerton A A, Gilardi R D, et al. Energetic materials-the preparation and structural characterization of three bisguanidinium dinitramides[J].
Acta Crystallogr Sect B, 1997, 53: 504-5012. |
| [63] |
Bottaro J C, Penwell P E, Schmitt R J. A new synthesis of alkyl-N, N-dinitramines by direct nitration of isocyanates[J].
Synth Commun, 1991, 21(7): 945-949. DOI:10.1080/00397919108019779 |
| [64] |
Hatano H, Onda T, Shiino K, et al. New synthetic method and properties of ammonium dinitramide[J].
Kayaku Gakkaishi, 1996, 57(4): 160-165. |
| [65] |
Hahma A, Edinsson E, Ostmark H. The properties of ammonium dinitramine (ADN): Part 2: melt casting[J].
J Energ Mater, 2010, 28(2): 114-138. |
| [66] |
Bathelt H, Volk F, Weindel M. ICT-Thermochemical Database, Version 3. 0, Fraunhofer-Institut fur Chemische Technologie[CP]. Pfinztal/Berghausen, Germany, 2001.
|
| [67] |
Wingborg N, Latypov N V. Triaminoguanidine dinitramide (TAGDN): synthesis and characterization[J].
Propellants Explos Pyrotech, 2003, 28(6): 314-318. |
| [68] |
Drake G W. Energetic Triazolium Salts: US Patent 6, 509, 473[P], 2003.
|
| [69] |
Kaplan G, Drake G W, Tollison K, et al. Synthesis characterization, and structural investigations of 1-amino-3-substituted 1, 2, 3-triazolium salts, and a new route to 1-substituted 1, 2, 3-triazoles[J].
J Heterocycl Chem, 2005, 42: 19-27. |
| [70] |
Xue H, Gao Y, Twamley B, et al. New energetic salts based on nitrogen-containing heterocycles[J].
Chem Mater, 2005, 17(1): 191-198. DOI:10.1021/cm048864x |
| [71] |
张亦安, 杜振华. 分子间炸药的研究概况发展趋势和关键技术[J].
火炸药学报, 1989(4): 24-33. ZHANG Yi-an, DU Zheng-hua. Development trend and key technology of intermolecular explosive[J]. Chinese Journal of Explosives & Propellants, 1989(4): 24-33. |
| [72] |
赵省向, 张亦安, 胡焕性, 等. EAK分子间炸药的热分解[J].
火炸药学报, 1999, 22(4): 24-26. ZHAO Xing-xiang, ZHANG Yi-an, HU Huan-xing, et al. Thermal decomposition of EAK intermolecular explosive[J]. Chinese Journal of Explosives & Propellants, 1999, 22(4): 24-26. |
| [73] |
赵省向, 张亦安, 王晓峰, 等. EAK基熔铸分子间炸药的能量和撞击感度[J].
火炸药学报, 2004, 27(3): 29-41. ZHAO Xing-xiang, ZHANG Yi-an, WANG Xiao-feng, et al. Thermal decomposition of EAK intermolecular explosive[J]. Chinese Journal of Explosives & Propellants, 2004, 27(3): 29-41. |
The current research situation at home and abroad of four types of explosives which can be used as carriers for melt-cast explosive were summarized.




