以TNT为液相载体的熔铸炸药是目前应用最广泛的军用混合炸药[1-2], 但TNT能量相对较低, 严重影响了熔铸炸药整体的威力[3-5], 因此寻找一种能量较高, 而且熔点能满足要求的液相载体成了人们关注的焦点[6-9]。
美国以43.5%甲基硝基胍(MeNQ)、36%硝酸铵(AN)、10.5%硝基胍(NQ)、10%高氯酸铵(AP)配制出MeNQ基低共熔物, 已作为非TNT基熔铸炸药液相载体应用于美国AFX-453航弹中, 但相关动力学的研究报道较少, 更无熔融动力学的文献报道[10-11]。本课题组根据上述配方制备出MeNQ基低共熔物, 采用差示扫描量热仪(DSC)对其进行详细的热分析实验研究, 获得了低共熔物的熔融曲线, 分析探讨了不同升温速率, 不同气氛以及不同添加剂条件下低共熔物的熔融特性, 并借助反应动力学相关概念, 结合熔融曲线, 计算了低共熔物熔融反应动力学, 得到了低共熔物熔融反应动力学参数, 以期相关研究结果可以为TNT替代物的改性研究提供参考依据。
2 实验部分 2.1 试剂与仪器原材料:甲基硝基胍(MeNQ),江苏天泽化工有限公司, 分析纯; 硝基胍(NQ),中物院化材所自制, 纯度大于99%;硝酸铵(AN)和高氯酸铵(AP),成都化学试剂有限公司, 均为分析纯; 2, 2′, 4, 4′, 6, 6′-六硝基均二苯基乙烯(HNS)和1, 3, 5-三硝基-1, 3, 5-三氮杂环辛烷(RDX),西安近代化学研究所提供的标准物质。
仪器: PerkinElmer的Diamond差示扫描量热仪(DSC)。
2.2 实验过程样品制备:分别称取17.42 g MeNQ, 14.40 g AN, 4.20 g NQ, 4.00 g AP混合后放入110 ℃的油浴中加热熔化, 搅拌使液体混合均匀后取出置于空气中密封冷凝。将冷凝后的MeNQ基低共熔物研磨后置于称量瓶中备测。
实验条件:将样品盛装在铂坩埚内, 分别在N2和静态空气的条件下, 采用程序升温法以不同的升温速率(30, 20, 10, 5 ℃·min-1), 在50~150 ℃温度范围内加热样品。计算机采集DSC信号的同时对基线进行自动校正、计算峰面积、反应起始温度等; 气体流速约为30 mL·min-1; 试样量约4.2 mg。
3 结果与讨论低共熔物熔融是一种复杂的物理化学反应, 目前很难对其机理进行准确描述。不同的外界条件下, 同一化学组成的物质可能具有不同的晶型, 随着温度的变化, 晶体会由一种晶型转变为另一种晶型, 当温度继续升高至一定程度后, 固相自由能会高于液相自由能, 使得固相变得不稳定, 从而发生熔融相变。
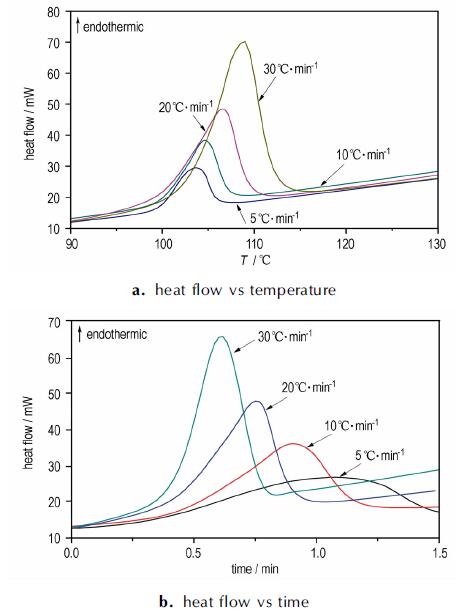
3.1 升温速率对MeNQ基低共熔物熔融的影响为了研究升温速率对MeNQ基低共熔物熔融过程的影响, 在N2气氛中采用5,10,20,30 ℃·min-1四种升温速率进行实验, 图 1为不同升温速率下MeNQ基低共熔物熔融反应曲线。由图 1a可知, 随着升温速率的提高, 熔融反应开始时间和峰值都有相应的延迟, 反应最大速率处温度从5 ℃·min-1时的103.6 ℃延迟到30 ℃·min-1时的108.8 ℃。通过坐标变换把图 1a的热流-温度关系变为热流-时间关系[12-15], 如图 1b所示。从图 1b上可以发现随着升温速率的增加, 熔化时间缩短, 即随着升温速率的增加, MeNQ基低共熔物的熔化速率增加。
|
图 1 不同升温速率下低共熔物的DSC曲线 Fig.1 DSC curves of eutectic at different heating rate |
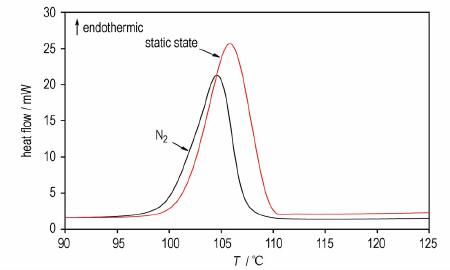
为了研究气氛对MeNQ基低共熔物熔融特性的影响, 10 ℃·min-1的升温速率下分别在静态(不通气)和惰性气氛(N2)下对样品进行熔融热分析实验, 结果如图 2所示。
|
图 2 不同气氛下低共熔物的DSC曲线(10 ℃·min-1) Fig.2 DSC curves of eutectic in N2 and static state at 10 ℃·min-1 |
由图 2分析发现,气氛对MeNQ基低共熔物熔融过程有轻微影响, 在10 ℃·min-1的加热速率下, 不通气体(静态)的情况下低共熔物开始熔融的温度比惰性气氛下要高2℃, 反应峰值处温度高约2℃, 原因在于惰性气氛下样品池中的温度分布更均匀, 使样品更容易受热熔化[16]。
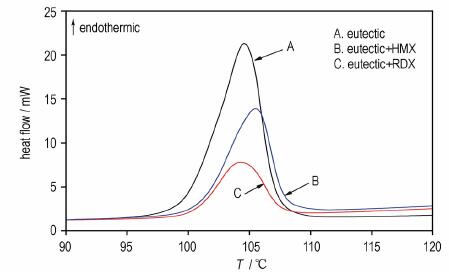
3.3 添加剂的影响国内外许多研究者认为, 在TNT或TNT系列低共熔物中添加一定比例的HMX、HNS或RDX能够降低其结晶过程中的过冷度, 消除自加热[16-19]。同时也有研究表明合适的添加剂可使一些低共熔物的熔点下降, 降低熔融处理的实现难度, 这在工程上很有意义。图 3为添加HMX、HNS后MeNQ基低共熔物的DSC曲线。由图 3可知, 添加HNS和RDX后, 熔融峰后移, 表明添加高能的RDX、HNS等不能促进MeNQ基低共熔物的熔融。这可能是因为HNS能够与TNT形成(TNT)2·HNS络合物, 抑制TNT过冷, 并产生大量晶核改善TNT的结晶性能, 进而降低TNT系列共熔物的熔点, 但它们不能与MeNQ形成络合物, 也无弱相互作用, 从而无法促进MeNQ基低共熔物的熔融。
|
图 3 不同添加剂下低共熔物的DSC曲线 Fig.3 DSC curves of eutectic at different additives |
国内外对低共熔物的结晶行为进行了广泛的研究, 但未见MeNQ基低共熔物熔融动力学的研究报导。本研究在热分析实验基础上尝试对MeNQ基低共熔物的熔融动力学进行探讨[14]:当反应进行的程度与放热或吸热效应成正比, 即反应进程与DSC曲线与基线围成的面积成正比时, 就可以利用DSC数据建立动力学方程。S′为t时刻熔融DSC曲线与基线围成的面积, S为反应全过程DSC与基线围成的面积。由于DSC测得的是热流数据dH/dt, 所以S即为反应的热效应。
任意时刻, 反应的转变分数可以表示为此时热效应占总热效应的分额[12]:
| $ \alpha = \frac{H}{{{H_0}}} = \frac{{S'}}{S} $ | (1) |
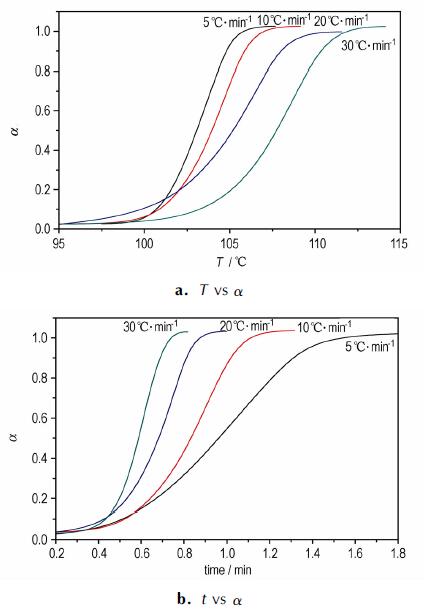
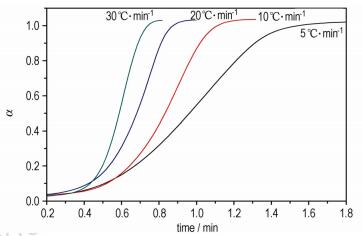
式中, α为反应物转化率; H为该时刻反应热效应累积值, kJ·mol-1; H0为反应的总热效应, kJ·mol-1。将图 1的DSC曲线进行积分处理, 可以获得如图 4所示的转化率α与温度T和时间t的关系。
|
图 4 不同升温速率下低共熔物的转化率曲线 Fig.4 Conversion rate curves of eutectic at different heating rate |
MeNQ基低共熔物熔融反应机理函数可表示为:
| $ f\left( \alpha \right) = {\left( {1-\alpha } \right)^n} $ | (2) |
将转化率对时间微分,可得任意时刻的反应速率[12]:
| $ \frac{{{\rm{d}}\alpha }}{{{\rm{d}}t}} = \frac{1}{{{H_0}}}\frac{{{\rm{d}}H}}{{{\rm{d}}t}} = {k_0}{\left( {1-\alpha } \right)^n} $ | (3) |
式中, n为反应级数; k0为反应速率常数, 按照Arrhenius公式写为[20]:
| $ {k_0} = A{e^{-\frac{{{E_{\rm{a}}}}}{{RT}}}} $ | (4) |
式中, A为指前因子, s-1; Ea为反应表观活化能, kJ·mol-1, 合并式(3)、(4), 则有:
| $ \frac{1}{{{H_0}}}\frac{{{\rm{d}}H}}{{{\rm{d}}t}} = A{e^{-\frac{{{E_{\rm{a}}}}}{{RT}}}}{\left( {1-\alpha } \right)^n} $ | (5) |
根据Satava方法, 对其熔融反应机制, 即反应级数n的判定时引入积分形式动力学机理函数[21]
| $ G\left( \alpha \right) = {k_0}t $ | (6) |
它与微分形式机理函数之间的关系为[20]
| $ G\left( \alpha \right) = \int_0^\alpha {f{{\left( \alpha \right)}^{-1}}{\rm{d}}\alpha } $ | (7) |
对于正确的机理函数f(α)所对应的G(α), 应当满足ln[G(α)]是1/T的线性函数[7]。利用实验数据与不同n值(n = 0, 1/2, 2/3, 1, 2)的机理函数进行拟合, 结果见图 5。不难看出, 在较宽的温度范围内, 当n=1/2时ln[G(α)]对1/T有良好的线性关系, 所以MeNQ基低共熔物的熔融过程可以由1/2级反应动力学方程来描述。

|
图 5 ln[G(α)]与1/T关系曲线 Fig.5 Curves of ln[G(α)] vs 1/T |
由Kissinger方程:
| $ \ln \frac{\beta }{{T_{\rm{p}}^2}} = \ln \frac{{AR}}{{{E_{\rm{a}}}}}-\frac{{{E_{\rm{a}}}}}{{R{T_{\rm{p}}}}} $ | (8) |
可获得MeNQ基低共熔物的熔融动力学常数Ea和A(表 1)。式中,β为反应速率, ℃·min-1; R为气体常数, J·mol-1·K-1; Tp为峰顶温度, K。
| 表 1 低共熔物熔融反应动力学参数 Tab.1 Kinetic parameters of melting reaction for eutectic |
从表 1数据可见, 升温速率从5 ℃·min-1增大到30 ℃·min-1, 熔融动力学常数Ea仅从11.74 kJ·mol-1增大到11.91 kJ·mol-1, A也仅从3364.19 s-1增大到3412.91 s-1, 即增大升温速率, MeNQ基低共熔物的熔融动力学常数Ea和A基本无变化。
4 结论(1) MeNQ基低共熔物熔融是一个吸热过程, 升温速率提高, 熔融反应后移。
(2) 气氛对MeNQ基低共熔物熔融有一定影响, 较惰性气氛而言, 静态条件下熔融反应移向更高温度。
(3) 实验样品中添加RDX、HNS后, 低共熔物的熔点升高, 说明高能RDX、HNS等不能促进MeNQ基低共熔物的熔融。
(4) MeNQ基低共熔物熔融过程可以用1/2级反应动力学方程来描述, 升温速率从5 ℃·min-1增加到30 ℃·min-1, 熔融动力学常数Ea仅从11.74 kJ·mol-1增大到11.91 kJ·mol-1, A也仅从3364.19 s-1增大到3412.91 s-1, 即增大升温速率, MeNQ基低共熔物的熔融动力学参数几乎不发生变化。
总之, MeNQ基低共熔物熔融是一个非常复杂的物理化学过程, 本研究仅在动力学方面进行了初步探索, 较为精确的反应机理还有待于进一步研究。
| [1] |
舒远杰, 霍冀川.
炸药学概论[M]. 北京: 化学工业出版社, 2011: 115-126.
|
| [2] |
刘萍, 许西宁, 尹孟超. 梯恩梯撞击安全性试验研究与评述[J].
火炸药学报, 1999(2): 19-24. LU Ping, XU Xi-ning, YIN Meng-chao. Test Research and Comment on Impact Safety of TNT[J]. Chinese Journal of Explosives & Propellants, 1999(2): 19-24. |
| [3] |
曹欣茂. 国外B炸药改性技术重要进展[J].
火炸药, 1994(3): 35-40. |
| [4] |
黄亨建, 董海山, 张明. B炸药的改性研究及其进展[J].
含能材料, 2001, 9(4): 183-186. HUANG Heng-jian, DONG Hai-shan, ZHANG Ming. Problems and developments in composition B modification research[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2001, 9(4): 183-186. |
| [5] |
XU Rui-juan, LUO Hong, WANG Xin-feng. Effect of additives on the modified composition B[J].
Chinese Journal of Explosives & Propellants, 2003, 26(2): 5-7. |
| [6] |
张光全, 董海山. 2, 4-二硝基苯甲醚为基熔铸炸药的研究进展[J].
含能材料, 2010, 18(5): 604-609. ZHANG Guang-quan, DONG Hai-shan. Review on melt-castable explosives based on 2, 4-dinitroanisole[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2010, 18(5): 604-609. |
| [7] |
张志忠, 王伯周, 姬月萍, 等. 部分新型高能量密度材料的国内研究进展[J].
火炸药学报, 2008, 31(2): 93-97. ZHANG Zhi-zhong, WANG Bo-zhou, JI Yue-ping, et al. Study progress of several high energy density materials (HEDM)[J]. Chinese Journal of Explosives & Propellants, 2008, 31(2): 93-97. |
| [8] |
李洪珍, 舒远杰, 黄弈刚, 等. 高能量密度材料1, 3, 3-三硝基氮杂环丁烷研究进展[J].
化学研究与应用, 2003, 15(1): 111-115. LI Hong-zheng, SHU Yuan-jie, HUANG Yi-gang, et al. Research progress in high energy density material 1, 3, 3-trinitroazetidine[J]. Chemical Research and Application, 2003, 15(1): 111-115. |
| [9] |
杜闪, 赵家乐, 李永祥, 等. 熔铸炸药载体的研究进展及其性能比较[J].
化工中间体, 2011(6): 32-35. DU Shan, ZHAO Jia-le, LI Yong-xiang, et al. Study progress on melt-cast explosives carriers and comparision of their performance[J]. Chemical Intermediate, 2011(6): 32-35. |
| [10] |
Michael A P, Stephen A A, Intermolecular Complex Explosives: USP 4948438[P], 1990.
|
| [11] |
张光全, 董海山. MeNQ的合成进展及其在熔铸炸药中的应用[J].
含能材料, 2008, 16(3): 353-355. ZHANG Guang-quan, DONG Hai-shan. Synthesis progress and application of N-Methyl-N'-nitroguanidine in melt/cast explosives[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2008, 16(3): 353-355. |
| [12] |
李润东, 池涌, 王雷, 等. 城市垃圾焚烧飞灰熔融动力学研究[J].
浙江大学学报, 2002, 36(5): 498-503. LI Run-dong, CHI Yong, WANG Lei, et al. Kinetic study of MSW incineration fly ash melting by DSC-DTA[J]. Journal of Zhejiang University, 2002, 36(5): 498-503. |
| [13] |
赵永椿, 张军营, 田冲, 等. 基于矿物质定量热分析的灰熔融反应动力学[J].
工程热物理学报, 2010, 31(3): 531-534. ZHAO Yong-chun, ZHANG Jun-ying, TIAN Chong, et al. Study on ash melting dynamic based on mineral quantitative thermo-analysis[J]. Journal of Engineering Thermophysics, 2010, 31(3): 531-534. |
| [14] |
胡荣祖, 史启祯.
热分析动力学[M]. 北京: 科学出版社, 2001: 47-64.
HU Rong-zu, SHI Qi-zhen. Kinetics of Thermal Analysis[M]. Beijing: Science Press, 2001: 47-64. |
| [15] |
李化启, 马瑞, 梁一泓, 等. 动态熔融过程中辉长岩主要矿物的熔融序列及其熔融动力学研究[J].
岩石学报, 2005, 21(6): 1749-1757. LI Hua-qi, MA Rui, LIANG Yi-hong, et al. Melting sequence and dynamics of the major minerals of gabbro in the process of dynamic melting[J]. Acta Petrologica Sinica, 2005, 21(6): 1749-1757. |
| [16] |
周文静, 张皋, 刘子如. DNTF、TNT和DNTF-TNT低共熔物在RDX中的结晶动力学研究[J].
含能材料, 2008, 16(3): 267-271. ZHOU Wen-jing, ZHANG Gao, LIU Zi-ru. Kinetics of non-isotherma l crystallizations of DNTF, TNT and DNTF-TNT eutectic system crystallization in RDX[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2008, 16(3): 267-271. |
| [17] |
周文静, 覃光明, 张皋, 等. DNTF的非等温结晶研究—I.在HMX中的结晶动力学[J].
含能材料, 2007, 15(6): 629-632. ZHOU Wen-jing, QIN Guang-ming, ZHANG Gao, et al. Non-isothermal crystallization of DNTF: I. crystallization kinetics in HMX[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2007, 15(6): 629-632. |
| [18] |
周文静, 刘子如, 张皋, 等. DNTF的非等温结晶研究(Ⅱ)在RDX中的结晶动力学[J].
含能材料, 2008, 16(1): 16-19. ZHOU Wen-jing, LIU Zi-ru, ZHANG Gao, et al. Behavior of non-isothermal crystallization of DNTF (Ⅱ): crystallization kinetics in RDX[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2008, 16(1): 16-19. |
| [19] |
周文静, 张皋, 刘子如. TNT在HMX和RDX中的非等温结晶动力学[J].
火炸药学报, 2008, 31(1): 34-37. ZHOU Wen-jing, ZHANG Gao, LIU Zi-ru. Non-isothermal crystallization kinetics of TNT in HMX and RDX[J]. Chinese Journal of Explosives & Propellants, 2008, 31(1): 34-37. |
| [20] |
傅献彩.
物理化学[M]. 北京: 高等教育出版社, 1990: 357-402.
FU Xian-cai. Physical Chemistry[M]. Beijing: High Education Press, 1990: 357-402. |
| [21] |
Satava V. Mechanism and kinetics from non-isothermal TG traces[J].
Thermochimica Acta, 1971, 2(5): 423-428. DOI:10.1016/0040-6031(71)85018-9 |
The melting process of eutectic based on methyl-nitroguanidine(MeNQ) was studied by differential scanning calorimetry at 50~150 ℃ under different atmosphere(static state and N2) and heating rates(5,10,20,30 ℃·min-1).




