2. 盐城师范学院, 江苏 盐城 224002
2. Yancheng Teachers College, Yancheng 224002, China
以含能化合物为配体合成有一定爆炸性能的含能配合物, 可用作军用、民用火工品、爆破器材的起爆药及含能催化剂[1-3]。Ritter和Licht[4]以2, 6-二氨基吡啶为原料, 通过硝化和氧化得到2, 6-二氨基-3, 5-二硝基吡啶-1-氧化物(ANPyO), 结构与TATB相似, 是一种新型的高能钝感炸药, 具有含氮量高、稳定性好、感度低、能量高等优点, 可以与铜、镍、钴等过渡金属形成含能配合物[5-7]。
目前, 对炸药热分解或推进剂燃烧性能的催化剂主要为惰性催化剂, 常用的有铜、铅、铁、铬、钛、铋、锡的氧化物, 它们虽能起着有效的催化作用, 却降低了推进剂体系的能量密度。含能催化剂本身具有较高能量, 催化作用的同时也为系统提供一定能量。可拓宽推进剂燃速范围、降低压力指数及特征信号, 是今后新型高效含能燃烧催化剂的一个主要发展方向[8-9]。黑索今(RDX)、奥克托今(HMX)和高氯酸铵(AP)为发射药和固体推进剂的重要组分, 其热分解特性直接影响推进剂的燃烧性能[10-14]。因此研究催化剂对RDX、HMX和AP热分解的催化作用具有重要意义。
本研究以ANPyO为配体, 选择铬、锌过渡金属为中心离子合成出两种含能配合物, 通过红外、元素分析、DSC、TG-DTG分析了两种配合物的组成及热分解性能, 研究了目标配合物对固体推进剂主要组分RDX、HMX和AP热分解的影响, 初步测试了其用作推进剂含能催化剂的可能性。
2 实验部分 2.1 试剂与仪器ANPyO为实验室合成[15], 为黄色粉末状小颗粒, 密度为1.888 g·cm-3, 熔融分解点大于340 ℃。N, N-二甲基甲酰胺(DMF)、CrCl3·3H2O、无水乙醇、Zn(CH3COO)2·2H2O, 均为市售化学纯或分析纯产品。RDX、HMX和AP, 南京东诺工业炸药高科技有限公司。
DSC823e差示扫描量热仪(瑞士METTLERTOLED公司), 试样量约为1.0 mg, 升温速率为20 K·min-1, 测试温度区间50~500 ℃, N2流量为30 mL·min-1; 热重分析仪(瑞士METTLER TOLEDO TGA/SDTA851e热分析仪), 试样量约为1.0 mg, 升温速率为20 K·min-1, 测试温度区间50~800 ℃, N2流量为30 mL·min-1; MAGNA-760型傅里叶变换红外光谱分析仪(KBr压片)(美国N ICOLET公司); 德国Vario EL Ⅲ CHNOS元素分析仪。
2.2 实验过程 2.2.1 Cr(Ⅲ)配合物的合成取0.215 g(1.0 mmol)三氟乙酸重结晶的ANPyO加入25 mL DMF中, 搅拌, 直接升温至90 ℃, 得到澄清的黄色溶液; 取0.09 g(0.33 mmol)CrCl3·3H2O溶于20 mL无水乙醇中, 然后逐渐加入溶ANPyO的DMF溶液中, 搅拌, 回流, 1 h后溶液变为黑色澄清溶液。冷却, 转移至烧杯中静止, 一周后烧杯底部有黑褐色晶体析出, 用蒸馏水清洗三次, 烘干, 得到0.102 g黑褐色晶状固体, 收率为44.16%。
2.2.2 Zn(Ⅱ)配合物的合成将0.215 g (1.0 mmol)三氟乙酸重结晶的ANPyO固体粉末分散在30 mL DMF中, 悬浮液体呈光亮的黄色。搅拌下, 将0.11 g(0.5 mmol)固体乙酸锌Zn(CH3COO)2·2H2O加入其中, 升温至80 ℃, 回流1.5 h, 得到黄色澄清溶液。将其加入100 mL冰水中, 有大量乳黄色粉末析出, 过滤, 用蒸馏水清洗三次, 烘干, 得到0.252 g乳黄色粉末固体, 收率为78.87%。
3 结果与讨论 3.1 配合物组成分析ANPyO及Cr(Ⅲ)和Zn(Ⅱ)两种配合物的红外曲线如图 1所示, 元素分析结果见表 1。

|
图 1 ANPyO及其配合物的FT-IR谱 Fig.1 FT-IR spectra of ANPyO and its complexes |
| 表 1 ANPyO及其配合物的元素分析 Tab.1 Elemental analysis of ANPyO and its complexes |
由图 1可知, 两种配合物的红外光谱相对ANPyO吸收峰强度和吸收频率发生了变化, 其中氨基(—NH2)的主要特征吸收峰变化表现得尤为显著, 由原先ANPyO中氨基的双强峰, 变为配合物中的单峰和三重峰。这就说明, 配体中的氨基参与了配位, 从而减弱了氨基N原子上的电子密度, 红外光谱发生了重要改变, 形成了配位化合物。
由表 1可见, 配体和配合物元素分析的计算值与实测值吻合。由文献[5]的单晶晶体结构可知, 作为双齿配体, ANPyO以分子中氮氧基的O原子和邻位的一个氨基N原子与金属离子配位, 其中参与配位的氨基失去了一个H原子, 生成的配合物中没有外接阴离子。根据金属配位方式, Cr(Ⅲ)和Zn (Ⅱ)大都为六配位, 再由元素分析和TG实验结果, 推断出配合物的分子式: Cr(Ⅲ)配合物的分子式为Cr(C5N5O5H4)3; Zn(Ⅱ)配合物的分子式为Zn(C5N5O5H4)2(DMF)2。
3.2 热分解分析ANPyO及Cr(Ⅲ)和Zn(Ⅱ)两种配合物在20 K·min-1线性升温条件下的DSC和TG-DTG曲线如图 2所示。

|
图 2 ANPyO及其配合物的DSC和TG-DTG曲线(β = 20K·min-1) Fig.2 DSC and TG-DTG curves of ANPyO and its complexes at 20 K·min-1 |
图 2a表明, 配体ANPyO有一个缓慢的吸热过程和一个剧烈的放热分解过程, 吸热过程始于200 ℃, 终于345℃, 峰温为338.32 ℃, 为ANPyO的熔融吸热峰; 分解放热峰温为356.46 ℃, 终于500 ℃。在其TG-DTG曲线(图 2d)上同样显示为一急剧的质量损失过程, 始于200 ℃, 终于360 ℃, 最大失重速率出现在338.14 ℃, 最后无残渣剩余。
图 2b表明, Cr(Ⅲ)配合物在50~500 ℃主要有一个放热峰, 始于200 ℃, 终于400 ℃, 峰温为326.93 ℃。由其TG-DTG曲线(图 2e)可知, Cr(Ⅲ)配合物的热分解失重过程分为两个阶段, 第一阶段为剧烈失重阶段, 开始于150 ℃左右, 结束于390 ℃, 质量损失达57.69%, 最大失重率发生在321.02 ℃。推测这一阶段为配合物骨架断裂, 配体ANPyO受热分解, 生成新的中间混合体。第二阶段为一缓慢失重阶段, 由390 ℃开始, 结束于750 ℃, 失重率为31.52%, 推测这一阶段为生成的中间体混合物受热继续分解, 最终生成金属氧化物。第一、二阶段的最终失重率达89.21%, 剩余残渣的质量分数为10.79%, 与计算得到的最终产物为Cr2O3的理论值10.95%相符, 因此推测剩余残渣为Cr2O3。
图 2c表明, Zn(Ⅱ)配合物的热分解过程有两个连续的放热峰, 发生在360~450 ℃, 峰温分别为395.55 ℃和414.79 ℃。其TG-DTG曲线(图 2f)表明, Zn(Ⅱ)配合物于100~700 ℃的热分解质量损失过程分为两个阶段, 第一阶段为剧烈质量损失过程, 失重率为67.88%, 终于400 ℃, 最大失重率发生在394.21 ℃, 推测这一阶段为配合物骨架断裂, 配位的ANPyO与DMF分子受热分解, 生成新的中间混合体; 随着温度的升高, 配合物继续失重, 直至700 ℃, 失重率为19.44%, 剩余残渣的质量分数为12.68%, 与计算得到的最终产物为ZnO的理论值12.67%符合, 因此推测剩余残渣为ZnO。
3.3 催化性能研究 3.3.1 对RDX热分解催化作用将RDX与两种配合物均按3:1的质量比混合, 测定RDX混合物前后的DSC曲线, 结果如图 3所示。
|
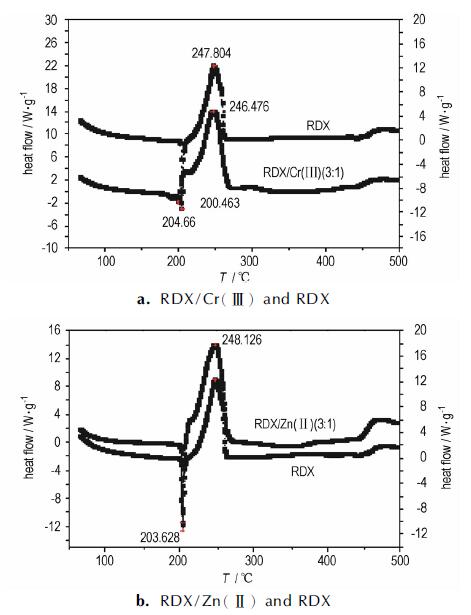
图 3 RDX与RDX/配合物的DSC曲线(β = 20 K·min-1) Fig.3 DSC curves of RDX and RDX/complexes with mass ratio of 3:1 at 20 K·min-1 |
由图 3可见, 纯品RDX的热分解主要包括1个吸热过程和1个放热过程。吸热峰发生在195~215 ℃, 峰温为204.66 ℃, 熔化吸热焓为143.73 J·g-1; 随着温度的升高, 出现一个较剧烈的放热分解峰, 发生在215~270 ℃, 峰温为247.80 ℃, 对应的RDX的分解放热量为1362.67 J·g-1。RDX与配合物混合后, 其吸热峰和放热峰的峰形和峰温基本没有变化, 其中Cr(Ⅲ)配合物与RDX混合物吸热峰峰顶温度(200.46 ℃)比纯RDX的吸热峰提前4.20 ℃, 放热峰峰顶温度(246.48 ℃)比纯品RDX放热峰提前1.32 ℃, 分解放热量从1362.67 J·g-1增至1669.02 J·g-1; Zn(Ⅱ)配合物与RDX混合物吸热峰峰顶温度与放热峰峰顶温度比纯品RDX相比基本没有变化, 仅分解放热量从1362.67 J·g-1增至1771.81 J·g-1。由此可见, 两种配合物对RDX的高温分解峰温影响较小, 仅能使RDX放热量增加, 对RDX热分解影响不大。
3.3.2 对HMX热分解催化作用将HMX与两种配合物均按3:1的质量比混合, 测定HMX混合物前后的DSC曲线, 结果如图 4所示。
|
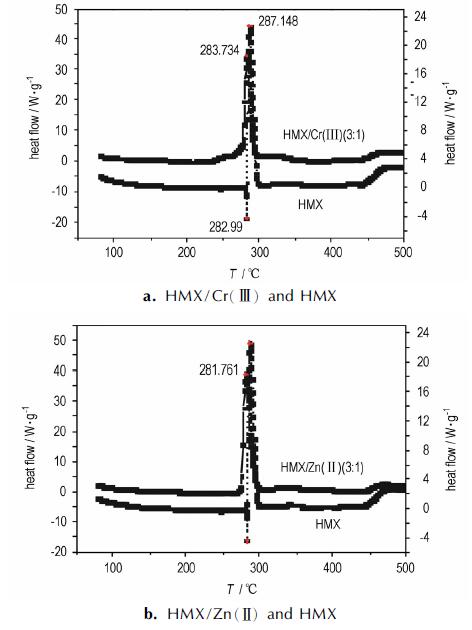
图 4 HMX与HMX/配合物的DSC曲线(β = 20 K·min-1) Fig.4 DSC curves of HMX and HMX/complexes with mass ratio of 3:1 at 20 K·min-1 |
由图 4可见, 纯品HMX的热分解主要包括1个吸热过程和1个剧烈的放热过程。吸热峰发生在275 ~285 ℃, 峰温为282.99 ℃, 熔化吸热焓为33.59 J·g-1; 随着温度的升高, 出现一个非常剧烈的放热分解峰, 发生在285~310 ℃, 峰温为287.15 ℃, 对应的HMX的分解放热量为1729.37 J·g-1。HMX与两种配合物混合后只有一个剧烈的放热峰, 其中Cr(Ⅲ)配合物与HMX混合物分解放热峰峰温(283.73 ℃)比纯品HMX放热峰提前3.42 ℃, 分解放热量从1729.37 J·g-1降至1259.04 J·g-1; Zn(Ⅱ)配合物与HMX混合物放热峰温(281.761 ℃)比纯HMX的放热峰提前5.39 ℃, 分解放热量从1729.37 J·g-1降至1685.42 J·g-1。因此, 两种配合物可以使HMX的高温分解峰温提前, 使热分解速度加快, 但是放热量却降低了, 对HMX热分解催化效果不明显。
3.3.3 对AP热分解催化作用将AP与两种配合物均按3:1的质量比混合, 测定AP混合物前后的DSC曲线, 结果如图 5所示。

|
图 5 AP与AP/配合物的DSC曲线(β= 20 K·min-1) Fig.5 DSC curves of APand AP/complexes with mass ratio of 3:1 at 20 K·min-1 |
由图 5可见, 纯品AP的热分解主要包括1个吸热过程和2个放热过程。吸热峰发生在240~250 ℃, 峰温为242.79 ℃, 为AP的晶型转变温度; 随着温度的升高, 出现一个缓慢的放热分解峰和一个剧烈的放热分解峰, 发生在300~450 ℃, 峰顶温度分别为329.99 ℃和429.49 ℃, 对应的AP的分解放热量分别为45.93 J·g-1和486.33 J·g-1。AP与配合物混合后吸热峰基本没有变化, 即配合物对AP的晶型转变温度基本没有影响。随后出现的放热过程为两物质的交叉放热过程, 两种混合物的放热峰差别较大。其中Cr(Ⅲ)配合物与AP混合物只有一个放热峰, 峰顶温度为307.17 ℃, 比AP的高温分解峰温(429.49 ℃)提前了122.32 ℃, 分解放热量从486.33 J·g-1增至1457.68 J·g-1; Zn(Ⅱ)配合物与AP的混合物有一个剧烈的放热峰, 峰形尖锐, 峰顶温度为387.09 ℃, 比AP的高温分解峰温(429.49 ℃)提前了42.40 ℃, 分解放热量从486.33 J·g-1增至1335.83 J·g-1。因此, 两种配合物都可以使AP的高温分解峰温大幅提前, 使分解速度加快, 分解放热量增加, 对AP热分解具有非常显著的催化作用。
4 结论以ANPyO为含能配体, 合成两种含能配合物Cr(C5N5O5H4)3和Zn (C5N5O5H4)2(DMF)2。DSC分析表明, 两种配合物对RDX和HMX热分解影响不大, 然而可使AP的高温分解峰温分别提前42.40 ℃和122.32 ℃, 分解放热量增加849.5 J·g-1和971.35 J·g-1, 对AP热分解催化效果显著, 说明两种配合物用作AP系固体推进剂含能催化剂具有一定可行性。
| [1] |
Kulkarni P B, Reddy T S, Nazare J K, et al. Trinitroanilino benzoic acid (TABA): potential energetic ballistic modifiers[J].
Journal of Hazardous Materials, 2005, 123(1-3): 54-60. DOI:10.1016/j.jhazmat.2005.04.010 |
| [2] |
Fyfe D W, Fmnabarger J W, Bickes T R W. BNCP prototype detonator studies using a semiconductor bridge initiator[C]//Proceedings Twentieth International Proytechnics Seminar, 1994, Colorado, USA.
|
| [3] |
Singh G, Felix S P. Studies on energetic compounds 25. An overview of preparation, thermolysis and applications of salt of 5-nitro-2, 4-dihydro-3H-1, 2, 4-triazol-3-one(NTO)[J].
Journal of Hazardous Materials, 2002, A90: 1-17. |
| [4] |
Licht H H, Ritter H. 2, 4, 6-trinitropyridine and related compound, synthesis and Characterization[J].
Propellants Explosives Pyrotechnics, 1988, 13: 25-29. DOI:10.1002/(ISSN)1521-4087 |
| [5] |
刘进剑, 刘祖亮, 成健. 含能配合物Ni(C5N5O5H4)2(by)2的晶体结构和热分解性能[J].
火炸药学报, 2012, 35(2): 36-39. LIU Jin-jian, LIU Zu-liang, CHENG Jian. Crystal Structure and thermal Decomposition Properties of Energetic Complex Ni(C5N5O5H4)2(by)2[J]. Chinese Journal of Explosives and Propellants, 2012, 35(2): 36-39. |
| [6] |
Liu J J, Liu Z L, Cheng J. Synthesis, crystal structure and properties of a novel tetra-nuclear Cu complex of ANPyO[J].
Journal of Solid State Chemistry, 2013, 197C: 198-203. |
| [7] |
Fiederling Nikolaus, Ruloff Cornelius. Die Erfindung betrifft neue Metallkompellkonplexverbindungen der allgemeinen Formel Me(DADPyOx)x' worin Me für ein Vbergangsmetallion und x für 1, 2, 3 order 4 steht, Verfahren zu deren Herstllung, sowie deren Verwendung: DE19525265A1[P], 1995.
|
| [8] |
张同来, 胡荣祖, 李福平, 等. [Pb(NTO)2(H2O)2]的制备, 分子结构和热分解机理研究[J].
化学学报, 1994, 52(6): 545-550. ZHANG Tong-lai, HU Rong-zu, LI Fu-ping, et al. Preparation, molecular structure and thermal decomposition mechanism of[Pb(NTO)2(H2O)2][J]. Acta Chimica Sinica, 1994, 52(6): 545-550. |
| [9] |
樊学忠, 李吉祯, 张腊莹, 等. NTO铅铜衍生物对AP-CMDB推进剂燃烧性能和热分解的影响[J].
含能材料, 2007, 15(4): 316-319. FAN Xue-zhong, LI Ji-zheng, ZHANG La-ying, et al. Influence of lead(Ⅱ) and copper(Ⅱ) salts of NTO on the combustion characteristics and thermal decomposition of AP-CMDB propellant[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2007, 15(4): 316-319. |
| [10] |
Trzcinski W A, Cudzilo S, Paszula J. Studies of free field and confined explosions of aluminum enriched RDX compositions[J].
Propellants Explosive Pyrotechnics, 2007, 32: 502-506. DOI:10.1002/(ISSN)1521-4087 |
| [11] |
Liu Y F, Chen Y, Shi L, et al. Synthesis of three novel laurylamine-derived long-chain ALKYL bonding agents and their interactions with RDX[J].
Propellants Explosive Pyrotechnics, 2012, 37: 69-73. DOI:10.1002/prep.v37.1 |
| [12] |
Liu H B, Jiao Q Z, Zhao Y, et al. Mixed oxides derived from Cu-Co layered double hydroxide nanorods: Preparation, characterization and their catalytic activities[J].
Journal of Alloys and Compounds, 2010, 496(1-2): 317-323. DOI:10.1016/j.jallcom.2010.02.004 |
| [13] |
Xia Z Q, Chen S P, Wei Q, et al. Syntheses and characterization of energetic compounds constructed from alkaline earth metal cations (Sr and Ba) and 1, 2-bis(tetrazol-5-yl)ethane[J].
Journal of Solid State Chemistry, 2011, 184(7): 1777-1783. DOI:10.1016/j.jssc.2011.05.017 |
| [14] |
DUAN H Z, LIN X Y, LIU G P, et al. Synthesis of Co nanoparticles and their catalytic effect on the decomposition of ammonium perchlorate[J].
Chinese Journal of Chemical Engineering, 2008, 16(2): 325-328. DOI:10.1016/S1004-9541(08)60082-8 |
| [15] |
成健, 姚其正, 刘祖亮. 2, 6-二氨基-3, 5-二硝基吡啶-N-氧化物的合成新方法[J].
有机化学, 2008(11): 1943-1947. CHENG Jian, YAO Qi-zheng, LIU Zu-liang. Novel synthesis of 2, 6-diamino-3, 5-dinitropyridine-N-oxide[J]. Chinese Journal of Organic Chemistry, 2008(11): 1943-1947. |

Two transition metal complexes with ligand 2, 6-diamino-3, 5-dinitropyridine-1-oxide (ANPyO) were synthesized. Their thermal decomposition processes and the catalytic behavior on the thermal decomposition reaction of RDX, HMX and AP were studied.



