近年来, 人们致力于寻找能量高、环境友好的含能材料。富氮化合物具有高氮、低碳、低氢的结构特征, 分子中含有大量的N—N和C—N键, 具有高正生成焓, 反应时能够释放较高的能量, 能生成以N2为主体的大量气体, 与较少氧化剂混合即可达到零氧平衡, 因此在推进剂、环保型气体发生剂等方面具有潜在的应用价值[1]。
四唑类化合物是目前受到高度关注的一类高氮含能化合物。目前已有很多关于5-氨基四唑(5-AT)合成和酸碱性研究的报道[2-6]。该化合物室温下以一水化合物形式存在, 由于60 ℃时结晶水即可自发从5-AT分子中离解出来, 所以药剂的质量和含水率易随环境温度的变化而改变, 并且含有5-AT药剂气体的反应产物中水蒸气的比率会增加。这些对其应用产生了不利影响。将5-AT转变成含能离子盐[7-14]不仅可以消除分子中结晶水引起的不稳定问题, 也可以将氧原子引入到分子中, 改善分子的氧平衡状况。目前研究较多的物质是5-氨基四唑硝酸盐(5-ATN), 其分子式为CH4N6O3, 含氮量较高, 为56.75%, 氧平衡为-10.8%, 作为气体发生剂组分具有良好的应用前景。5-AT与硝酸在不同温度下反应均可制得5-ATN。Moritz von等[15]将5-AT与浓硝酸(65%)混合后, 先在沸水浴中反应, 后在冰水浴中结晶; S.P. Burns等[16]则相反, 首先5-AT与浓硝酸(65%)在冰水浴中反应1 h, 加入蒸馏水后煮沸, 室温下冷却结晶; 孟令桥[17]在70~75 ℃条件下5-AT与浓硝酸(65%)持续反应1.5 h, 产率为88.91%;马桂霞等[18]在70℃热水浴中反应1 h, 产率为65%。这些合成方法反应温度较高, 产率较低, 反应时间过长。
本研究以5-氨基四唑一水化合物(5-AT·H2O)为原料, 常温下与硝酸反应一步制得5-ATN。正交实验得到最优合成工艺: 20 ℃下, 5 g 5-AT·H2O与15 mL浓硝酸(65%)边搅拌边反应15 min, 目标物产率达92.6%。并用元素分析、红外光谱测试、核磁共振氢谱分析和X-射线单晶衍射证明了其结构, 同时吸湿性测试表明5-ATN的吸湿性较低。和文献报道比较, 该工艺反应温度降低、时间缩短、产率提高, 为5-ATN的工业化生产奠定了良好的基础。
2 实验部分 2.1 试剂与仪器5-AT·H2O、浓硝酸(65%)、无水乙醇、硝酸钾, 均为市售分析纯试剂。
ZRD-1全自动熔点仪; 德国vario EL元素分析仪; 美国尼高力公司FT-IR4700红外光谱仪(IR); 瑞士ARX400 Bruker核磁共振谱仪; 日立S-4700扫描电子显微镜; Rigaku 742+单晶衍射仪; HWS-70B恒温恒湿箱。
2.2 合成方法5-ATN合成路线见Scheme 1。
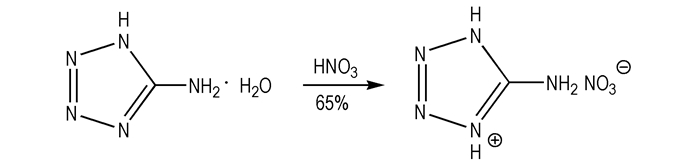
|
Scheme1 Synthesis route of 5-ATN |
20 ℃下, 将5 g 5-AT·H2O溶于15 mL水中, 缓慢加入15 mL浓硝酸(质量分数为65%), 边搅拌边反应15 min。室温下自然冷却, 逐渐析出晶体, 抽滤, 冰水洗涤, 50 ℃干燥, 产率为92.6%。m.p.: 174 ℃; 1H NMR(DMSO-d6, δ): 11.035(5-AT成盐后只出现一种质子的氢, 说明成盐后形成了较多的氢键); IR(KBr, cm-1)ν: 3425、3335(N—H), 2960、2821(N+—H), 1727(C=N), 1436、1338(C—N), 1384(NO3-), 1107~1039(四唑环); Anal. calcd for CH4N6O3: C 8.11, H 2.72, N 56.75; found C 8.10, H 2.70, N 56.61。
2.3 SEM分析和X-射线单晶衍射用日立S-4700扫描电子显微镜, 放大800倍观察5-ATN的表面形貌。
将1 g 5-ATN溶解在20 mL无水乙醇中, 完全溶解后用锡纸封口, 置于室温环境中, 至有大量晶体析出, 选取大小合适的晶体进行测试, 通过Rigaku 742+单晶衍射仪收集衍射数据。
3 结果与讨论 3.1 SEM图分析和X-射线单晶衍射分析5-ATN的表面形貌如图 1所示。由图 1可以看出, 合成的5-ATN形状规则且表面光滑。

|
图 1 5-ATN的SEM图 Fig.1 SEM photograph of 5-ATN |
5-ATN的分子结构如图 2所示, 该晶体属于单斜晶系, P21/c空间群, a=1.0545(5)nm, b=0.34422(18)nm, c=1.4613(8)nm, α=γ= 90°, β=90.550(8)°, V=0.5304(5)nm3, Z=4。结构包括[5-ATH]+阳离子和NO3-阴离子, 通过强氢键连接组成: O(3)…H(1)—N(1) (O(3)—N(1) 0.2752 nm), O(3)…H(4)—N(4) (O(3)—N(4) 0.2762 nm), O(1)…H(5A)—N(5) (O(1)—N(5) 0.3262 nm)和O(2)…H(5B)—N(5) (O(2)—N(5) 0.3259 nm)。表 1为5-ATN的键长和键角, 结果与文献[15, 18]相符。
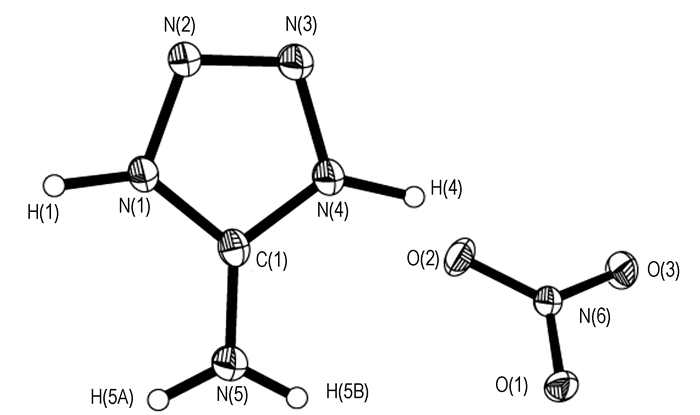
|
图 2 5-ATN的晶体结构图 Fig.2 Molecular structure of 5-ATN |
| 表 1 5-ATN的键长、键角 Tab.1 Structural parameters for 5-ATN |
根据文献[15-18], 用正交实验[19]方法, 选取硝酸的用量、反应时间和反应温度这三种因素作为正交实验因素, 优化指标为5-ATN的产率, 因素水平表见表 2。
| 表 2 因素水平表 Tab.2 Factors and levels |
本研究正交实验结果如表 3和表 4所示。为了统计方便和直观分析,将产率指标值做适当简化(xi=yi-85),进行统计分析。
| 表 3 正交试验结果 Tab.3 Results of orthogonal experiments |
| 表 4 方差分析结果 Tab.4 Results of variance analysis |
表 3中nullable为空列,以多余空列来计算实验误差Se,使实验更精准。方差(S=Q-CT)的大小反映该因素对实验指标均值偏离的程度,数值越大,表明该因素水平的微小变动会导致指标值的较大波动,因此,方差最大的称为主要因素,相反,方差值很小,甚至比实验误差的计算值还小,说明该因素水平值的很大变动所导致实验指标值的波动很微弱,称这一类因素为摒弃因素,可以将这类因素的方差合并到实验误差之中,记为当量误差SeΔ。从表 4方差分析可知,因素A硝酸的用量对5-ATN产率的影响最大,因素C反应温度次之,反应时间对产率的影响最小。
实验的目的是为了寻找更好的因素水平的组合并付诸于生产,最好的因素水平组合即为最佳生产条件。方法是首先在主要因素产率中,挑选产率最高的对应水平,即在ki中选取产率最高的主要因素所对应的水平,第二步是决定次要因素的最好水平,方法同上。针对本实验,主要因素是A(硝酸的用量),最佳水平为A3,具体优化反应条件为:A3B1C1。即硝酸用量为15 mL,反应时间为15 min,反应温度为50 ℃。
优化条件中反应时间和反应温度都选择了水平1,说明并未得到真正优化,由于反应温度比反应时间对实验结果的影响更大,所以应继续降低温度,对反应温度范围10~50 ℃的正交结果进行分析。
3.2.2 进一步优化同样选择硝酸的用量(A)、反应时间(B)和反应温度(C)这三种因素作为正交实验因素,因素水平表见表 5。本研究实验数据见表 6和表 7,分析方法同上。反应时间为摒弃因素,故并入实验误差当中,记为当量误差SeΔ。由于反应时间对实验的影响较小,所以反应时间的选择应从省时、省力和经济性等方面来考虑,所以选定反应时间B1为15 min。于是最佳生产条件可定为A3B1C2,即硝酸含量为15 mL,反应时间为15 min,反应温度为20 ℃。
| 表 5 因素水平表 Tab.5 Factors and levels |
| 表 6 正交试验结果 Tab.6 Results of orthogonal experiments |
| 表 7 方差分析结果 Tab.7 Results of variance analysis |
以最佳水平的组合实验三次,考察是否可以达到预期的目标,结果见表 8。由表 8可知,最佳生产条件重复性较好,平均产率达到92.6%,表明实验得到了较优的合成工艺条件。
| 表 8 验证实验结果 Tab.8 Results of verification experiments |
根据GJB 5891.9-2006《火工品药剂测试方法》中吸湿性测定方法,在恒温(30 ℃),常压条件下,将干试样放在盛有硝酸钾饱和溶液的干燥器内,经过24 h吸湿,测试试样吸收水分的质量,结果见表 9。
| 表 9 5-ATN的吸湿性测试结果 Tab.9 Results of hygroscopic test of 5-ATN |
取三次吸湿性实验的平均值0.086%为5-ATN 24 h的吸湿量,说明5-ATN的吸湿性很小,可以消除5-AT分子中结晶水引起的不稳定问题,为5-ATN的实际应用提供广阔前景。
4 结论(1) 以5-AT为原料,与硝酸反应一步制得5-ATN,并通过元素分析、红外光谱、核磁共振氢谱和X-射线单晶衍射测试证明成功合成5-ATN。
(2) 正交实验得到最优合成工艺:5-AT的用量为5 g,硝酸的用量为15 mL,反应温度为20 ℃,反应时间为15 min,目标物产率达92.6%。该工艺反应温度降低、时间缩短、产率提高。总之,该工艺能耗低、操作简便,易于工业化生产。
(3) 表面形貌分析,说明5-ATN晶体表面光滑。吸湿性测试研究表明,5-ATN吸湿性低,避免由于吸水或结晶水等引起不稳定问题。在气体发生剂领域,有望成功替代5-AT。
| [1] |
王宏社, 杜志明. 富氮化合物研究进展[J].
含能材料, 2005, 13(3): 196-203. WANG Hong-she, DU Zhi-ming. Progress in synthesis and properties of nitrogen-rich[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2005, 13(3): 196-203. |
| [2] |
Stierstorfer J, Tarantik K R, Klapötke T M. New energetic materical: functionalized 1-ethyl-5-aminotetrazoles and 1-ethyl-5-nitriminotatrazoles[J].
Chemistry-A European Journal, 2009, 15: 5775-5792. DOI:10.1002/chem.v15:23 |
| [3] |
王宏社, 杜志明. ZnBr2催化合成5-氨基四唑[J].
含能材料, 2005, 13(6): 368-371. WANG Hong-she, DU Zhi-ming. Synthesis of 5-aminotetrazole catalyzed by zinc bromide[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2005, 13(6): 368-371. |
| [4] |
Murotani Masahiro, Mura Hajime, Takeda Makoto, Shibafuchi Hiroshi. Process for producing 5-aminotetrazole: EP 69325[P], 1994.
|
| [5] |
Rothgery E F, Knollmueller K O. Process for the preparation of 5-aminotetrazole: US, 5424449[P], 1995.
|
| [6] |
Ogawa H, Tanaka H, Oonishi A. Preparation of 5-aminotetrazole by cyclizing dicyanodiamide with sodium azide: JP 08333354[P], 1996.
|
| [7] |
Rittenhouse C T, Ariz G. Di-silver aminotetrazole perchlorate: US, 3663553[P], 1972.
|
| [8] |
Sinditskii V P, Fogelzang A E, Levshenkov A I, et al. Combustion of 5-aminotetrazole salts[C]//Proceedings of the 21st International Pyrotechnics Seminar, 1995: 762-773.
|
| [9] |
Jin C M, Ye C, Piekarski C, et al. Mono and bridged azolium picrates as energetic salts[J].
European Journal of Inorganic Chemistry, 2005, 18: 3760-3767. |
| [10] |
Denffer M V, Klapötke T M, Sabaté C M. Hydrates of 5-amino-1H-tetrazolium halogenide salts-starting materials for the synthesis of energetic compounds[J].
Zeitschrift Fur Anorganische und Allgemeine Chemie, 2008, 634: 2575-2582. DOI:10.1002/zaac.v634:14 |
| [11] |
Brill T B, Ramanathan H. Thermal decomposition of energetic materials 76: chemical pathways that control the buring rates of 5-aminotetrazole and its hydrohalide salts[J].
Combustion and Flame, 2000, 122(1/2): 165-171. |
| [12] |
Karaghiosoff K, Klapötke T M, Mayer P, et al. Salts of methylated 5-aminotetrazoles with energetic anions[J].
Inorganic Chemistry, 2008, 47: 1007-1019. DOI:10.1021/ic701832z |
| [13] |
Klapötke T M, Sabaté C M, Penger A, et al. Energetic salts of low-symmetry methylated 5-aminotetrazoles[J].
European Journal of Inorganic Chemistry, 2009: 880-896. |
| [14] |
Gálvez-Ruiz J C, Holl G, Karaghiosoff K, et al. Derivatives of 1, 5-diamino-1H-tetrazole: a new family of energetic heterocyclic-based salts[J].
Inorganic Chemistry, 2005, 44(12): 4237-4253. DOI:10.1021/ic050104g |
| [15] |
Moritz von Denffer, Thomas M. Klapotke. Improved synthesis and x-ray structure of 5-aminotetrazolium nitrate[J].
Proplellants Explosives Pyrotechnics, 2005(3): 191-195. |
| [16] |
Burns S P, Khandhadia P S. Method of formulating a gas generant composition: USP 6475312[P], 2002.
|
| [17] |
孟令桥. 双四唑肼及氨基四唑含能盐合成及性能研究[D]. 北京: 北京理工大学, 2010.
MENG Ling-qiao. Synthesis and performance studies of bistetrazolohydrazine and aminotetrazolium salts[D]. Beijing Institute of Technology, 2010. |
| [18] |
MA Gui-xia, ZHANG Tong-lai, ZHANG Jian-guo, et al. Thermal decomposition and molecular structure of 5-aminotetrazolium nitrate[J].
Thermochimica Acta, 2004, 12(423): 137-141. |
| [19] |
沈邦兴, 文昌俊.
实验设计及工程应用[M]. 中国计量出版社, 2005.
SHEN Bang-xing, WEN Chang-jun. Design of experiment and engineering application[M]. Beijing: Chinese Metrology Press, 2005 |
5-Aminotetrazolium nitrate was synthesized from 5-aminotetrazole monohydrate(5-AT·H2O) and concentrated nitric acid. The effects of nitric acid dosage, reaction time and reaction temperature on the yield of 5-ATN were studied by orthogonal experiment.




