2. 西安近代化学研究所, 陕西 西安 710065
2. Xi′an Modern Chemistry Research Institute, Xi′an 710065, China
自Kroto等[1]于1985年在研究中发现富勒烯C60, Kratschmer等[2]于1990年实现富勒烯宏量制备以来, 富勒烯及其衍生物的研究就引起了全球科学家们的浓厚兴趣。C60是碳的第三种纯碳形态, 由60个碳原子组成, 包含12个五元环和20个六元环, 因结构独特, 具有许多优异特性。富勒烯及其衍生物已经影响到电子学、光学、磁学、化学、医学、材料科学和生物工程等领域[3]。
探索富勒烯衍生物在含能材料、推进剂中的应用也是目前比较活跃的领域之一[4-11]。双基推进剂中添加一定量的富勒烯C60, 能提高铅盐的催化效率, 推进剂分解热增大, 平台效应范围增大, 推进剂压力指数降低, 低压下, 燃速大幅度提高[12]。李疏芬[13]认为, 推进剂中加入富勒烯C60后, C60与新生成的铅通过配键作用形成C60-Pb络合物, 提高了铅的分散度, 加速了含能材料分解, 即燃面上C60-Pb活性催化中心催化机理。基于此, 从分子水平上在C60分子上引入一些含能基团, 得到新型含能富勒烯衍生物, 将其作为燃烧催化剂添加到推进剂中, 将可能既提高铅盐的催化效率又能提供一定的能量, 取代本身并不具有能量的传统燃烧催化剂碳黑。目前, 富勒烯基含能材料在推进剂中应用研究尚未见报道。本研究以乙二胺、富勒烯C60、硝酸为原料, 经两步反应合成并分离出了目前尚未见报道的富勒烯基含能材料——富勒烯乙二胺硝酸盐, 并采用紫外(UV-Vis)、红外光谱(FT-IR)、元素分析、X射线光电子能谱(XPS)等对产物结构进行表征, 用差热分析(DTA)、热重分析(TG)、热重红外联用(TG-IR)等技术对产物热分解特性进行了研究。
2 实验部分 2.1 试剂与仪器试剂: C60, 自制, 纯度>99%;乙二胺、丙酮、硝酸, 均为分析纯, 成都市科龙化工试剂厂。
仪器:美国尼高力仪器公司Nicolet 5700型傅里叶变换红外吸收光谱仪; 日本岛津公司UV-3150型紫外-可见-近红外光谱仪; 德国元素分析系统公司Vario EL CUBE型元素分析仪; 美国TA仪器公司SDTQ600同步热分析仪; 美国Thermo公司VG250型X射线光电子能谱仪; 德国耐驰仪器制造有限公司型号为TG209F1与美国尼高力公司型号为Nicolet 8700的热重红外联用仪。
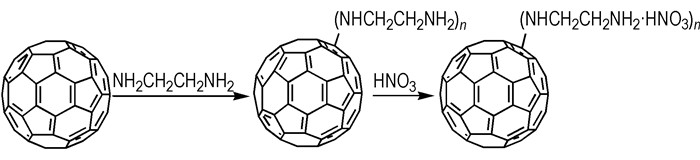
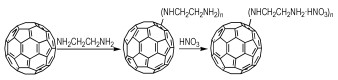
2.2 富勒烯乙二胺硝酸盐的制备以富勒烯和乙二胺为初始原料通过亲核加成反应合成富勒烯乙二胺, 富勒烯乙二胺再与硝酸反应合成富勒烯乙二胺硝酸盐, 制备路线见Scheme 1。
|
Scheme 1 Synthesis of fullerene ethylenediamine nitrate |
参考文献[14], 称取富勒烯C60 1.0 g, 量取新蒸乙二胺500 mL, 置于1000 mL三口烧瓶中, 氮气保护, 80 ℃油浴下反应4 d。反应完毕后减压旋蒸除去过量乙二胺, 得棕色粘稠物, 先加入30 mL蒸馏水溶解粘稠物, 再加入500 mL丙酮稀释结晶, 有棕黄色固体析出, 过滤, 真空干燥至恒重, 得2.3 g棕黄色富勒烯乙二胺。
富勒烯乙二胺是多加成混合物, 其结构式可表示HnC60(H2NCH2CH2NH2)n, 其中n为平均值。参考文献[14]以溴甲酚绿-甲基红为指示剂, 用HCl标准溶液滴定衍生物中的氨基含量, 测得n=16, 即本文的富勒烯乙二胺结构式为H16C60(H2NCH2CH2NH2)16。
2.2.2 富勒烯乙二胺硝酸盐的制备称取富勒烯乙二胺0.5 g, 置于100 mL单口烧瓶, 用20 mL去离子水溶解后, 加入5 mL的2 mol·L-1硝酸, 于25 ℃下, 磁力搅拌反应1 h。反应完毕后减压旋蒸除去溶剂及未反应完的硝酸, 真空干燥至恒重, 得0.8 g棕黄色固体, 即为富勒烯乙二胺硝酸盐。
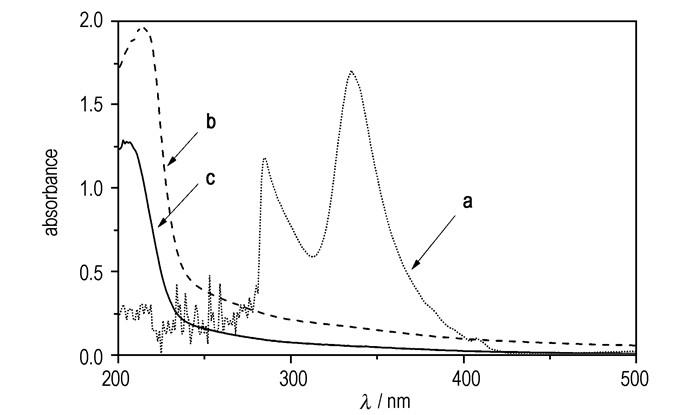
3 结果与讨论 3.1 富勒烯乙二胺硝酸盐的结构表征采用紫外可见光谱、红外光谱、元素分析以及X射线光电子能谱等测试手段对产物结构进行了表征。富勒烯、富勒烯乙二胺和富勒烯乙二胺硝酸盐的紫外-可见光谱如图 1所示, C60在284, 334, 405 nm处有吸收峰, 说明C60是Ih对称, 高度离域大π共轭体系结构, 共轭体系使分子的最高已占据轨道能级升高, 最低空轨道能级降低, π→π*跃迁的能量降低; C60在284, 334, 405 nm有吸收峰,与文献[15]的结果一致。C60与乙二胺反应生成的富勒烯乙二胺只在215 nm有吸收, 后者与硝酸成盐后的富勒烯乙二胺硝酸盐只在205 nm有吸收峰, C60的特征吸收峰消失, 紫外吸收蓝移。说明反应后, C60的高度离域大π共轭体系被破坏, 生成多加成产物。
|
图 1 富勒烯(a)、富勒烯乙二胺(b)和富勒烯乙二胺硝酸盐(c)的紫外光谱图 Fig.1 UV-Vis curves of fullerene (a), fullerene ethylenediamine (b), fullerene ethylenediamine nitrate (c) |
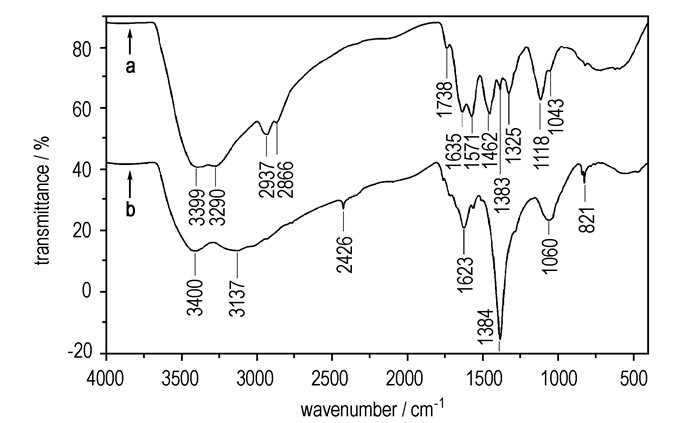
图 2为富勒烯乙二胺和富勒烯乙二胺硝酸盐的红外吸收光谱图。富勒烯乙二胺的N—H键的反对称伸缩振动和对称伸缩振动分别在3399,3290 cm-1处有较强的吸收, 2937,2866 cm-1为亚甲基的反对称伸缩振动和对称伸缩振动吸收, 1462 cm-1为亚甲基变形振动吸收, 1118,1043 cm-1为C—N键的伸缩振动吸收, 1325 cm-1为临近碳笼的C—N键的伸缩振动吸收, 由于碳笼的共轭效应使得C—N键的伸缩振动吸收向高频移动。从图 2可以看出, 富勒烯乙二胺与硝酸反应成盐后, 富勒烯乙二胺硝酸盐化合物N—H键的伸缩振动在3400,3137 cm-1处有很强较宽吸收, 由于硝酸提供质子使得N—H键的振动加强, 峰变宽; 1623 cm-1处为N—H键的弯曲振动, 1060 cm-1为C—N键的伸缩振动吸收峰, 1384,821 cm-1为硝酸根的吸收, 说明硝酸与富勒烯乙二胺反应生成了富勒烯乙二胺硝酸盐, 初步表征了产物结构。
|
图 2 富勒烯乙二胺(a)和富勒烯乙二胺硝酸盐(b)红外吸收图谱 Fig.2 FT-IR spectra of fullerene ethylenediamine (a) and fullerene ethylenediamine nitrate (b) |
元素分析分析结果(%), C 42.00, N 24.52, H 5.26, n=16时, 理论值(%), C 42.1, N 24.56, H 5.26, 测试值与理论值相符, 因此富勒烯乙二胺硝酸盐的结构式为(H16C60(H2NCH2CH2NH2·HNO3)16)。
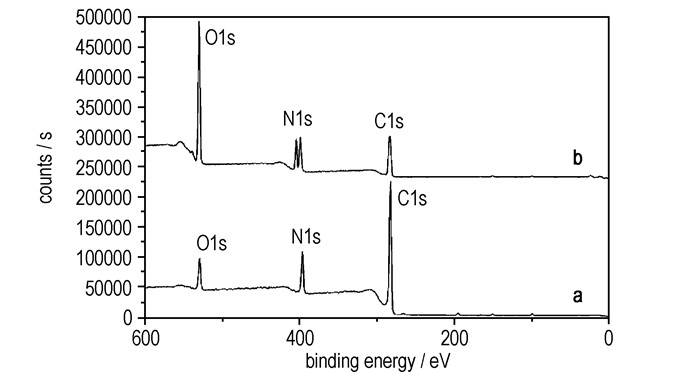
为了进一步表征产物结构, 对目标产物及原料富勒烯乙二胺进行了X射线光电子能谱(XPS)分析, 结果如图 3所示。从图 3可以看出, 富勒烯乙二胺有C1s峰、N1s峰和O1s峰, 其中C1s峰强度比较大, 说明其中C含量比较高; 而O1s峰的出现, 是由于测试过程中, 样品吸附了空气中的氧造成。富勒烯乙二胺硝酸盐同样有C1s峰、N1s峰和O1s峰, 与富勒烯乙二胺相比富勒烯乙二胺硝酸盐的O1s峰强度更大, 且多了一个N1s峰, 这是由于硝酸的引入, 引入大量的O和N元素, 404.17 eV为硝酸根的N1s[16]。从图 4b可以看出在富勒烯乙二胺硝酸盐的N1s峰出现3个峰, 说明有3种化学环境完全不同的N, 其中404.17 eV为NO3-中N1s峰, 证明引入了NO3-。
|
图 3 富勒烯乙二胺(a)及富勒烯乙二胺硝酸盐(b)XPS谱 Fig.3 XPS spectra of fullerene ethylenediamine(a) and fullerene ethylenediamine nitrate(b) |
|
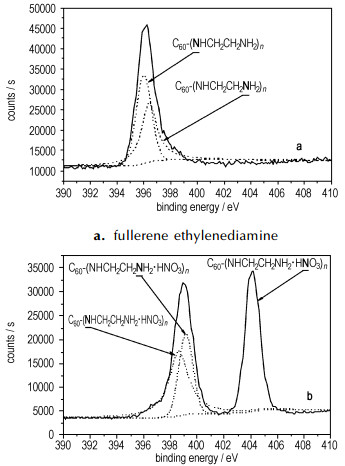
图 4 富勒烯乙二胺和富勒烯乙二胺硝酸盐的N1s XPS谱 Fig.4 N1s XPS spectra of fullerene ethylenediamine and ethylenediamine nitrate |
图 4为富勒烯乙二胺和富勒烯乙二胺硝酸盐的N1s谱图。富勒烯乙二胺中有两种N原子分别为396.10 eV的靠近富勒烯球的仲胺N原子和397.62 eV的氨基N原子。富勒烯乙二胺硝酸盐中有3种N原子分别为398.65 eV的与富勒烯球相连的仲胺N原子、399.17 eV的远离富勒烯球的N原子(—CH2CH2—NH2·HNO3)和404.17 eV处硝酸根的N原子。由图 4可以发现, 富勒烯乙二胺与硝酸反应后, N原子的电子云密度降低, N1s峰向高能端移动, 原因是硝酸引入, 通过诱导效应使N原子的电子云密度发生一定偏移。
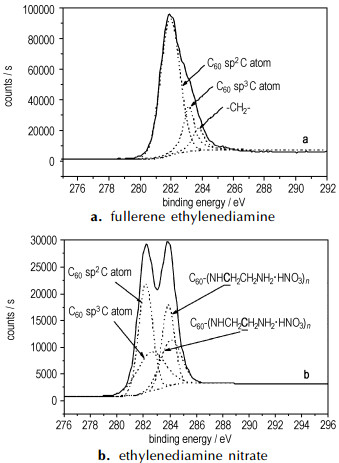
图 5a为富勒烯乙二胺C1s光谱图。从图 5a中可以看到样品中有3种C杂化: 281.87 eV的sp2C原子, 283.11 eV的sp3C原子, 283.75 eV的碳链—CH2—N峰[17-19], 283.11 eV的C1s峰出现是由于富勒烯C60与乙二胺加成反应后, 富勒烯的sp2C原子通过[6, 6][20]键加成后转变成sp3C原子。
|
图 5 富勒烯乙二胺与富勒烯乙二胺硝酸盐的C1s XPS谱 Fig.5 C1s XPS spectra of fullerene ethylenediamine and ethylenediamine nitrate |
图 5b为富勒烯乙二胺硝酸盐C1s谱图。从图 5b中可看出, 富勒烯乙二胺硝酸盐中有4种C原子, 分别为282.17 eV的sp2C原子、282.57 eV的sp3C原子、283.87 eV的靠近富勒烯球C原子(C60—NHCH2—)和284.08 eV的远离富勒烯球的C原子(—CH2—NH2HNO3) [17-19]。硝酸的引入, 向富勒烯乙二胺引入质子, 通过诱导效应使远离富勒烯球的C原子电荷密度偏移, 此C1s峰向高能量端移动。
3.2 富勒烯乙二胺硝酸盐的热分解特性采用同步热分析仪和TG-IR联用仪对富勒烯乙二胺硝酸盐进行了热分解特性研究。同步分析实验条件:样品质量3.02 mg, 升温速率10 ℃·min-1, 空气气氛, 空气流速100 mL·min-1, 温度范围为室温~700 ℃。TG-IR联用追踪实验条件:样品质量2.35 mg升温速率10 ℃·min-1, 温度范围为室温~700 ℃, 空气气氛。
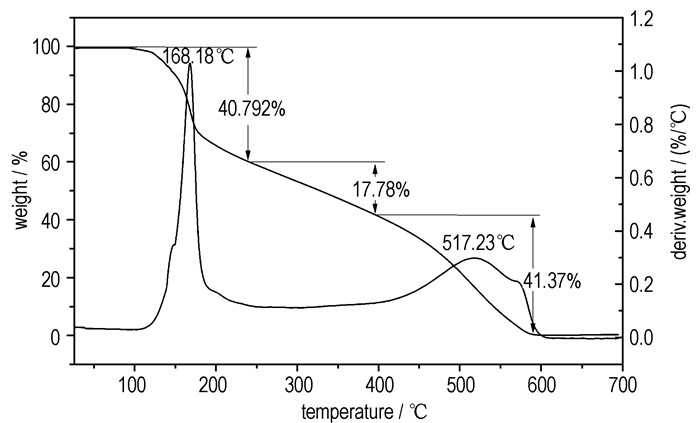
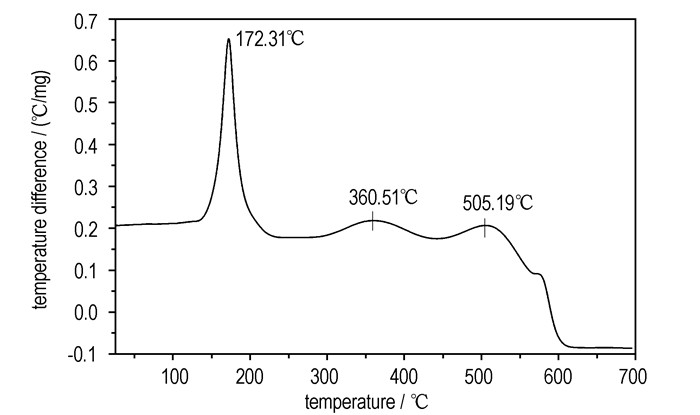
图 6为富勒烯乙二胺硝酸盐的TG-DTG曲线, 由图 6可以看到富勒烯乙二胺硝酸盐在室温~700 ℃范围内有两个失重阶段, 分别为100~250 ℃和250~580 ℃; 富勒烯乙二胺硝酸盐的初始分解温度为100 ℃, 在100~250 ℃, 失重40.79%, 168.18 ℃时, 失重到最大, 结合富勒烯乙二胺硝酸盐的DTA曲线(图 7), 产物在172.31 ℃剧烈分解, 放热峰强而高, 可能是由于硝酸根在短时间内迅速分解及部分支链分解, 因为硝酸根全部分解的理论失重为37.5%, 而TG曲线显示失重40.79%。第二阶段(250~580 ℃)失重占总失重的59.21%, 由图 7可以看出, 在360.51, 505.19 ℃分别有较弱的放热峰, 可能是碳笼上残留的部分支链分解脱离碳笼和碳笼分解, 这也可以解释图 6所示的第二阶段的热失重。
|
图 6 富勒烯乙二胺硝酸盐的TG-DTG曲线 Fig.6 TG-DTG curve for fullerene ethylenediamine nitrate |
|
图 7 富勒烯乙二胺硝酸盐的DTA曲线 Fig.7 DTA curve for fullerene ethylenediamine nitrate |
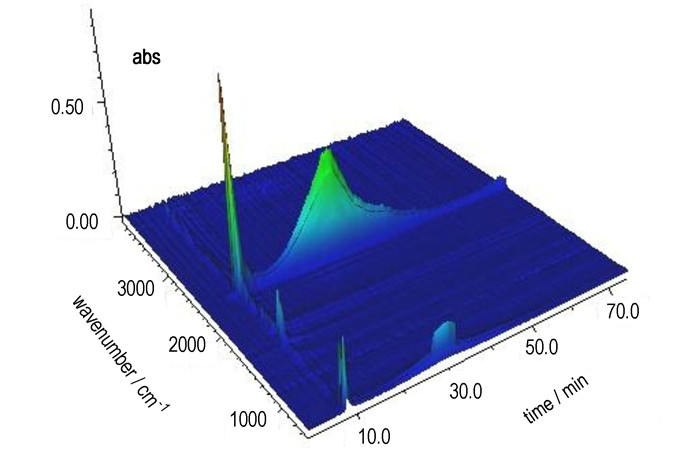
为进一步研究富勒烯乙二胺硝酸盐热分解, 用TG-IR联用技术表征其分解过程。富勒烯乙二胺硝酸盐分解过程中所得的三维红外图谱如图 8所示, 表明富勒烯乙二胺硝酸盐分两个阶段分解: 100~250 ℃和250~580 ℃。
|
图 8 富勒烯乙二胺硝酸盐的红外三维谱图 Fig.8 3D Infrared spectra of fullerene ethylenediamine nitrate |
从图 8可以看出, 100~250 ℃温度范围内有H2O (3732, 3626, 1600 cm-1)、CO2 (2360, 2310, 670 cm-1)、CO (2185, 2111 cm-1)、N2O (2239 cm-1) [21]和NO2 (1629 cm-1)等气体释放, 250~580 ℃温度范围内只有CO2的吸收峰(2360, 2310, 670 cm-1)。
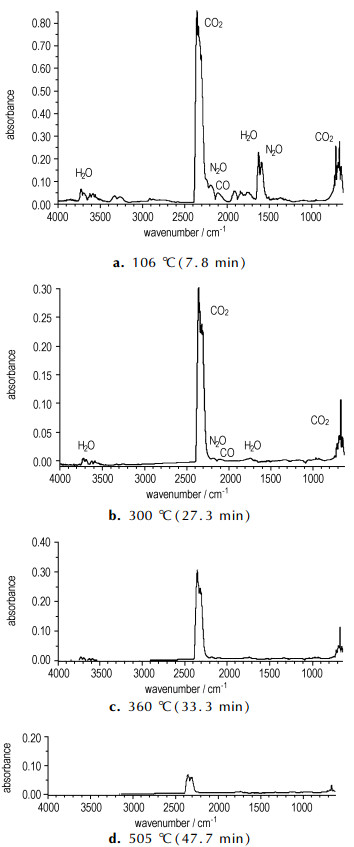
图 9为富勒烯乙二胺硝酸盐在室温~700 ℃升温过程中, 7.8 min(a)、27.3 min(b)、33.3 min(c)和47.7 min(d)时释放气体的红外吸收图谱。从图 9可以看出, 7.8 min(106 ℃)时, 气体的主要成分有H2O (3732, 3626, 1600 cm-1)、CO2(2360, 2310, 670 cm-1)、CO(2185, 2111 cm-1)、N2O(2239cm-1)和NO2(1629cm-1), 气体是硝酸根和部分支链分解释放; 27.3 min(300 ℃)时, 有CO2和少量的H2O、CO和N2O气体, 为残留的部分支链分解释放, 33.3 min(360 ℃)时, H2O、CO和N2O峰已经相当弱, 说明支链接近分解完全; 到47.7 min(505 ℃)时, 只释放出CO2(2360, 2310, 670 cm-1)气体, 此阶段碳笼分解氧化成CO2; 与TG-DTG分析结果一致。
|
图 9 106, 300, 360 ℃和505 ℃时富勒烯乙二胺硝酸盐释放气体红外谱图 Fig.9 FT-IR spectra of the gas released from fullerene ethylenediamine nitrate at 106, 300, 360, 505 ℃ |
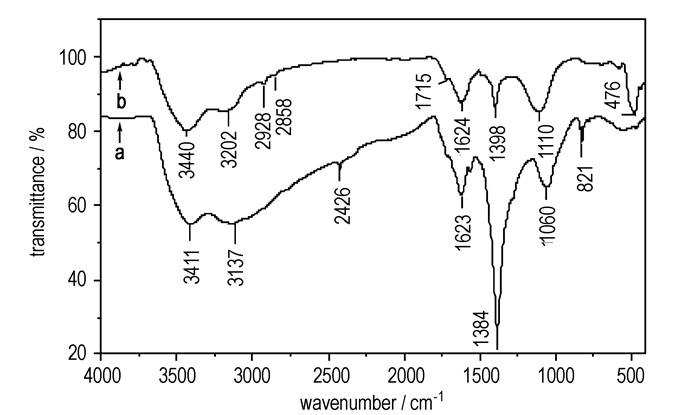
为进一步研究第一阶段分解后残留物成分, 将样品加热到260 ℃停止加热, 残留物KBr压片测红外, 结果如图 10所示。从图 10可以看出, 260 ℃后残留物已经没有NO3-特征吸收峰, 表明第一阶段热分解后不存在NO3-, 但仍有伯胺的N—H键伸缩振动吸收双峰(3440, 3202 cm-1), —NH键弯曲振动吸收峰(1624 cm-1), C—N键的伸缩振动吸收峰(1110 cm-1), —CH2的吸收峰(2926, 2858 cm-1), 可以推测第一阶段分解后, 残留物还存在—CH2NH2片段, 结合第一阶段样品分解释放出H2O、CO2、CO、N2O和NO2等气体; 进一步证明第一阶段为硝酸根和部分支链分解。富勒烯乙二胺硝酸盐具体分解机理还有待进一步研究。
|
图 10 富勒烯乙二胺硝酸盐、富勒烯乙二胺硝酸盐260 ℃后残留物的红外吸收图谱 Fig.10 FT-IR spectra of fullerene ethylenediamine nitrate and residues of fullerene ethylenediamine nitrate after 260 ℃ |
(1) 以富勒烯、乙二胺和硝酸为原料在温和条件下, 制备了一种未见文献报道的新型含能富勒烯衍生物——富勒烯乙二胺硝酸盐; 并通过化学滴定、紫外可见光谱、红外光谱、元素分析及XPS确证其结构式为(H16C60(H2NCH2CH2NH2·HNO3)16)。
(2) 用同步热分析仪和TG-IR联用仪对富勒烯乙二胺硝酸盐的热分解特性进行了研究。结果表明, 富勒烯乙二胺硝酸盐的热稳定性较好, 其分解分别发生在100~250 ℃和250~580 ℃两个阶段; 在100 ℃开始失重, 最大失重峰值温度为168.18 ℃, 第一阶段硝酸和部分支链发生分解, 释放出H2O、CO2、CO、N2O和NO2, 第二阶段残留的部分支链和碳笼分解, 主要释放CO2气体。
| [1] |
Kroto H W, Heath J R, O′Brien S C, et a1. C60: Buekminster fullerene[J].
Nature, 1985, 318: 262-263. |
| [2] |
Kratshmer W, Iamb L D, Fostiropoulos K, et al. Solid C60: A new form of carbon[J].
Nature, 1990, 347: 354-356. DOI:10.1038/347354a0 |
| [3] |
邓顺柳, 谢素原. 富勒烯合成化学研究进展[J].
化学进展, 2011, 23(1): 53-63. DENG Shun-liu, XIE Su-yuan. Synthetic chemistry of fullerenes[J]. Progress in Chemistry, 2011, 23(1): 53-63. |
| [4] |
Pichierri F. Proposal for using C60 anions as propellants for ion engines[J].
Physics Letters A, 2003, 318: 425-428. DOI:10.1016/j.physleta.2003.09.036 |
| [5] |
WANG Nai-xing, LI Ji-sheng, JI Gai-jiao. Synthesis of trinitrophenyl C60 derivative[J].
Propellants Explosives Pyro-technics, 1996, 21: 317-318. DOI:10.1002/(ISSN)1521-4087 |
| [6] |
彭汝芳, 金波, 马冬梅, 等. 2-(2-硝基苯基)吡咯烷[3′, 4′: 1, 2][60]富勒烯的合成[J].
火炸药学报, 2007, 30(2): 29-32. PENG Ru-fang, JIN Bo, MA Dong-mei, et al. Synthesis of 2-(2-nitrophenyl) fullerenopyrrolidine[J]. Chinese Journal of Explosives & Propellants, 2007, 30(2): 29-32. |
| [7] |
Greiner B E, Frederick J, Robert A, et al. Com-bustion effects of C60 soot in ammonium nitrate propellants[J].
Journal of Propulsion and Power, 2003, 19(4): 713-715. DOI:10.2514/2.6161 |
| [8] |
JIN Bo, PENG Ru-fang, TAN Bi-sheng, et al. Synthesis and characterization of nitro fulleropyrrolidine derivatives[J].
Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(3): 287-292. |
| [9] |
李丽, 彭汝芳, 金波, 等. 富勒烯乙二胺铅盐的制备及研究[J].
功能材料, 2013, 6(44): 814-821. LI li, PENG Ru-fang, JIN Bo, et al. Preparation and characterization of fullerene ethylenediamine lead salt[J]. Journal of Functional Materials, 2013, 6(44): 814-821. |
| [10] |
WANG Nai-xing. Review on the nitration of[60] fullerene[J].
Propellants Explosives Pyrotechnics, 2001, 26: 109-111. DOI:10.1002/(ISSN)1521-4087 |
| [11] |
Christian A, Yalaha, F L. Explosive/energetic fullerenes[P]. US: 7025840B1, 2006, 11.
|
| [12] |
王晗, 赵凤起, 李上文, 等. 碳物质在固体推进剂中的功能及其作用机理[J].
火炸药学报, 2006, 29(4): 32-35. WANG Han, ZHAO Feng-qi, LI Shang-wen, et al. Function of carbon materials used in solid propellants and their action mechanism[J]. Chinese Journal of Explosives & Propellants, 2006, 29(4): 32-35. |
| [13] |
李疏芬, 何德球, 单文刚, 等. 含C60的RDX-CMDB推进剂性能研究[J].
推进技术, 1997, 6(18): 71-83. LI Shu-fen, HE De-qiu, SHAN Wen-gang, et al. A study on comprehensive characteristics of RDX-CMDB propellants containing fullerene[J]. Journal of Propulsion Technology, 1997, 6(18): 71-83. |
| [14] |
方鹏飞, 吴静, 熊鸣, 等. 富勒烯胺金属配合物的制备及其催化性能研究[J].
武汉大学学报, 2003, 49(2): 175-178. FANG Peng-fei, WU Jing, XIONG Ming, et al. Preparation and study on the catalytic activity of fullerene-amine metal complexes[J]. Journal of Wuhan University (Natural Science Edition), 2003, 49(2): 175-178. |
| [15] |
Hare T P, Kroto H W, Taylor R. Preparation and UV/visible spectra of fullerenes C60 and C70[J].
Chemical Physics Letters, 1991, 45(177): 394-398. |
| [16] |
Bruce C B. Cellulose nitrate as a binding energy reference in N(ls) XPS studies[J].
Applied Surface Science, 1990, 45(3): 221-227. DOI:10.1016/0169-4332(90)90005-K |
| [17] |
CHEN Yuan-yin, FANG Peng-fei, ZHU Ling, et al. Synthesis of fullerene ethylenediamine derivative platinum complex and its catalytic behavior in the hydrosilylation of olefins[J].
Chemical Journal of Chinese University, 1998, 19(7): 1011-1015. |
| [18] |
王国建, 金吉琼. 聚乙烯马来酸酐接枝聚合物修饰多壁碳纳米管[J].
新型炭材料, 2012, 27(1): 19-25. WANG Guo-jian, JIN Ji-qiong. Chemical modification of multiwalled carbon nanotubes by polyethylene-grafted maleic anhydride[J]. New Carbon Materials, 2012, 27(1): 19-25. |
| [19] |
叶芸, 游玉香, 汤巧治, 等. 不同强酸氧化对碳纳米管场发射特性的影响[J].
功能材料, 2010, 9(41): 1529-1535. YE Yun, YOU Yu-xiang, TANG Qiao-zhi, et al. Effect of concentrated acid oxidation on field emission properties of carbon nanotubes[J]. Journal of Functional Materials, 2010, 9(41): 1529-1535. |
| [20] |
唐光诗, 朱鹤孙. C60的加成反应[J].
化学进展, 1999, 9(3): 300-309. TANG Guang-shi, ZHU He-sun. The addition reaction of C60[J]. Progress in Chemistry, 1999, 9(3): 300-309. |
Fullerene ethylenediamine nitrate was synthesized via reaction of fullerene, ethylenediamine and dilute nitric acid, which was characterized by UV-Vis, FT-IR, elemental analysis and XPS. Its thermal decomposition was investigated by TG, DTA and TG-FTIR.




