六硝基六氮杂异伍兹烷(CL-20, HNIW)是迄今为止综合性能最好的高能量密度化合物, 它的合成与工艺研究是目前高能量密度材料领域的研究热点之一[1-8]。六苄基六氮杂异伍兹烷(HBIW)是制备CL-20的关键中间体, 由苄胺和乙二醛在酸催化下缩合得到[8](Scheme 1)。由HBIW经氢解、硝化等步骤合成CL-20是目前含能材料领域的主要工艺途径[8]。对HBIW结构的研究可为其氢解、硝化等反应的深入研究提供技术手段与理论依据。尽管已有文献报道了其氢解产物及杂质的单晶结构[2], 但HBIW自身的单晶结构数据却未见报道。另外在分子结构波谱表征方面, 已有文献[9-12]报道了HBIW的红外、质谱数据, 文献中也列举了其核磁氢谱[9-12]、碳谱数据[11], 但由于早期仪器分辨率及核磁技术的限制, 核磁信号指认不完全, 且已归属的信号尚有商榷之处。为深入表征HBIW分子结构, 本研究首次利用单晶衍射技术对HBIW的晶体结构进行确认, 并采用500 MHz超导核磁共振波谱仪对HBIW的NMR信号首次进行全归属, 为该类化合物的深入研究提供基础数据与参考。

|
Scheme 1 [8] |
材料: HBIW,由北京理工大学提供,西安近代化学研究所纯化,HPLC归一化法纯度99.8%,元素分析C、H、N质量分数与理论值的误差不超过0.3%。
试剂:氘代氯仿(CDCl3,99.8%)、氘代丙酮(Acetone-d6,99.8%)、氘代二甲基亚砜(DMSO-d6,99.8%), 美国CIL公司; 丙酮,分析纯。
2.2 仪器与方法仪器:瑞士Bruker公司AV500型(500 MHz)超导核磁共振仪; 德国BRUKER SMART APEX Ⅱ CCD型X-射线单晶衍射仪。
方法:一维实验。采用正向检测探头(BBO多核宽带探头), Φ5 mm样品管, 1H NMR观测频率为500.13 MHz, 13C NMR的观测频率为125.77 MHz, 15N NMR的观测频率为50.69 MHz。1H、13C NMR以四甲基硅烷为内标(δ0), 15N NMR以硝基甲烷(CH3NO2)为外标(δN0);二维实验:采样点阵t2×t1=1024×512, FT变换数据点阵F2×F1=1024×1024, NS=8, 1H-13C gHSQC (gradient Heteronuclear Singular Quantum Coherence, 梯度异核单量子相干), 1H-13C gHMBC(gradient Heteronuclear Multiple Bond Coherence, 梯度异核多键相干)中D4=1s/(4JCH)=1.78 ms, D2=1s/(2JCH) =3.57 ms, D6=1s/(2×nJCH)=71.4 ms, 1H-15N gHMBC中D2=1s/(2JNH) =5.56 ms, D6=1s/(2×nJNH)=100 ms。
2.3 单晶样品制备及晶体结构测定取少量纯化的HBIW固体溶于适量的丙酮中, 缓慢挥发2周后得到单晶。选取0.12 mm×0.11 mm×0.11 mm晶体置于X射线单晶衍射仪上, 用单色化的MoKα射线(λ= 0.710 73Å)为光源, 以ω/2θ扫描方式, 室温296(2)K, 收集衍射点, 所有计算用Shelxtl-97程序包解出, 非氢原子坐标和各向异性温度因子经全矩阵最小二乘法修正。
3 结果与讨论 3.1 HBIW的单晶结构晶体结构分析表明, HBIW分子式为C96H96N12, 分子量为1417.85, 为2个HBIW分子结构信息。化合物晶体属正交晶系, 空间群为Pca2(1), 晶胞参数: a=0.10724(2) nm, b=0.37001(7) nm, c=0.20476(4) nm, α=β=γ=90°, V=8.125(3)×103 nm3, Z=4, Dc=1.159 g·cm-3, F(000)=3024, R1=0.0554, wR2=0.1249, 最终差值电子云密度的最高峰为219 e·nm-3, 最低峰为-159 e·nm-3。HBIW的分子单晶结构和晶胞堆积图见图 1, 部分键长、键角和二面角数据见表 1和表 2。

|
图 1 HBIW的单晶结构和堆积图 Fig.1 Single crystal structure and packing of the molecule of HBIW |
| 表 1 HBIW的部分键长与键角 Tab.1 Selected bond lengths and bond angles of HBIW |
| 表 2 HBIW的部分扭角数据 Tab.2 Selected torsion angles for HBIW |
从单晶结构分析可知, HBIW分子基本为对称结构, 五元氮杂环上除桥头C原子外的其他4个原子基本在同一平面, 桥头C原子偏离该平面0.065 nm, 与N原子直接相连的4个苄基均指向环外, 相邻较近的N(3)与N(6)所连两个苄基苯环平面夹角大约呈86°, 几乎相互垂直。骨架中相距较远的2个苯环则有小的夹角, 大约为12°, 接近于平行。六元氮杂环则为船式构型, 两端夹角分别为53.67 °与51.43°。骨架外六元环N(1)与N(2)所连的苯环也存在稍小夹角, 大约为57.5°。因异伍兹烷环张力较大, 苄基基团相对拥挤而使6个苯环稍有扭曲, 五元氮杂环上4个苯环具有较大的扭角, 最大扭角可达2.3°。从键长分析看, 异伍兹烷骨架上的键长在0.145~0.160 nm之间, 其中以C(45)—C(48)桥键键长值(0.1588(3) nm)最大, 稍长于普通C—C键长(0.154 nm), 接近于CL-20分子中相应键长(0.159 nm)。另外, 五元氮杂环所连4个苄基N—C键长稍长于环外的2个苄基N—C键长, 这就使得其可能更容易脱去。
3.2 HBIW的NMR表征 3.2.1 不同氘代试剂溶液中HBIW的谱图特征常温下, HBIW在氘代氯仿、氘代丙酮、氘代二甲基亚砜中的溶解度不同, 在0.6 mL的氘代丙酮和氘代二甲基亚砜中仅能溶解10 mg左右的样品, 使得碳谱检测所需时间较长, 而氮谱检测则难以实现。而在0.6 mL氘代氯仿中可溶解约100 mg的样品, 溶解度较大, 可方便地进行全面的核磁分析。
分别在三种氘代试剂中对HBIW进行了NMR研究, 三种试剂的溶剂效应使得图谱分辨率有所不同, 在氢谱(图 2a)中, 除去芳环区存在δ7.50~δ7.00(m, 30H)多重峰及相应的残余溶剂信号外, 烷基区明显呈两簇峰, 一簇为δ3.50(s, 2H)附近的单峰, 另一簇峰为δ4.30~δ3.90(m, 16H)的多重谱线。在氘代氯仿溶液中, 该多重谱线为6条谱线, 而氘代丙酮与氘代二甲基亚砜溶液中为3条谱线。其中, 氘代氯仿中两端低中间高的4条谱线, 为典型的AB自旋裂分特征, 应为五元环氮上的苄基旋转受阻引起的偕位氢不等价所致。而在其他两种溶剂中则化学位移重合使其不可分辨, 从而表现为1条谱线(单峰)。

|
图 2 HBIW在氘代二甲基亚砜(A)、氘代丙酮(B)、氘代氯仿(C)溶液中的1H NMR谱(a)及13C NMR谱(b) Fig.2 1H NMR and 13C NMR spectra of HBIW in DMSO-d6(A), Acetone-d6(B) and CDCl3(C) |
在碳谱(图 2b)中, 氘代氯仿与氘代丙酮中的谱图分辨率较好, 可发现有清晰可辨的12条谱线(文献[11]仅发现9条谱线), 且基本呈1高1低, 对应于异伍兹烷环中两类碳(环内与桥头碳)信号及两类苄基(五元环所连4个苄基与六元环所连2个苄基)信号。而二甲基亚砜中的芳环部分信号重合较为严重, δ128附近的三条谱线, 位移差小于δ0.05, 需要较高分辨率的仪器才能使其信号分离。
综上, HBIW在氘代氯仿溶液中可获得完整且分辨率较好的核磁图谱, 因此, 在氘代氯仿中开展了HBIW的NMR研究。
3.2.2 1H NMR和13C NMR归属氢谱中, 设置δ3.58(s)积分面积为2, 则图谱中氢原子总个数为48, 与预定结构一致。其中, 芳环区存在δ7.50~δ7.00(m, 30H, 文献[11, 12]为δ7.20~δ7.24)多重峰, 从峰形及积分面积上分析, 为典型的单取代苯环特征, 归属为HBIW中6个苄基基团中苯基。烷基区中明显呈两簇峰, δ3.58(s, 2H, 文献[11, 12]为δ3.59)为骨架中桥头碳氢, 另一组峰δ4.25~δ3.95(m, 16H)为苄基中的6个CH2与异伍兹烷骨架中的4个CH。放大该区域, 可观察到6条谱线, 除去δ4.16(s, 4H)与δ4.03(s, 4H)信号, 中间δ4.13~δ4.04(m, 8H)为两边低中间高的4条谱线, 属典型的AB裂分, 依据其化学位移δ4.13, δ4.10, δ4.07, δ4.04, 计算得其两个氢化学位移分别为δa4.11, δb4.05, 偶合常数为13.0 Hz, 为典型的同碳偕位偶合常数, 与其结构一致, 对应于五元环所连四个苄基中的亚甲基。鉴于文献[11]中该信号为δ4.09(s, 8H), 故升高5 ℃, 按文献条件(30 ℃)进行测试, 结果显示谱峰受温度影响变化较小, 该峰仍未变为单峰, 可见文献结果[11-12]与实验事实不符。δ4.16(s, 4H)与δ4.03(s, 4H)均为单峰, 化学位移也较为接近, 单凭经验推断可能会得出错误的归属, 故需要结合DEPT(Distortionless Enhancement by Polarization Transfer, 不失真的极化转移增强)及gHSQC技术作进一步确认。
碳谱有12条谱线, 证明分子具有对称结构。通过DEPT分析可区分碳的杂化类型, 分子中有两种亚甲基(δ56.89, δ56.22)、八种次甲基(δ129.18, δ128.33, δ128.14, δ128.05, δ126.72, δ126.62, δ80.66, δ76.92)、两种季碳(δ140.75, δ140.72), 与分子结构一致。依据谱线强度分析, δ140.75一高与δ140.72一低两种季碳信号分别归属为C—13/20/28/33与C—5/9。同理, δ56.22与δ56.89分别归属为五元环所连四个苄基中的亚甲基及剩余的两个亚甲基。δ76.92与δ80.66分别归属为五元环内次甲基及桥头次甲基。苯环区δ131.00~δ125.00三高三低6个CH信号, 分别属于五元环上所连4个苯环与五元环外2个苯环的CH信号, 根据强度可指认126.72与126.62分别为C—16/23/25/36与C—2/12。其他碳具体归属还需要结合二维核磁进行分析。
1H-13C gHSQC则将直接相连的碳与氢的信号一一对应, 根据已知的碳的位移可确定如下归属:如δ3.58(s, 4H)与δ80.66(C—45/48)有相关信号, 故可确定δ3.58为H—45/48, 相应的, δ4.16(s, 4H)与δ76.92(C—43/44/46/47)有相关信号, 证实其应为次甲基H—43/44/46/47, 而δ4.03(s, 4H)与δ56.89(C—31/38)有相关信号, 证实其应为亚甲基C—31/38上的氢。Nielsen等[11-12]将δ4.16(s, 4H)指认为亚甲基上的氢, 将δ4.03(s, 4H)指认为次甲基上的氢, 与本实验事实不符, 显然是错误的。由于芳环氢信号较为拥挤, 难以直接辨认, 可由芳环碳信号(下文归属)所对应的gHSQC相关信号中间接获得。
1H-13C gHMBC谱可检测到碳与氢的远程相关信号(通常为二、三键), 如δ56.22(C—39/40/41/42)、δ56.89(C—31/38)分别与δ3.58 (H—45/48)、δ4.16(H—43/44/46/47)相关, 同时还与芳环有相关信号, 证实6个苄基与异伍兹烷相连, 进一步证实了结构。另外, 芳环次甲基δ128.33、δ129.18分别与烷基区的亚甲基H—31/38、H—39/40/41/42有相关信号, 归属δ128.33、δ129.18分别为C—4/6/8/10与C—14/18/19/21/27/29/32/34, 从而δ128.14、δ128.05应分别为C—15/17/22/24/25/27/32/34与C—1/3/7/11。从谱图中还可观测到芳环碳与间位氢的较强相关信号, 符合芳环氢碳远程偶合三键强于二键的规律, 与其结构一致。
至此, 通过1D NMR和2D NMR的测试和谱图解析, 对HBIW的1H NMR、13C NMR信号进行了完全归属, 确证了该结构与Scheme 1相符。有关NMR详细数据归属见表 3。
| 表 3 HBIW的1H、13C NMR数据(CDCl3, 25 ℃) Tab.3 Data of 1H NMR and 13C NMR for HBIW (CDCl3, 25 ℃) |
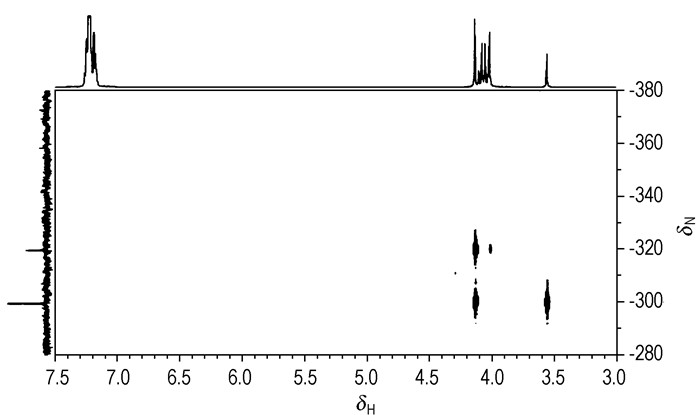
为了进一步确认其结构, 利用15N NMR及二维1H-15N gHMBC对化合物HBIW进行了结构分析, 结果见表 4。15N NMR中发现2个氮信号, 分别为δ-317.0与δ-297.1, 在二维1H-15N gHMBC(图 3)中, δ-317.0与五元环内CH有相关峰, 同时还与六元环苄基亚甲基有较弱的相关信号, 归属为N—1/2与相邻碳上氢的二键相关信号。δ-297.1也与五元环内CH信号相关, 同时还与异伍兹烷桥头CH信号相关, 分析其应为五元氮环上的N—3/4/5/6信号。数据列入表 4。
| 表 4 HBIW的15N NMR数据(CDCl3, 25 ℃) Tab.4 15N NMR data for HBIW (CDCl3, 25 ℃) |
|
图 3 1H-15N gHMBC of HBIW (CDCl3) Fig.3 HBIW的1H-15N gHMBC NMR谱 |
采用单晶衍射技术分析了在丙酮溶液中培养的HBIW单晶结构, 获得了其晶体结构参数。采用一维及二维1H、13C、15N NMR技术, 分别在氘代氯仿、氘代丙酮、氘代二甲基亚砜溶液中, 对HBIW的结构进行了表征, 讨论了在三种溶液中的NMR信号特征, 修正了文献中的错误, 完成了HBIW的核磁信号全归属。
(1) 通过单晶衍射确认了HBIW的化学结构及晶体结构, 由于较大的环张力, 苯环与五元环有一定扭曲, 五元氮杂环所连4个苄基N—C键长稍长于环外的2个苄基N—C键长。
(2) HBIW在氯仿溶液中具有最佳图谱特征, 通过1H NMR、13C NMR、15N NMR一维及二维NMR技术, 完成HBIW的核磁全归属, 确认其1H位移δ4.16(s, 4H)和δ4.03(s, 4H)分别为六元环上CH及六元环所连苄基上的CH2, 15N位移分别为δ-317.0(六元环)和δ-297.1(五元环)。
| [1] |
Nielsen A T, Chafin A P, Christian S L, et al. Synthesis of polyazapolycyclic caged polynitramines[J].
Tetrahedron, 1998, 54(39): 11793-11812. DOI:10.1016/S0040-4020(98)83040-8 |
| [2] |
刘进全, 王建龙, 韩伟荣, 等. 六苄基六氮杂异伍兹烷(HBIW)氢解反应及产物晶体结构[J].
含能材料, 2003, 11(1): 4-7. LIU Jin-quan, WANG Jian-long, HAN wei-rong, et al. Study on hyogenolysis of HBIW and crystal structures of the reaction products[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2003, 11(1): 4-7. |
| [3] |
赵信岐, 施倪承. ε-六硝基六氮杂异伍兹烷的晶体结构[J].
科学通报, 1995, 40(23): 2158-2160. DOI:10.3321/j.issn:0023-074X.1995.23.013 |
| [4] |
方涛, 孙成辉, 赵信岐. 四乙酰基二硝基六氮杂异伍兹烷的合成与表征[J].
含能材料, 2004, 12(5): 291-293. FANG Tao, SUN Chen-hui, ZHAO Xin-qi. Synthesis and Characterization of Teraacetyldinitrohexaazaisowutzitane[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2004, 12(5): 291-293. |
| [5] |
孙成辉, 方涛, 杨宗云, 等. 硝-硫混酸硝化四乙酰基六氮杂异伍兹烷制备CL-20反应机理[J].
含能材料, 2009, 17(2): 161-164. SUN Chen-hui, FANG Tao, YANG Zong-yun, et al. Reaction mechanism of preparation CL-20 from tetraacetylhexaazaisowurtzitane nitrated by Mixture of nitric Acid and sulfuric Acid[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(2): 161-164. |
| [6] |
赵信岐, 方涛, 孙成辉. 六硝基六氮杂异伍兹烷制备工艺研究开发新进展[J].
兵工学报, 2004, 25(3): 354-358. ZHAO Xin-Qi, FANG Tao, SUN Chen-hui. Research and development of HNIW synthesis[J]. Acta Armanentarii, 2004, 25(3): 354-358. |
| [7] |
王昕, 彭翠枝. 国外六硝基六氮杂异伍兹烷的发展现状[J].
火炸药学报, 2007, 30(5): 45-48. WANG Xin, PENG Cui-zhi. Development of hexanitrohexaazaisowurtaitane at abroad[J]. Chinese Journal of Explosives and Propellants, 2007, 30(5): 45-48. |
| [8] |
欧育湘, 孟征, 刘进全. 高能量密度化合物CL-20的合成和制备工艺进展[J].
化工进展, 2007, 26(6): 762-768. OU Yu-xiang, MENG Zheng, LIU Jin-quan. Advance in high energy density compound CL-20-developments of synthesis route and production technologies of CL-20[J]. Chemical Industry and Engineering Progress, 2007, 26(6): 762-768. |
| [9] |
欧育湘, 徐永江, 刘利华, 等. 乙腈法与乙醇法合成六苄基六氮杂异伍兹烷的比较[J].
含能材料, 1999, 7(4): 152-156. OU Yu-xiang, XU Yong-jiang, LIU Li-hua, et al. Comparison of acetonitrile process with ethanol process for synthesis of hexabenzylhexaazaisowurtzitane[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 1999, 7(4): 152-156. |
| [10] |
郑福平, 欧育湘, 陈江涛, 等. 有机酸催化合成2, 4, 6, 8, 10, 12-六苄基-2, 4, 6, 8, 10, 12-六氮杂异伍兹烷[J].
精细化工, 2000, 17(1): 27-29. ZHENG Fu-ping, OU Yu-xiang, CHEN Jiang-tao, et al. Preparation of 2, 4, 6, 8, 10, 12-hexabenzy-l 2, 4, 6, 8, 10, 12-hexaazaisowurtzitane catalyzed by organic acids[J]. Fine Chemicals, 2000, 17(1): 27-29. |
| [11] |
Nielsen A T, Nissan R A, Venderah D J, et al. Polyazapolycyclics by condensation of aldehydes with amines. formation of 2, 4, 6, 8, 10, 12-hexabenzyl-2, 4, 6, 8, 10, 12-hexaazatetracyclo[5.5.0.05, 9.03, 11] dodecafnreosm glyoxal and benzylamines1[J].
Org Chem, 1990, 55: 1459-1466. DOI:10.1021/jo00292a015 |
| [12] |
Sikder A K, Sikder Nirmala, Gandhe B R, et al. Hexanitrohexaazaisowurtaitane or CL-20 in India: synthesis and characterisation[J].
Defence Science Journal, 2002, 52(2): 135-146. DOI:10.14429/dsj.52.2158 |

The single crystal structure of HBIW was determined by X-ray single diffractiometer analysis and the molecular structure of HBIW was established by a combination of 1D (1H NMR, 13C NMR and 15N NMR) and 2D (gHSQC and gHMBC) NMR techniques.



