硝基苯类化合物是重要的含能材料, 广泛应用于炸药、石油化工、燃料等行业[1]。在炸药工业排放的污染物中, 废水所占比例最高, 大约占了各种污染物的75%以上[2], 在其产生的废水中含有多种硝基苯类化合物[3], 如梯恩梯(TNT)、地恩梯(DNT)、三硝基苯(TNB)和硝基苯(NB)等。这些污染物往往含能高、爆炸性强、毒性较大, 并且硝基苯类化合物化学性质稳定, 不易被生物降解, 具有强烈的致癌致突变性, 如果不经处理直接排放, 会对环境造成重大污染, 已被美国环境保护署(EPA)划为第一类环境危害物质[4-5]。目前该类炸药废水处理的方法通常是先经化学氧化法预处理, 提高废水可生化性[6-7], 再利用生物法降解处理[8-9], 达到国家规定的排放标准。
臭氧是绿色无污染的强氧化剂(氧化还原电位2.07 V), 自然界中氧化能力仅次于氟(氧化还原电位2.87 V)[10], 现已广泛应用于炸药废水处理领域。基于臭氧分解产生羟基自由基(氧化还原电位2.8 V)的高级氧化技术, 由于不受废水种类、成分、浓度的限制, 且不会造成二次污染, 已成为环保领域研究的热点[11-13]。由于羟基自由基在氧化过程中起主导作用, 所以学者们希望通过耦合不同工艺来提高臭氧在水中的分解速率, 产生强氧化性的羟基自由基从而提高氧化效率。臭氧的分解速率可表示为:-rO3=k×CLO3。由此可以看出, 提高反应速率系数k值和液相中臭氧浓度CLO3都可以增加臭氧分解产生羟基自由基的速率。目前, 大部分工艺研究主要集中在如何提高k值上, 如O3/H2O2[14]、O3/UV[15]、O3/催化剂[16]、O3/超声波[17]等组合工艺。但少有科技工作者通过提高水中臭氧浓度CLO3的方法, 即提高臭氧的传质效率使单位时间内溶解于水中的臭氧量增加, 进而生成更多的羟基自由基来提高氧化效率。主要原因是臭氧水溶性差[18], 传质过程属于液膜控制过程, 而常规方法对气液传质面积提高不明显。因此, 增大气液传质面积和加速气液相界面更新速率将为强化臭氧高级氧化工艺开辟一条新途径。
旋转填料床(Rotating Packed Bed, RPB)通过产生离心力来模拟超重力场, 是一种能强化传递反应过程的新型设备[19]。在超重力场中, 废水被高速旋转的填料切割成较小的液滴、液丝和液膜, 极大的提高了气液接触面积和降低了液膜阻力, 强化了气液传质过程[20-21]。所以对于臭氧组合工艺处理含硝基苯类化合物废水来说, 结合超重力技术有很大的应用前景。
为更好了解臭氧高级氧化工艺降解含硝基苯类化合物炸药废水的特性, 本研究以硝基苯类化合物为模拟污染物, 考察超重力因子、初始pH值、双氧水浓度、液体流量和处理时间等因素在不同臭氧氧化工艺(旋转填料床(RPB)-O3/H2O2工艺、RPB-O3工艺、曝气反应装置(Bubbling Reactor, BR)-O3/H2O2工艺和BR-O3工艺)中对其去除率的影响。分析了不同氧化工艺对硝基苯类化合物的降解能力, 筛选出高效的氧化降解工艺。探讨了不同氧化工艺下的臭氧氧化降解动力学, 以期为超重力技术在臭氧氧化硝基苯类炸药废水处理领域提供一定的理论基础。
2 实验部分 2.1 实验材料主要试剂:30%的过氧化氢, 分析纯, 天津市天力化学试剂有限公司; 重铬酸钾, 分析纯, 上海浦江化工厂; 硫酸亚铁铵, 分析纯, 成都化学试剂厂; α-萘基乙二胺二盐酸盐, 分析纯, 天津市东丽区天大化学试剂厂; 二甲基甲酰胺、硝基苯, 分析纯, 天津市科密欧化学试剂开发中心。
模拟含硝基苯类化合物废水, 由硝基苯与去离子水配制而成。废水水质:pH为7.5, 硝基苯类化合物浓度为200 mg·L-1, 化学需氧量CODCr=557 mg·L-1。
2.2 实验装置与方法实验装置采用自制的错流型旋转填料床, 转子内填料为不锈钢波纹丝网填料, 内径40 mm, 外径75 mm, 轴向高度75 mm。
仪器设备:戴安Ultimate 3000液相色谱仪、721型分光光度计、LBC-50W(S)型臭氧发生器(山东绿邦光电设备有限公司)、ZML-2型湿式气体流量计(余姚市银环流量仪表有限公司)、PHS-3C型精密酸度计等。
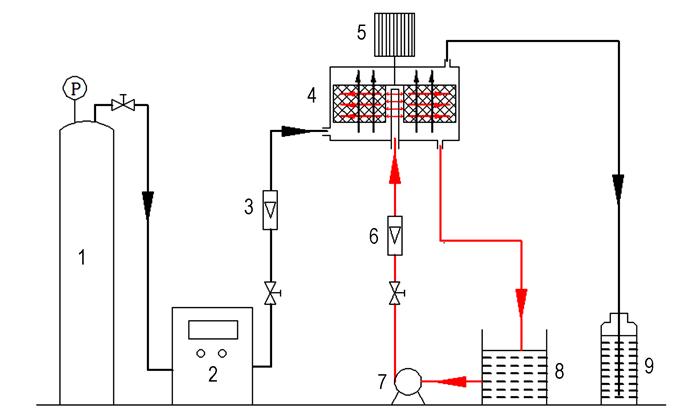
2.3 实验方案 2.3.1 RPB-O3/H2O2工艺和RPB-O3工艺实验在室温(18±1) ℃下进行, 整个反应过程近似认为恒温。RPB-O3/H2O2工艺处理硝基苯类化合物废水的工艺流程如图 1所示:氧气经臭氧发生器产生一定浓度的臭氧气体, 经气体流量计进入旋转填料床底部, 然后向上通过填料。液体由储液槽经泵循环送入旋转填料床中心, 然后沿径向甩出, 同时与从下方进入的气体错流接触, 进行氧化反应。液体甩到壁面后由液相出口流到储液槽内, 进行循环。未反应的气体进入尾气处理罐。本工艺先在废水中加入双氧水, 然后在超重力场中与臭氧错流接触反应。RPB-O3工艺流程和上述基本一致, 区别在于废水中没有添加双氧水。
|
图 1 实验工艺流程图 1—氧气瓶, 2—臭氧发生器, 3—气体流量计, 4—旋转填料床, 5—电机, 6—液体流量计, 7—泵, 8—储液槽, 9—尾气处理装置 Fig.1 Diagram of experiment process flow 1—oxygen bottle, 2—ozone generator, 3—gas flowmeter, 4—rotating packed bed, 5—electromotor, 6—fluid flowmeter, 7—liquid pump, 8—fluid reservoir, 9—tail gas treating unit |
将产生的臭氧通过气体流量计计量, 通入装有废水的曝气反应装置中(DN50-Φ56 mm, 500 mm), 采用砂芯曝气头于反应器底部布气, 臭氧经曝气头成细小气泡与废水接触反应, 考察不同条件下的处理效果。
2.4 分析方法废水的处理效果以硝基苯类化合物去除率来表示, 浓度采用戴安Ultimate 3000液相色谱仪测定, 检测波长262 nm, C18反相柱(250 mm×4.6 mm×5 μm), 流动相:甲醇/水(70/30), 流速:0.9 mL·min-1, 柱温20 ℃, 进样量20 μL。硝基苯类化合物去除率的计算公式为:
| $ \eta = \frac{{{C_0}-{C_t}}}{{{C_0}}} \times 100\% $ | (1) |
式中, C0和Ct分别为处理前后的硝基苯类化合物浓度, mg·L-1。
3 结果与讨论 3.1 超重力因子对RPB-O3/H2O2和RPB-O3工艺处理效果影响超重力因子β是用来衡量超重力场强弱的无量纲, 是旋转填料床的平均离心加速度与重力加速度之比[22]。超重力因子β对有机物降解影响的显著与否, 决定了超重力技术能否强化臭氧氧化法降解含硝基苯类化合物废水。
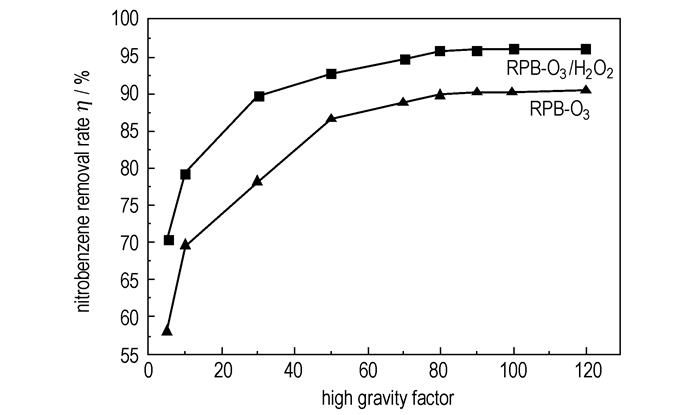
调节水样的初始pH值为10.5, 液体流量120 L·h-1, 气体流量75 L·h-1, 臭氧浓度50 mg·L-1, RPB-O3/H2O2工艺中添加双氧水使其浓度为4.9 mmol·L-1。处理25 min, 考察超重力因子对硝基苯类化合物去除率的影响, 结果如图 2所示。
|
图 2 超重力因子(β)对硝基苯类化合物去除率的影响 Fig.2 Influence of high gravity factor(β) on nitrobenzene compounds removal rate |
从图 2可以看出, 当超重力因子β从5增加到120时, RPB-O3/H2O2工艺和RPB-O3工艺中硝基苯类化合物的去除率分别从70.4%增加到96.1%和从58.1%增加到90.5%。在与之对应的操作条件下利用去离子水吸收臭氧气体(单次吸收), 当超重力因子从5增加到120时, 臭氧水浓度从1.07 mg·L-1增加到了2.61 mg·L-1。分析可知, 增大超重力因子可提高硝基苯类化合物的去除率, 是通过提高臭氧传质速率和臭氧水浓度来实现的。因为臭氧氧化硝基苯类化合物受臭氧从气相到液相传质速率的控制, 而传质过程为液膜控制过程[23], 随着旋转填料床转速的不断增大, 超重力因子越来越大, 废水在超重力场中受到填料强大的剪切力作用, 被切割成细小的液丝、液滴和液膜, 极大地降低了液膜的厚度和液滴的大小, 增大了气液相间接触面积和相界面更新速度, 有效地提高了臭氧从气相到液相的传质速率, 进而提高了氧化效率。当超重力因子为80, 处理时间25 min, RPB-O3工艺和RPB-O3/H2O2工艺对硝基苯类化合物的去除率分别达到88.7%和95.8%。当处理时间为40 min, RPB-O3/H2O2工艺出水中硝基苯类化合物浓度小于3 mg·L-1, 达到国家二级排放标准(GB 8978-1996)。当超重力因子超过80时, 去除率趋于平缓, 此时再提高转速对传质的促进作用不明显, 反而会增加过多的动力消耗。可见, 气液传质对反应有一定的上限, 故适宜条件选取β=80。
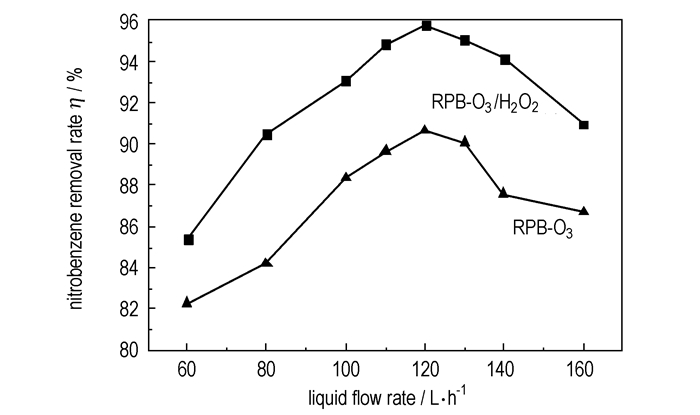
3.2 液体流量对RPB-O3/H2O2和RPB-O3工艺处理效果影响调节水样的初始pH=10.5, β=80, 气体流量75 L·h-1, 臭氧浓度50 mg·L-1, 双氧水浓度4.9 mmol·L-1。处理25 min, 考察不同液体流量下硝基苯类化合物的去除率, 结果如图 3所示。
|
图 3 液体流量对硝基苯类化合物去除率的影响 Fig.3 Influence of liquid flow rate(L) on nitrobenzene compounds removal rate |
从图 3可看出, 在气体流量一定的条件下, RPB-O3/H2O2工艺和RPB-O3工艺的处理效果随着液体流量的增加都表现出先增大后减小的趋势, 在液体流量为120 L·h-1时硝基苯类化合物的去除率达到最高。因为在较低液流量下, 旋转填料床中的填料不能被液体全部润湿, 气液接触面积没有实质性的提高, 并且单位时间内气液接触次数较少, 臭氧传质效率低, 造成O3气体的浪费, 经济上也不合理。但是当液体流量过大时, 虽然填料可以很好地被液体润湿, 但由于液体流量过大, 造成填料中液滴的尺寸和液膜的厚度增加, 液膜传质阻力变大, 并且气液接触时间变短, 因此, 不利于臭氧的传质[24]。综合考虑, 选取适宜的液体流量为120 L·h-1。
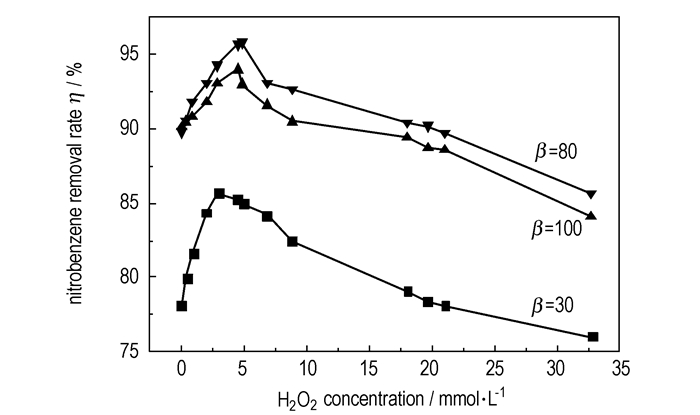
3.3 双氧水浓度对RPB-O3/H2O2工艺的影响调节水样的初始pH值为10.5, 液体流量120 L·h-1, 气体流量75 L·h-1, 臭氧浓度50 mg·L-1, 在超重力因子分别为30、80和100条件下, 处理25 min, 考察双氧水浓度对硝基苯类化合物去除率的影响, 结果如图 4所示。
|
图 4 双氧水浓度对硝基苯类化合物去除率的影响 Fig.4 Influence of H2O2 concentration CH2O2 on nitrobenzene compounds removal rate |
从图 4可看出, 在相同的超重力因子条件下, 随着双氧水浓度的增加, 硝基苯类化合物的去除率呈现先增大后减小的趋势。当超重力因子为30、80和100时, 适宜的双氧水浓度分别为2.9, 4.9, 4.5 mmol·L-1。在O3/H2O2工艺中, 羟基自由基的浓度与臭氧的传质效率是成正比的, 具体的说它取决于臭氧吸收的最大速率, 双氧水的作用主要是催化水中溶解的臭氧分解[24]。当超重力因子从30增加到80时, 臭氧的溶解速率不断提高, 双氧水和臭氧的适宜配比发生变化, 适宜双氧水浓度从2.9 mmol·L-1提高到4.9 mmol·L-1。但是从氧化机理中可以知道, 在臭氧的分解反应中, 双氧水的作用会发生变化, 它也可以通过自由基的链式反应, 抑制臭氧的分解。换言之, 双氧水浓度的增加抑制或是降低了硝基苯类化合物的去除速率。在低浓度时H2O2分解的中间产物HO2-是臭氧产生·OH的促进剂, 如式(a)~式(b)所示。但是当双氧水浓度高于临界值时, 过多的双氧水会与硝基苯类化合物竞争·OH, 使·OH浓度降低, 反而成了·OH的捕获剂, 如式(c)所示。故当超重力因子为80时, 适宜的双氧水浓度为4.9 mmol·L-1。
| $ {{\rm{H}}_{\rm{2}}}{{\rm{O}}_{\rm{2}}} \leftrightarrow {{\rm{H}}^{\rm{ + }}}{\rm{ + H}}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} $ | (a) |
| $ {{\rm{O}}_{\rm{3}}}{\rm{ + H}}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} \to {\rm{\cdot OH + }}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} $ | (b) |
| $ {{\rm{H}}_{\rm{2}}}{{\rm{O}}_{\rm{2}}}{\rm{ + \cdot OH}} \to {{\rm{H}}_{\rm{2}}}{\rm{O + \cdot H}}{{\rm{O}}_{\rm{2}}} $ | (c) |
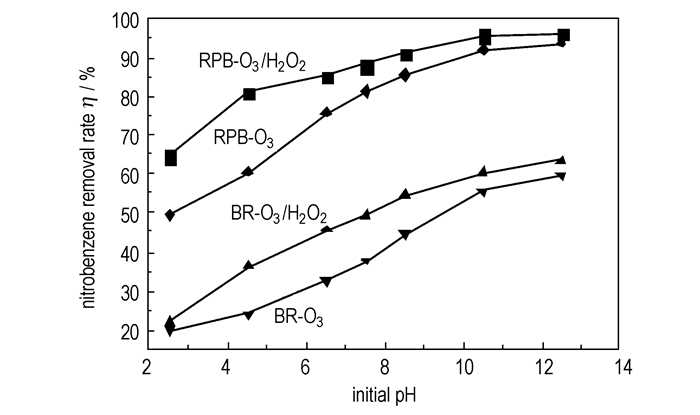
考察初始pH值对不同工艺处理效果的影响, 结果如图 5所示。
|
图 5 初始pH对硝基苯类化合物去除率的影响 Fig.5 Influence of initial pH value on nitrobenzene compounds removal rate |
从图 5中可以看出, 在酸性环境下, 四种工艺体系中硝基苯类化合物的去除率都不高, 但随着pH值的升高, 四种工艺对其去除率都显著提高。这是因为在酸性环境下, 臭氧不易分解产生·OH, 降解途径主要是臭氧直接氧化反应。而随着pH值的升高, 降解率明显上升, 主要原因是OH-在自由基链反应中起引发剂的作用, 使臭氧更容易分解产生为强氧化性的羟基自由基, 进而提高了氧化降解效率[25], 如式(d)和(e)所示, 综合考虑初始PH值选取10.5。
| $ {{\rm{O}}_{\rm{3}}}{\rm{ + O}}{{\rm{H}}^{\rm{ - }}} \to {\rm{H}}{{\rm{O}}_{\rm{2}}}^{\rm{ - }}{\rm{ + }}{{\rm{O}}_{\rm{2}}} $ | (d) |
| $ {{\rm{O}}_{\rm{3}}}{\rm{ + H}}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} \to {\rm{\cdot OH + }}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} $ | (e) |
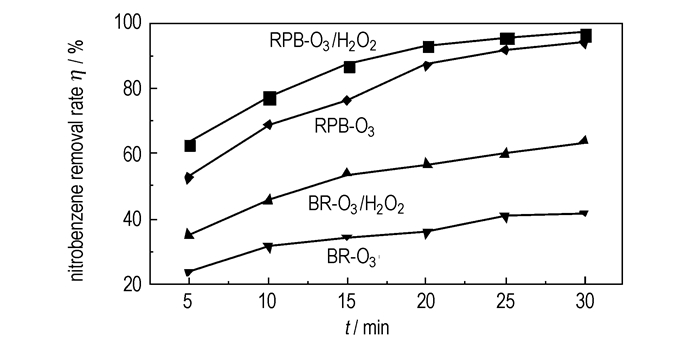
表 1给出了臭氧浓度为50 mg·L-1四种工艺的适宜条件, 在此条件下对比分析不同工艺对硝基苯类化合物去除率的影响, 结果如图 6所示。
| 表 1 操作条件 Tab.1 Operation conditions for four technology condition |
|
图 6 四种工艺条件的实验结果对比 Fig.6 Experimental results obtained by four technological conditions |
由图 6可知, 随着处理时间的增加, 四种工艺中硝基苯类化合物的去除率都呈增加的趋势。在处理时间25 min时, RPB-O3/H2O2工艺和RPB-O3工艺中其去除率达90%以上, BR-O3/H2O2工艺和BR-O3工艺对硝基苯类化合物的去除率仅分别为60.1%和40.9%。可见, 在臭氧氧化工艺中, 使用超重力技术可以很大程度地提高硝基苯类化合物的去除率。当处理时间为40 min, RPB-O3/H2O2工艺对硝基苯类化合物的去除率可达99%, 出水中硝基苯类化合物浓度小于3 mg·L-1, 达到国家二级排放标准(GB 8978-1996)。
对于O3/H2O2氧化工艺, 存在两个降解机理。
直接氧化:臭氧与有机物A的直接反应, 将其降解, 如式(f)所示。
| $ {{\rm{O}}_{\rm{3}}}{\rm{ + A}} \to {\rm{products}} $ | (f) |
间接氧化:双氧水催化臭氧反应生成氧化性更强的羟基自由基(·OH), 将硝基苯类化合物氧化降解成小分子物质, 并进一步矿化, 如式(g)和(h)所示。在碱性条件下, 此过程占主导作用[26]。
| $ {{\rm{H}}_{\rm{2}}}{{\rm{O}}_{\rm{2}}} \leftrightarrow {{\rm{H}}^{\rm{ + }}}{\rm{ + H}}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} $ | (g) |
| $ {{\rm{O}}_{\rm{3}}}{\rm{ + H}}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} \to {\rm{\cdot OH + }}{{\rm{O}}_{\rm{2}}}{\rm{ + }}{{\rm{O}}_{\rm{2}}}^{\rm{ - }} $ | (h) |
从机理分析中可以明显看出, 臭氧从气相到液相的溶解速率和生成羟基自由基的速率是决定硝基苯类化合物去除率的关键。实验数据显示, 在相同的处理时间下, 使用超重力技术的处理工艺(RPB-O3/H2O2工艺和RPB-O3工艺)对硝基苯类化合物的去除率明显高于传统曝气处理工艺(BR-O3/H2O2工艺和BR-O3工艺)。这是因为在反应过程中, 超重力场通过改变气-液相界面的流动形态, 使得气相液相微观混合和传质过程得到极大强化[27], 进而提高了臭氧溶解速率和氧化效率。对于O3/H2O2氧化工艺和O3氧化工艺, 双氧水的存在, 可以协同臭氧加速分解产生大量氧化性更强的羟基自由基, 加快硝基苯类化合物的降解过程, 进而提高其去除效果。实验结果表明, 在处理5 min时, RPB-O3/H2O2工艺对硝基苯类化合物的去除率比RPB-O3工艺高出10.5%, BR-O3/H2O2工艺下的去除率比BR-O3工艺高出11.3%, 证明双氧水的存在强化了臭氧氧化降解硝基苯类化合物的能力。
综合分析可知, RPB-O3/H2O2工艺对硝基苯类化合物具有较强的降解能力, 可作为含硝基苯类化合物炸药废水的预处理工艺。
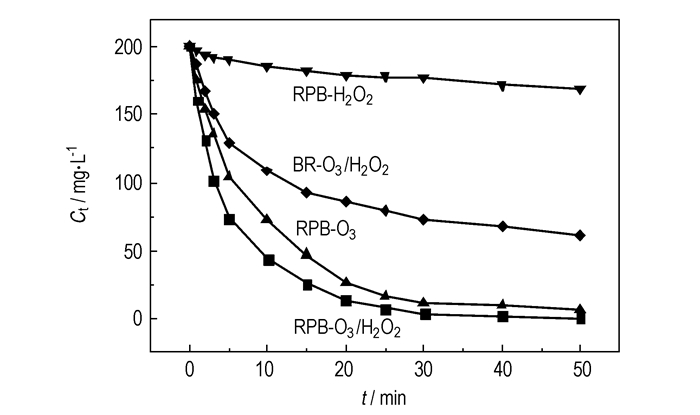
5 不同组合工艺降解硝基苯类化合物的动力学在适宜条件下, 分别考察RPB-O3/H2O2、BR-O3/H2O2、RPB-O3和RPB-H2O2四种工艺处理废水时硝基苯类化合物浓度Ct随时间t的变化规律, 结果如图 7所示。
|
图 7 硝基苯类化合物质量浓度随时间的变化规律 Fig.7 Nitrobenzene compounds mass concentration vs reaction time |
从图 7可看出, RPB-H2O2工艺对硝基苯类化合物的降解能力非常有限, 只有少许发生了降解, 证明超重力技术并不能强化双氧水氧化降解能力。而RPB-O3工艺对硝基苯类化合物的去除率比较高, 但是这两种处理方法下的去除率相加总和低于RPB-O3/H2O2工艺对硝基苯类化合物的去除率。这说明超重力、臭氧和双氧水之间存在协同作用, 强化了氧化降解硝基苯类化合物的能力。
分析实验结果可知, 在臭氧氧化降解硝基苯类化合物的过程中, 存在臭氧分子的直接氧化和羟基自由基的间接氧化, 如式(2)所示; 当存在双氧水时, 增加了双氧水的直接氧化作用, 如式(3)所示。
| $ - \frac{{{\rm{d}}\left[C \right]}}{{{\rm{d}}t}} = {k_{{{\rm{O}}_{\rm{3}}}}}\left[C \right] + {k_\cdot}_{{\rm{OH}}}[C] $ | (2) |
| $ - \frac{{{\rm{d}}\left[C \right]}}{{{\rm{d}}t}} = {k_{{{\rm{O}}_{\rm{3}}}/{{\rm{H}}_{\rm{2}}}{{\rm{O}}_2}}}\left[C \right] = {k_{{{\rm{O}}_3}}}\left[C \right] + {k_{{{\rm{H}}_{\rm{2}}}{{\rm{O}}_2}}}\left[C \right] + {k_{\cdot{\rm{OH}}}}[C] $ | (3) |
式(2)和式(3)中, kO3、kH2O2和k·OH分别表示臭氧、双氧水和羟基自由基单独氧化时的反应速率常数, min-1; [C]表示t时刻硝基苯类化合物的浓度, mol·L-1。
研究尝试用表观假一级反应动力学方程拟合硝基苯类化合物在四种工艺下的降解, 如式(4)。
| $ {\rm{ln}}\left( {\frac{{{c_0}}}{{{c_{\rm{t}}}}}} \right) = kt + b $ | (4) |
式中, C0、Ct分别为初始浓度和t时刻的浓度, mol·L-1; k为表观假一级反应动力学常数, min-1。在O3氧化工艺中, k=kO3+k·OH; 在O3/H2O2氧化工艺中, k=kO3+kH2O2+k·OH。所拟合的表观假一级反应动力学常数k见表 2。
| 表 2 表观假一级反应速率常数和相关系数 Tab.2 Apparent pseudo-first-order reaction rate constant and correlation coefficient |
从表 2可看出, 拟合的相关系数较高, 表明硝基苯类化合物在四种工艺下的降解都较符合表观假一级动力学。在超重力场中, 双氧水的加入可以提高臭氧氧化降解硝基苯类化合物的速率, 速率常数k从0.08430 min-1提高到0.11008 min-1。超重力环境下, O3/H2O2工艺中硝基苯类化合物的降解速率常数明显高于传统曝气反应条件下的降解速率常数, k从0.02231 min-1提高到0.11008 min-1, 强化效果非常明显, 证明RPB结合O3/H2O2氧化工艺可用于含硝基苯类化合物炸药废水的预处理阶段。
6 结论(1) 在RPB-O3/H2O2、RPB-O3、BR-O3/H2O2和BR-O3四种工艺中, 超重力环境下臭氧氧化效率得到很大提高, 对硝基苯类化合物表现出较强的降解性能。
(2) 对于RPB-O3/H2O2工艺和RPB-O3工艺, 硝基苯类化合物去除率随着超重力因子、初始pH值的增大而增大, 而随着双氧水浓度和液体流量的增大, 表现为先增加后减小的趋势。当超重力因子为80, 双氧水浓度为4.9 mmol·L-1, 液体流量120 L·h-1和初始pH=10.5时, 处理40 min去除率可达99%, 硝基苯类化合物达国家二级排放标准(GB 8978-1996)。
(3) 在RPB-O3/H2O2、RPB-O3、RPB-H2O2和BR-O3/H2O2四种工艺中硝基苯类化合物降解都符合表观假一级动力学。RPB-O3/H2O2工艺中降解速率常数明显高于BR-O3/H2O2工艺中的降解速率常数, k从0.02231 min-1提高到0.11008 min-1, 说明RPB-O3/H2O2工艺可用于含硝基苯类化合物炸药废水的预处理。
| [1] |
肖忠良, 胡双启, 吴晓青, 等.
火炸药的安全与环保技术[M]. 北京: 北京理工大学出版社, 2006.
|
| [2] |
孙荣康, 瞿美林, 陆才正.
火炸药工业的污染及其防治[M]. 北京: 兵器工业出版社, 1990.
|
| [3] |
郭亮, 焦纬洲, 刘有智, 等. 含硝基苯类化合物废水处理技术研究进展[J].
化工环保, 2013, 33(4): 299-303. GUO Liang, JIAO Wei-zhou, LIU You-zhi, et al. Research progresses in treatment of wastewater containing nitrobenzene compounds[J]. Environmental Protection of hemical Industry, 2013, 33(4): 299-303. |
| [4] |
邢立群, 郑新梅, 刘红玲, 等. 中国主要河流中硝基苯生态风险研究[J].
中国环境科学, 2011, 31(2): 301-306. XING Li-qun, ZHENG Xin-mei, LIU Hong-ling, et al. Ecological risk assessment of nitrobenzene in main rivers of China[J]. China Environmental Science, 2011, 31(2): 301-306. |
| [5] |
JIAO Wei-zhou, LIU You-zhi, LIU Wen-li, et al. Degradation of nitrobenzene-containing wastewater with O3 and H2O2 by high gravity technology[J].
China Petroleum Processing and Petrochemical Technology, 2013, 15(1): 85-94. |
| [6] |
常双君, 刘玉存. 超临界水氧化处理TNT炸药废水的研究[J].
含能材料, 2007, 15(3): 285-288. CHANG Shuang-jun, LIU Yu-cun. Treatment of TNT wastewater by supercritical water oxidation[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2007, 15(3): 285-288. |
| [7] |
吴耀国, 焦剑, 赵大为, 等. 炸药废水处理的高级氧化技术[J].
含能材料, 2003, 11(3): 166-169. WU Yao-guo, JIAO Jian, ZHAO Da-wei, et al. Advance oxidation process for treatment of waste water contaminated by explosives[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2003, 11(3): 166-169. |
| [8] |
王惠娥, 孙继林, 颜事龙, 等. 白腐真菌-泥炭净化处理DDNP废水[J].
含能材料, 2013, 21(3): 367-371. WANG Hui-e, SUN Ji-lin, YAN Shi-long, et al. Waste-water treatment of diazodinitrophenel by white rot fungus-peat[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2013, 21(3): 367-371. |
| [9] |
王仁桃, 任云霞, 刘黎, 等. 厌氧悬浮填料生物膜反应器处理费托合成废水[J].
燃料化学学报, 2011, 39(4): 307-310. WANG Ren-tao, REN Yun-xia, LIU Li, et al. Performance of anaerobic-aerobic MBBR system for treating Fischer-Tropsch-processing wastewater[J]. Journal of Fuel Chemistry and Technology, 2011, 39(4): 307-310. |
| [10] |
Beltrán, Fernando J.
Ozone reaction kinetics for water and wastewater systems[M]. Taylor & Francis Routledge, 2004 |
| [11] |
ZENG Ze-quan, ZOU Hai-kui, LI Xin, et al. Degradation of phenol by ozone in the presence of fenton reagent in a rotating packed bed[J].
Chemical Engineering Journal, 2013, 229: 404-411. DOI:10.1016/j.cej.2013.06.018 |
| [12] |
刁金祥, 刘有智, 王贺, 等. 旋转填料床中O3/H2O2法处理TNT红水[J].
含能材料, 2007, 15(3): 281-284. DIAO Jin-xiang, LIU You-zhi, WANG He, et al. O3/H2O2 oxidative treatment of TNT red-water in a rotating packed bed[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2007, 15(3): 281-284. |
| [13] |
贾瑛, 李毅, 张秋禹. UV-Fenton方法处理偏二甲肼废水[J].
含能材料, 2009, 17(3): 365-368. JIA Ying, LI Yi, ZHANG Qiu-yu. Degradation of unsymmetrialdimethy hydrazine wastewater by UV-Fenton process[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(3): 365-368. |
| [14] |
Park C G, Choi E S, Jeon H W, et al. Effect of nitrate on the degradation of bisphenol A by UV/H2O2 and ozone/H2O2 oxidation in aqueous solution[J].
Desalination and Water Treatment, 2014, 52(4-6): 797-804. DOI:10.1080/19443994.2013.827297 |
| [15] |
Van Aken P, Van Eyck K, Degrève J, et al. COD and AOX removal and biodegradability assessment for fenton and O3/UV oxidation processes:a case study from a graphical industry wastewater[J].
Ozone:Science & Engineering, 2013, 35(1): 16-21. |
| [16] |
Pengphol S, Uthaibutra J, Arquero O, et al. Oxidative degradation and detoxification of chlorpyrifos by ultrasonic and ozone treatments[J].
Journal of Agricultural Science, 2012, 4(8): 164 |
| [17] |
Colombo A, Cappelletti G, Ardizzone S, et al. Bisphenol A endocrine disruptor complete degradation using TiO2 photocatalysis with ozone[J].
Environmental Chemistry Letters, 2012, 10(1): 55-60. DOI:10.1007/s10311-011-0328-0 |
| [18] |
储金宇, 吴春笃, 陈万金, 等.
臭氧技术及应用[M]. 北京: 化学工业出版社, 2002: 23-24.
|
| [19] |
刘有智.
超重力化工过程与技术[M]. 北京: 国防工业出版社, 2009: 1-5.
|
| [20] |
邹海魁, 邵磊, 陈建峰. 超重力技术进展—从实验室到工业化[J].
化工学报, 2006, 57(8): 1810-1816. ZOU Hai-kui, SHAO Lei, CHEN Jian-feng. Progress of higee technology-from laboratory to commercialization[J]. Journal of Chemical Industry and Engineering(China), 2006, 57(8): 1810-1816. |
| [21] |
JIAO Wei-zhou, LIU You-zhi, QI Gui-sheng. Gas pressure drop and mass transfer characteristics in cross-flow rotating packed bed with porous plate packing[J].
Industrial & Engineering Chemistry Research, 2010, 49(8): 3732-3740. |
| [22] |
JIAO Wei-zhou, LIU You-zhi, QI Gui-sheng. Micromixing efficiency of viscous media in novel impinging stream-rotating packed bed reactor[J].
Industrial & Engineering Chemistry Research, 2012, 51(20): 7113-7118. |
| [23] |
焦纬洲, 刘有智, 侯晓婷, 等. 酸析与超声波-超重力-臭氧氧化法联合预处理二硝基甲苯废水[J].
化工环保, 2011, 31(3): 239-243. JIAO Wei-zhou, LIU You-zhi, HOU Xiao-ting, et al. Pretreatment of DNT wastewater by acid precipitation and ultrasonic-high gravity-ozone oxidation process[J]. Environmental Protection of Chemical Industry, 2011, 31(3): 239-243. |
| [24] |
ZENG Ze-quan, WANG Jun-fang, LI Zen-hao, et al. The advanced oxidation process of phenol solution by O3/H2O2 in a rotating packed bed[J].
Ozone:Science & Engineering, 2013, 35(2): 101-108. |
| [25] |
梁晓贤, 刘有智, 焦纬洲, 等. RPB-O3/H2O2法处理含黑索今废水的实验研究[J].
现代化工, 2012, 32(9): 89-92. LIANG Xiao-xian, LIU You-zhi, JIAO Wei-zhou, et al. Experimental research on treatment of RDX wastewater with RPB-O3/H2O2[J]. Modern Chemical Industry, 2012, 32(9): 89-92. |
| [26] |
LIN Chia-chang, CHAO Chen-yu, LIU Mei-yun, et al. Feasibility of ozone absorption by H2O2 solution in rotating packed beds[J].
Journal of Hazardous Materials, 2009, 167(1): 1014-1020. |
| [27] |
JIAO Wei-zhou, LIU You-zhi, QI Gui-sheng. A new impinging stream-rotating packed bed reactor for improvement of micromixing iodide and iodate[J].
Chemical Engineering Journal, 2010, 157(1): 168-173. DOI:10.1016/j.cej.2009.11.032 |

Four combined processes of RPB-O3/H2O2, RPB-O3, BR-O3/H2O2 and BR-O3 were experimentally conducted to treat nitrobenzene compounds in simulated wastewater.




