Mn3O4以其独特的物理化学性质在电池材料、信息存储、环境治理、催化反应等领域获得了广泛的应用, 成为近年来研究的热点[1-3]。Mn3O4材料的形貌、尺寸和表面状态对其物理化学性质及应用性能有着非常重要的影响, 因此, 研究特定形貌的Mn3O4的性能具有非常重要的意义。Dubal等[4]制备了介孔结构的Mn3O4片层并证明了它具有较好的电化学性能; Du等[5]报道了Mn3O4纳米棒的合成并研究其磁学性质; Li等[6]在石墨烯片层上成功负载了超细的Mn3O4纳米粒子并报道了其优异的催化性能, 但是目前就Mn3O4纳米微球的合成及其性质还鲜见报道。
高氯酸铵(AP)是复合固体推进剂常用的氧化剂, 其分解特性对推进剂的燃烧有重要影响[7-8]。通常情况下, 降低AP的分解温度就能得到更高的燃速, 而过渡金属氧化物(Fe2O3、CuO、Cr2O3、Co2O3等)是AP热分解常用的催化剂[8-12]。不过, 将Mn3O4纳米微球添加到AP基复合推进剂中的报道还很少。为了进一步提高AP基复合推进剂的燃烧速率, 在制备Mn3O4纳米粒子的基础之上, 探讨Mn3O4纳米粒子对AP热分解性质的影响尤为重要。此外, Mn3O4作为一种价格低廉、无毒的环保型催化剂, 在甲烷、一氧化碳的氧化及硝基苯的选择性还原方面表现出优异的催化性能[13]。因此, 研究Mn3O4纳米微球对AP热分解性质的影响, 不但可以拓宽Mn3O4纳米粒子的应用领域, 还有可能为寻找高能物质的新型催化剂提供借鉴。
2 实验部分 2.1 试剂与仪器试剂:乙醇, 分析纯, 成都市科龙化工试剂厂; 四水合乙酸锰, 分析纯, 成都市联合化工试剂研究所; 高氯酸铵, 分析纯, 中国国药集团; 商用微米级Mn3O4粉体, 分析纯, 阿拉丁。
仪器:高压反应釜(80 mL), 无锡金洪惠石化节能设备科技有限公司; 智能控温仪及加热设备, 上海博讯实业有限公司; 集热式磁力加热搅拌器, 金坛市医疗仪器; X′Pert PRO型多晶X射线衍射仪(XRD), 荷兰PANalytical公司; Ultra 55场发射扫描电子显微镜(FESEM), 德国Carl Zeiss光学仪器有限公司; Libra 200FE透射电子显微镜(TEM), 德国Carl Zeiss光学仪器有限公司; SDT Q600同步热分析仪, 美国TA仪器公司。
2.2 Mn3O4微球的制备室温下, 200 mL烧杯中加入50 mL无水乙醇, 四水合乙酸锰(13 mmol·L-1), 将得到的混合液搅拌30 min, 使其充分溶解后, 封装于高压反应釜中, 加热, 待反应一段时间后, 自然冷却至室温。然后将所得沉淀高速离心分离, 并用蒸馏水和乙醇洗涤, 真空干燥得到褐红色粉末, 即Mn3O4微球。
2.3 催化性能测试利用溶剂蒸发法制备Mn3O4/AP样品, 过程:将Mn3O4样品与AP按质量比为1:100, 3:100和5:100在超声波作用下均匀分散在乙醇和水的混合溶液(体积比为1:2)中, 在80 ℃的条件下加热搅拌, 使溶剂挥发。然后, 干燥、取样进行热分析实验。采用SDT Q600型综合热分析仪(DSC-TG)进行热分解试验, 测试条件:试样重2 mg左右, 升温速率20 ℃·min-1, 气氛为流动的Ar, 流量100 mL·min-1, 标样, α-Al2O3, 氧化铝加盖坩埚。
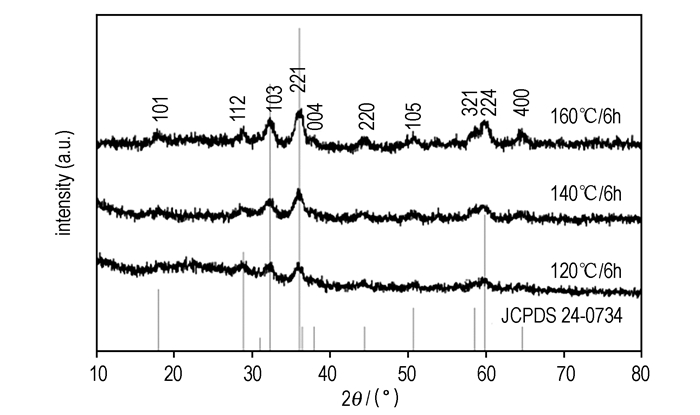
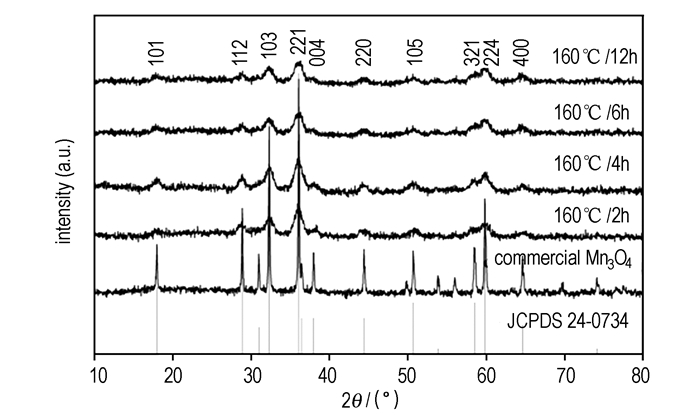
3 结果与讨论 3.1 XRD图谱分析对不同反应温度及不同反应时间下制备的Mn3O4微球样品进行了XRD分析, 结果分别如图 1和图 2所示。由图 1可知, 样品的结晶度随着反应温度的升高而变好。特别是160 ℃下反应6 h制备的Mn3O4微球样品, 其衍射峰与黑锰矿的标准XRD卡片(JPCDS Card NO. 24-0734)一致, 并且没有发现其它氧化锰的衍射峰, 说明该方法能制备纯度较高的Mn3O4微球。同时, 该衍射峰对称、尖锐、矮小, 说明产物是具有较高结晶度的Mn3O4纳米粒子。由Scherrer公式计算得到其晶粒尺寸为4~10 nm。在图 2中, 反应时间为2 h, 产物的XRD衍射峰较弱, 表明其结晶度不好。随着反应时间的延长, XRD衍射峰增强, 表明晶型发展的愈加完善, 晶粒逐渐长大, 如反应时间为4 h时,产物的XRD衍射峰与6 h下制备的样品几乎一致,且晶粒尺寸也介于4~10 nm之间,但超过4 h后, 产物的XRD衍射峰强度增加不明显。因此, 从节能角度考虑, 适宜的反应时间为4 h。此外, 对比样品与商用的Mn3O4的XRD图可推断出, 制备的Mn3O4微球的晶粒尺寸较商用的小。
|
图 1 不同温度下制备的Mn3O4微球XRD图谱 Fig.1 XRD patterns of Mn3O4 microspheres prepared at different heating temperature |
|
图 2 不同时间下制备的Mn3O4微球XRD图谱 Fig.2 XRD patterns of Mn3O4 microspheres prepared at different heating time |
为了对比制备的Mn3O4微球和商用的Mn3O4粉体的形貌, 进行了场发射扫描电子显微镜(FESEM)分析, 结果见图 3。由图 3可知, 商用的Mn3O4粉体没有规则的形貌(图 3b), 而由四水合乙酸锰制备的Mn3O4是分散性较好的微球, 直径介于几百纳米到微米之间, 且表面较为均匀。由图 3a的箭头处还可看出, Mn3O4微球的表面上附着超细的Mn3O4纳米粒子(几个纳米), 由此可推断出, 超细Mn3O4纳米粒子由于本身的不稳定性, 在高温高压的环境下, 易于聚集形成Mn3O4微球。

|
图 3 制备的Mn3O4微球及商品源Mn3O4粉体的FESEM照片 Fig.3 FESEM images of obtained Mn3O4 and commercial Mn3O4 powder |
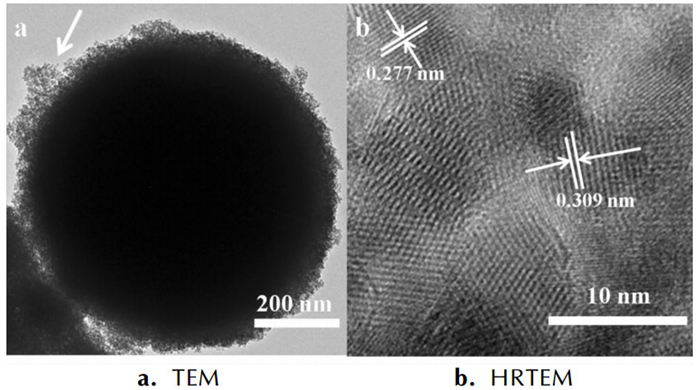
图 4为制备的Mn3O4微球的透射电子显微镜(TEM)照片。图 4a为单个Mn3O4微球的低分辨率透射图片, 由此可以看出, Mn3O4微球的周围包裹着一层超细Mn3O4纳米粒子。说明Mn3O4微球的形成不是一步合成, 而是由无数超细纳米粒子聚集形成。为了进一步解释超细纳米粒子的形成机理, 对图 4a箭头处进行高分辨率透射扫描(HRTEM)分析, 结果如图 4b所示。照片显示出超细Mn3O4纳米粒子的直径在10 nm左右, 这与用Scherrer公式计算在160 ℃、6 h下制备的Mn3O4纳米粒子的数值一致, 说明该实验方法能制备超细的Mn3O4纳米粒子。同时, 图 4b还表明超细Mn3O4纳米粒子是沿着不同方向生长的, 如图中的0.277 nm和0.309 nm晶格间距分别与黑锰矿Mn3O4的标准卡片(JPCDS Card NO. 24-0734)中(101)和(103)面一致, 表明制备出的Mn3O4微球应该是多晶体。
|
图 4 样品的TEM和HRTEM照片 Fig.4 TEM and HRTEM images of Mn3O4 obtained |
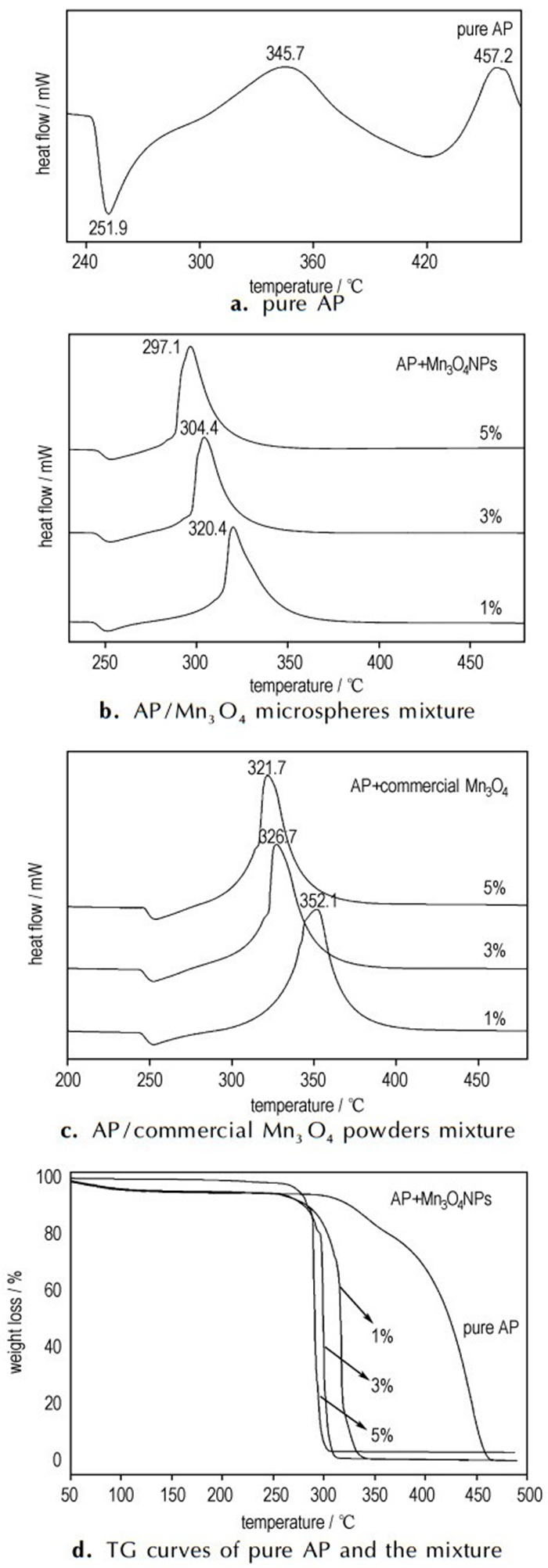
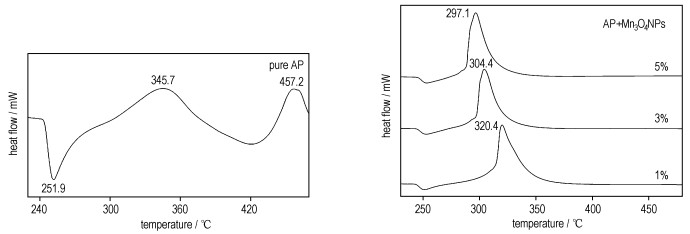
为了研究制备的Mn3O4微球对AP热分解性质的影响, 分别测试了纯AP, Mn3O4微球与AP不同质量比(1%, 3%和5%)的混合物, 以及商用Mn3O4与AP不同质量比的混合物的热分解性能, 得到DSC-TG曲线, 见图 5。曲线5a可知:纯AP的热分解可分为3个过程: 251.9 ℃是晶型转变的吸热峰, AP由斜方晶系转变为立方晶系。345.7 ℃是AP的低温分解峰, AP部分分解并生成中间产物。而457.2℃则是AP的高温分解峰, AP完全分解为挥发性产物。这与文献相符[14]。图 5b为不同含量Mn3O4微球对AP热分解过程的影响。由图 5b可知, 合成的Mn3O4微球对AP的晶型转变过程没有影响, 但对AP的放热分解过程影响显著, 使AP的热分解峰的位置明显提前。当Mn3O4微球与AP质量比为1%时, 就能将AP的热分解峰提前到320.4 ℃, 当质量比增加到5%时, AP的热分解峰提前到297.1℃。图 5c是商用Mn3O4粉体催化AP的热分解曲线, 其催化效果明显弱于制备的Mn3O4微球。为了进一步解释制备的Mn3O4微球的催化效应, 对Mn3O4与AP不同质量比的混合物和纯AP做了TG分析, 结果如图 5d。结果显示随着Mn3O4微球与AP质量比的增加, 反应失重温度提前, 这与图 5b的DSC曲线相符。
|
图 5 AP的热分解曲线及其与Mn3O4微球混合物的失重曲线 Fig.5 AP thermal decomposition curves of different samples |
上述结果表明, 在AP中加入Mn3O4微球后, AP只存在一个放热分解峰, 且分解峰的位置随着Mn3O4微球含量的增加而提前。这表明随着Mn3O4微球含量的增加, AP的分解在较低的温度下即可进行, 分解更容易。通过研究Mn3O4微球对AP热分解的催化性能, 其可能的催化机理为: (1)过渡态金属氧化物在电子转移过程中的桥梁催化作用。(2)纳米粉体的表面效应。AP低温热分解的速度控制步骤是电子从ClO4-向NH4+的转移过程[15]。Mn3O4微球为过渡态金属氧化物, 其在电子转移过程中能起到桥梁作用, 如方程(1)所示, 低价态氧化物价带通过接受ClO4-中转移的电子, 实现空穴的湮没, 进而催化AP的低温分解。AP的高温分解阶段, 大部分分解反应为气相反应, 而Mn3O4微球是由超细的纳米粒子聚集而成, 形成大量的活性位点, 极易吸附气相反应物分子, 这有助于它们之间的化学反应和反应放热, 促进AP高温热分解的进行。
| $ {\left[{\rm{e}} \right]^ + } + {\rm{ClO}}_4^ - \to {{\rm{O}}_{{\rm{oxide}}}} + {\rm{ClO}}_3^ - \to \frac{1}{2}{{\rm{O}}_2} + {\rm{ClO}}_3^ - + {\rm{e}} $ | (1) |
(1) 以四水合乙酸锰为锰源, 无水乙醇做溶剂, 通过溶剂热法成功制备了分散性和结晶度均较好, 纯度较高的Mn3O4微球。适宜的反应温度为160 ℃, 时间为4 h。
(2) 制备的Mn3O4微球对AP的催化效果明显优于商用的Mn3O4粉体, 能使AP的热分解峰提前到297.1 ℃。因此, 制备的Mn3O4微球有望在AP基的复合固体推进剂中得到应用。
| [1] |
AN Gui-min, YU Ping, XIAO Mei-jun, et al. Low-temperature synthesis of Mn3O4 nanoparticles loaded on multi-walled carbon nanotubes and their application in electrochemical capacitors[J].
Nanotechnology, 2008, 19(27): 275709 DOI:10.1088/0957-4484/19/27/275709 |
| [2] |
Seo W S, Jo H H, Prof K L, et al. Size-dependent magnetic properties of colloidal Mn3O4 and MnO nanoparticles[J].
Angew Chem Int Ed, 2004, 43(9): 1115-1117. DOI:10.1002/(ISSN)1521-3773 |
| [3] |
Stobbe E R, Boer B A, GEUS J W. The reduction and oxidation behaviour of manganese oxides[J].
Catal Today, 1999, 47(1-4): 161-167. DOI:10.1016/S0920-5861(98)00296-X |
| [4] |
Dubal D P, Holze R. High capacity rechargeable battery electrode based on mesoporous stacked Mn3O4 nanosheets[J].
RSC Advances, 2012, 2(32): 12096-12100. DOI:10.1039/c2ra21806b |
| [5] |
DU Jin, GAO Yong-qian, CHAI Lan-lan, et al. Hausmannite Mn3O4 nanorods: synthesis, characterization and magnetic properties[J].
Nanotechnology, 2006, 17(19): 4923-4928. DOI:10.1088/0957-4484/17/19/024 |
| [6] |
LI Na, GENG Zheng-feng, CAO Min-hua, et al. Well-dispersed ultrafine Mn3O4 nanoparticles on graphene as a promising catalyst for the thermal decomposition of ammonium perchlorate[J].
Carbon, 2013, 54: 124-132. DOI:10.1016/j.carbon.2012.11.009 |
| [7] |
Shusser M, Culock F E, Cohen N S. Combustion response of ammonium perchlorate composite propellants[J].
Propul Power, 2002, 18(5): 1093-1100. DOI:10.2514/2.6039 |
| [8] |
Jacobs P W M, Whitehead H M. Decomposition and combustion of ammonium perchlorate[J].
Chem Rev, 1969, 69(4): 551-590. DOI:10.1021/cr60260a005 |
| [9] |
FU Ting-ming, LIU Fei-quan, LIU Lin, et al. Catalytic thermal decomposition of ammonium perchlorate using manganese oxide octahedral molecular (OMS)[J].
Catalysis Communications, 2006, 10(1): 108-112. |
| [10] |
CHEN Li-juan, LI Li-ping, LI Guang-she. Synthesis of CuO nanorods and their catalytic activity in the thermal decomposition of ammonium perchlorate[J].
Journal of Alloys and Compounds, 2008, 464(1): 532-536. |
| [11] |
LU Shan-shan, JING Xiao-yan, LIU Jing-yuan, et al. Synthesis of porous sheet-like Co3O4 microstructure by precipitation method and its potential applications in the thermal decomposition of ammonium perchlorate[J].
Journal of Solid State Chemistry, 2013, 197: 345-351. DOI:10.1016/j.jssc.2012.09.020 |
| [12] |
WANG Yan-ping, ZHU Jun-wu, YANG Xu-jie, et al. Preparation of NiO nanoparticles and their catalytic activity in the thermal decomposition of ammonium perchlorate[J].
Thermochimica Acta, 2005, 437(1): 106-109. |
| [13] |
Ahmad T, Ramanujchary K V, Lofland S E, et al. Nanorods of manganese oxalate: a single source precursor to different manganese oxide nanoparticles (MnO, Mn2O3, Mn3O4)[J].
Journal of Materials Chemistry, 2004, 14(23): 3406-3410. DOI:10.1039/b409010a |
| [14] |
Fitzgerald R P, Brewster M Q. Flame and surface structure of laminate propellants with coarse and fine ammonium perchlorate[J].
Combust Flame, 2004, 136(3): 313-326. DOI:10.1016/j.combustflame.2003.10.008 |
| [15] |
LI Na, CAO Min-hua, WU Qing-yin, et al. A facile one-step method to produce Ni/graphene nanocomposites and their application to the thermal decomposition of ammonium perchlorate[J].
Cryst Eng Comm, 2012, 14(2): 428-434. DOI:10.1039/C1CE05858D |
Mn3O4 microspheres were successfully prepared. The composition and morphology of Mn3O4 microspheres were characterized by XRD, FESEM and TEM. The effects of Mn3O4 microspheres on the thermal decomposition properties of AP were investigated by DSC.




