四硝基甘脲(TNGU)属于咪唑类炸药[1], 由我国炸药合成专家彭忠吉等[2]于1965年首次合成, 它具有密度高热稳定性好等特点, 其结晶密度高达2.04 g·cm-3, 可作为高能炸药、推进剂和烟火药的高能组分, 传爆药的装药[3], 以及其它高能炸药的合成中间体。有关TNGU研究的文献较少, 文献[2]报道的合成方法是以甘脲为原料, 在浓硝酸/醋酸酐(15:7.5, V/V)体系下, 3~5 ℃硝化8 h。此法反应时间长, 产生废酸量大, 且工艺重现性欠佳。Jacque Boileau等[4-5]以二硝基甘脲为原料, 采用含有N2O5(5%~50%)的发烟硝酸为硝化剂在0~10 ℃硝化制得TNGU, 但产品纯度较低。为此, 本研究在文献[2]的基础上, 研究了TNGU的合成工艺, 通过将硝化温度提高到30 ℃, 强化了硝化反应, 缩短了硝化时间, 减少了硝化剂用量、废酸液量, 提高了产品收率, 达到了工艺重现性好的目的。
2 实验部分 2.1 试剂与仪器实验药品及试剂:尿素; 乙二醛, 40%;盐酸, 37%;发烟硝酸, 98%;醋酸酐; 乙醇, 95%;二氯甲烷; 乙酸乙酯; 石油醚60~90 ℃。国药集团化学试剂有限公司。
实验仪器:北京祥鹄科技XH-100A微波合成萃取仪; 北京泰克仪器X-4显微镜熔点测定仪; 上海沪铄电子科技有限公司ZF-7三用紫外分析仪; 天津港东科技发展股份有限公司FTIR7600红外光谱仪; 瑞士Bruker DRX300 MHZ, Bruker 400 MHZ Advance Ⅲ超导核磁共振仪; 德国VARIO EL Ⅲ元素分析仪; 德国NETZSCH DSC204差示扫描量热仪。
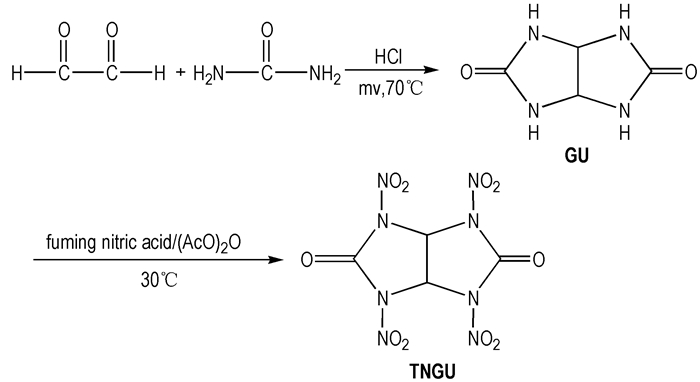
2.2 合成路线以尿素和乙二醛为原料, 微波加热, 盐酸催化下缩合成甘脲(GU), 再经发烟硝酸和醋酸酐硝化生成TNGU。合成路线见scheme 1。
|
Scheme1 Synthetic route of TNGU |
在装有回流冷凝管、温度计和磁力搅拌器的三口烧瓶中加入6.40 g (约0.105 mol)尿素及10 mL蒸馏水, 将烧瓶放入微波合成萃取仪中搅拌加热, 加热频率2450 Hz, 功率600 W; 70 ℃下加入7. 30 g (约0.05 mol)混有2滴浓盐酸的40%乙二醛7.30 g(约0.05 mol), 出现白色沉淀, 反应15 min后停止, 冷却至室温, 过滤, 用稀氢氧化钠洗涤再用蒸馏水洗涤至中性, 后用乙醇洗涤两三次, 晾干, 在120 ℃干燥5 h后得6.27 g白色粉末状固体, 收率88.2%, m.p.317.1 ℃(文献[6]300 ℃以上)。IR(KBr, ν/cm-1): 3208, 2842, 1691, 1128, 892, 737, 607, 其红外谱图与萨特勒标准红外谱图及文献[7]一致; 1 H NMR(DMSO-d6, 300 MHz), δ: 5.229 (S, 2H, CH), 7.139(S, 4H, NH); Anal. calcd for C4H6N4O2: C 33.81, H 4.26, N 39.42; found C 33.58, H 4.37, N 39.52。
2.3.2 TNGU的合成在冰水浴下, 于带有搅拌及冷凝管的四口烧瓶中加入70 mL发烟硝酸, 快速搅拌下分批加入5.0 g(0.035 mol)GU, 滴加35 mL醋酸酐, 调节滴加速度以保持烧瓶内温度15~25 ℃。滴加完毕, 继续搅拌5~10 min, 升温至30 ℃反应4 h。冷却至室温, 过滤, 蒸馏水洗至中性, 后依次用乙醇、二氯甲烷(体积比1:4)、二氯甲烷洗涤。真空干燥得产品, 用丙酮-石油醚重结晶, 干燥得6.26 g白色粉末状固体, 收率84.5%。IR(KBr, ν/cm-1): 3000, 1810, 1610, 1265, 900, 781, 688, 其红外谱图与文献[2]红外谱图基本一致; 1H NMR(Acetone-d6, 400 MHz), δ: 7.784(S, 2H, CH); 13C NMR(Acetone-d6, 400 MHz), δ: 205.544(—C=O) 65.044(—CH); Anal. calcd for C4H2N8O10: C 14.92, H 0.63, N 34.79; found C 14.59, H 0.87, N 34.98。
2.2.3 TNGU的DSC测定样品量约1 mg, N2流速50 mL·min-1, 样品盘采用带盖的铝坩埚, 温度50~300 ℃, 升温速率2, 5, 10, 20 ℃·min-1。
3 结果与讨论 3.1 不同因素对硝化反应的影响 3.1.1 温度对TNGU收率的影响取发烟硝酸90 mL, 控制水浴温度在0~35 ℃, 反应4 h。考察反应温度对反应的影响, 其结果见表 1。
| 表 1 温度对TNGU收率的影响 Tab.1 Effects of the reaction temperatures on yield of TNGU |
由表 1可见, 随着反应温度的升高, 产品收率提高。这是由于硝基是吸电子基, 低温下氮原子上的氢一旦被硝基取代, 其它未被取代氮原子上的氢就不易被硝化, 所以, 升高温度有利于硝化反应。但考虑到当反应温度超过30 ℃, 发烟硝酸挥发冒烟严重, 增加了反应的不安全因素, 且产品收率增加缓慢。所以, 反应温度宜控制在25~30 ℃, 此时收率约为84%。
3.2.2 时间对TNGU收率的影响取发烟硝酸90 mL, 控制水浴温度在25 ℃。在此温度下反应3~12 h。考察反应时间对反应的影响, 其结果见表 2。
| 表 2 时间对TNGU收率的影响 Tab.2 Effects of the reaction times on nitration reaction |
由表 2可见, 随着反应时间的延长, 产品收率逐渐提高, 当反应时间为5 h时产品收率最高为84.3%。由于反应时间从4 h延长至5 h时, 产品收率增加很少, 而且超过5 h后产品收率有下降的倾向, 这可能是由于部分产品发生了水解或分解。所以, 反应时间控制在4 h左右。由表 1和表 2可知, 提高硝化温度, 可大大提高硝化反应效率及产品收率, 缩短硝化时间, 比文献[2]报道反应8 h缩短了4 h。
3.1.3 硝酸用量对TNGU收率的影响取发烟硝酸60~90 mL, 醋酸体积为30~45 mL, 控制水浴温度在25 ℃。在此温度下反应4 h。考察发烟硝酸用量对反应的影响, 其结果见表 3。
| 表 3 硝酸用量对TNGU收率的影响 Tab.3 Effects of nitric acid dosages on nitration reaction |
由表 3可知, 发烟硝酸的用量在实验范围内对产品收率影响不大, 收率约为84%。增加发烟硝酸用量势必增加了废酸液的量; 发烟硝酸用量少, 产品后续处理发粘; 综合考虑, 发烟硝酸用量控制在70 mL左右, 此时, 废酸液比文献[2]减少30 mL。
3.1.4 醋酸酐用量等其它条件对TNGU收率的影响在硝化反应中除了上述因素对反应有影响外, 还存在着其它影响因素, 比如醋酸酐用量及其滴加速度, 开启加热的时间等。在上述其它反应条件不变时, 通过改变醋酸酐用量, 分别取发烟硝酸体积的1、1/2及1/3体积时, 考察醋酸酐用量对硝化反应的影响, 其结果见表 4。
| 表 4 醋酸酐用量对TNGU收率的影响 Tab.4 Effects of acetic anhydride dosages on nitration reaction |
在硝酸-醋酸酐体系中, 醋酸酐的比例不宜过低, 否则, 脱水效果不好; 但也不宜过高, 醋酸酐体积过大硝酸浓度相对较低, 硝化能力不够, 由表 4可知, 硝酸和醋酸酐的体积比为2:1时对反应有利, 即醋酸酐为35 mL, 此时, 硝化反应属于“和缓的”硝化反应[8], 产品收率较高为84.3%。
当上述其它反应条件不变, 改变醋酐滴加速度, 考察其对硝化反应的影响, 其结果见表 5。
| 表 5 醋酸酐滴加速度对硝化反应的影响 Tab.5 Effects of acetic anhydride dropping speed on nitration reaction |
由于醋酐滴加速度的快慢直接影响着反应液的温度, 滴加速度越快, 反应液温度上升越快; 滴加速度越慢, 反应液温度上升越慢, 从表 5可知, 醋酸酐滴加速度太快或太慢都不好, 滴加太慢反应温度太低, 不利于多硝胺基的生成, 大部分生成了溶解性不好的二硝基甘脲, 导致产品收率降低; 滴加速度加快反应液温度升高快, 有利于多销胺基的生成, 但当滴加速度超过2 mL·min-1时, 反应液冒出许多黄色硝烟, 增加了实验的不安全性, 且瞬间反应液温度上升过高, 氧化反应严重, 得到了灰色的粗产品, 降低产品收率。综合考虑, 醋酸酐滴加速度控制在1~1.5 mL·min-1, 确保反应液温度15~25 ℃, 此时产品收率大于84%。
此外, 开启加热的时间主要以反应液温度为准, 最好在反应液温度未下降到15 ℃以下及时开启加热, 并在整个硝化反应过程中控制好温度。
可见, 优化工艺条件为: GU 5g, 发烟硝酸70 mL, 醋酸酐35 mL, 硝化温度30 ℃, 硝化时间4 h, 醋酐滴加速度为1.5 mL·min-1, 平行3次实验结果, TNGU收率平均为84.5%。此工艺较文献[2]的废酸液量减少30 mL, 硝化时间缩短4 h。
3.2 产品热分析不同升温速率下TNGU的DSC曲线如图 1所示。

|
图 1 不同升温速率下TNGU的DSC曲线 Fig.1 DSCcurves of TNGU at different heating rates |
由图 1可知, TNGU不经过熔化直接放热分解, 当升温速率为20 K·min-1时, 从164.7 ℃开始分解并伴随放热, 经过外推起始温度216.6 ℃快速分解, 直到到达峰值温度227.0 ℃, 放热量达到最大。给出个某升温速率下的结果, 分解温度较高, 是一种热稳定性良好的炸药。对于不同的升温速率β, 求得其对应的峰顶温度Tp, 利用Kissinger法[9]和Ozawa法[10]进行热动力学参数计算。计算结果如表 5所示, 两者计算结果非常接近。
Kissinger方程为
| $ {\rm{ln}}\left( {\frac{\mathit{\beta }}{{\mathit{T}_{\rm{P}}^2}}} \right){\rm{ = ln}}\left( {\frac{{{\mathit{A}_{\rm{K}}}\mathit{R}}}{{{\mathit{E}_{\rm{K}}}}}} \right){\rm{ - }}\frac{{{\mathit{E}_{\rm{K}}}}}{\mathit{R}}\frac{1}{\mathit{T}} $ | (1) |
式中, β为升温速率, K·min-1; AK为Kissinger计算的指前因子, s-1; EK为Kissinger计算的表观活化能, J·mol-1; R为理想气体常数, 8.314 J·mol-1·K-1; T为温度, K。
Ozawa方程为
| $ {\rm{lg}}\mathit{\beta }{\rm{ = lg}}\left( {\frac{{\mathit{A}{\mathit{E}_{\rm{O}}}}}{{\mathit{RG}\left( \mathit{\alpha } \right)}}} \right){\rm{ - 2}}{\rm{.315 - 0}}{\rm{.4567}}\frac{{{\mathit{E}_{\rm{O}}}}}{{\mathit{RT}}} $ | (2) |
式中, β, T, R同上; A为指前因子, s-1; EO为Ozawa计算的表观活化能, J·mol-1; G(α)为机理函数的积分形式。
| 表 6 由TNGU的DSC曲线得到的动力学参数 Tab.6 The kinetic parameters values from the DSC curves of TNGU |
根据DSC曲线, 由公式(3)和(4)可估算炸药的临界爆炸温度, 由公式(3)、(5)~(7)可获得炸药热分解活化熵变、活化函变及活化吉布斯自由能变化值[11-13]。
| $ {\mathit{T}_{{\rm{e}}\mathit{i}}}{\rm{ = }}{\mathit{T}_{{\rm{e0}}}}{\rm{ + }}{\mathit{a}_{\rm{1}}}{\mathit{\beta }_\mathit{i}}{\rm{ + }}{\mathit{a}_{\rm{2}}}\mathit{\beta }_\mathit{i}^2{\rm{ + }}{\mathit{a}_{\rm{3}}}\mathit{\beta }_\mathit{i}^3{\rm{ + }} \cdots {\rm{ + }}{\mathit{a}_{{\rm{n - 2}}}}\mathit{\beta }_\mathit{i}^{{\rm{n}} - 2}{\rm{, }}\;\mathit{i}{\rm{ = 1, 2, 3, }} \cdots \mathit{n}{\rm{}} $ | (3) |
式中, Te0, Tp0分别为β→0时的外推起始温度和外推峰值温度, K。由图 1中的Te和TP按公式(3)进行多项式拟合, 可得Te0=455.92 K, Tp0=471.56 K。
| $ {\mathit{T}_{\rm{b}}}{\rm{ = }}\frac{{{\mathit{E}_O}{\rm{ - }}\sqrt {\mathit{E}_\mathit{O}^2{\rm{4}}{\mathit{E}_\mathit{O}}\mathit{R}{\mathit{T}_{{\rm{e0}}}}} }}{{{\rm{2}}\mathit{R}}} $ | (4) |
式中,Tb为临界爆炸温度, K; EO为Ozawa计算的表观活化能,kJ·mol-1。
将Te0代入公式(4)中得, Tb=465.34 K。
| $ \mathit{A}{\rm{ = }}\frac{{{\mathit{k}_{\rm{B}}}\mathit{T}}}{\mathit{h}}{{\rm{e}}^{{\rm{\Delta }}\mathit{S} \ne/\mathit{R}}} $ | (5) |
| $ {\rm{\Delta }}\mathit{H}{\rm{ = }}\mathit{E}{\rm{ - }}\mathit{RT} $ | (6) |
| $ {\rm{\Delta }}{\mathit{G}^ \ne }{\rm{ = \Delta }}{\mathit{H}^ \ne }{\rm{ - }}\mathit{T}{\rm{\Delta }}{\mathit{S}^ \ne } $ | (7) |
式中, ΔS≠、ΔH≠和ΔG≠分别为T=TP0对应的热分解活化熵变、热分解活化热函和热分解活化吉布斯自由能变化。kB为玻尔兹曼常数, 1.3807×10-23J·K-1; h为普朗克常数, 6.6261×10-34 J·s。
将T=Tp0, E=198.92 kJ·mol-1, A=1025.09s-1代入(5)~(7)上式中, 可得出, ΔS≠=171.46 J·mol-1、ΔH≠=195.00 kJ·mol-1和ΔG≠=194.99 kJ·mol-1。表明TNGU的热分解为放热熵增反应。
4 结论(1) 以乙二醛与尿素为原料, 盐酸存在下, 经微波加热至70 ℃, 15 min合成了GU, 收率为88.2%。在发烟硝酸与醋酸的硝化体系下, GU经一步硝化制备了TNGU, 优化工艺条件为: GU 5 g, 发烟硝酸70 mL, 醋酸酐35 mL, 硝化温度30 ℃, 硝化时间4 h, 醋酐滴加速度为1.5 mL·min-1, TNGU收率为84.5%。提高硝化温度, 反应时间比文献[2]缩短4 h, 产生的废酸液量减少30 mL。
(2) 用DSC分析获得了TNGU在不同升温速率时的热分解曲线和峰温, 用Kissinger和Ozawa法计算获得了TNGU的表观活化能分别是198.92 kJ·mol-1和191.09 kJ·mol-1。
(3) 利用DSC曲线的外推起始温度和外推峰值温度分别估算了TNGU的临界爆炸温度为Tb=465.34 K, 外推温度下的ΔS≠、ΔH≠和ΔG≠分别为171.46 J·mol-1、195.00 kJ·mol-1和194.99 kJ·mol-1。TNGU的热分解为放热熵增反应。
| [1] |
曹端林, 王小军, 杨彩云, 等. 1-甲基-4, 5-二硝基咪唑合成工艺[J].
含能材料, 2009, 17(6): 678-680. CAO Duan-lin, WANG Xiao-jun, YANG Cai-yun, et al. Synthesis of 1-methyl-4, 5-dinitroimidazole[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(6): 678-680. |
| [2] |
彭忠吉, 万道正. 四硝基甘脲及其水解产物的合成研究[J].
兵工学报, 1980(3): 23-27. PENG Zhong-ji, WAN Dao-zheng. The synthetic study of tetranitroglycoluril and its hydrolyzed product[J]. Acta Armamentarii, 1980(3): 23-27. |
| [3] |
Jai Prakash Agrawal, Robert Dale Hodgson.
Organic Chemistry of Explosives[M]. New York: John Wiley Sons, Ltd, 2007: 277-288.
|
| [4] |
Boileau Jacques, Emeury Jean Marie L, Kehren Jean Paul. Teteranitroglycoluril, herstellungsverfahren dafuer und verwendung als explosivstoff: DEP 2435651[P], 1975.
|
| [5] |
Boileau Jacques, Emeury Jean Marie L, Kehren Jean Paul. Tetranitronglycoluril and method of preparation thereof: USP 4487938[P], 1984.
|
| [6] |
夏宇正, 焦书科. 甘脲的合成与鉴定[J].
北京化工学院学报(自然科学版), 1990, 17(3): 73-76. XIA Yu-zheng, JIAO Shu-ke. Synthesis and characterization of glycoluril[J]. Chinese Journal of Beijing Institute of Chemical Industry, 1990, 17(3): 73-76. |
| [7] |
王上文, 李来生, 刘超, 等. 甘脲用作气相色谱固定相的色谱性能研究[J].
分析实验室, 2008, 27(7): 18-22. WANG Shang-wen, LI Lai-sheng, LIU Chao, et al. Studies on chromatographic properties of glycocluril as a new type of gas chromatopraphic column packing material[J]. Chinese Journal of Analysis Laboratory, 2008, 27(7): 18-22. |
| [8] |
吕春绪.
硝酰阳离子理论[M]. 北京: 兵器工业出版社, 2006: 16-43.
LU Chun-xu. Theory of nitrylcation[M]. Beijing: Arms industry publishment, 2006: 16-43. |
| [9] |
Homer E. Kissinger. Reaction kinetics in differential thermal analysis[J].
Analytical Chemistry, 1959, 29(11): 1702-1706. |
| [10] |
Takeo Ozawa. A new method of analyzing thermogravimatrie data[J].
Bulletin of Chemical Society of Japan, 1965, 38(11): 1881-1886. DOI:10.1246/bcsj.38.1881 |
| [11] |
HU Rong-zu, GAO Hong-xu, ZHAO Feng-qi, et al. Theory and numerical method of calculating the kinetic parameters of exothermic decomposition reaction of energetic materials from peak temperature of DSC curves at constant heating rates[J].
Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(6): 643-649. |
| [12] |
ZHANG Tong-lai, HU Rong-zu, XIE Yi, et al. The estimation of critical temperatures of thermal explosion for energetic materials using non-isothermal DSC[J].
Thermochim Acta, 1994, 244: 171-176. DOI:10.1016/0040-6031(94)80216-5 |
| [13] |
GAO Hong-xu, ZHAO Feng-qi, HU Rong-zu, et al. Estimation of the kinetic parameters of thermal decomposition reaction and thermal safety on hexanitrohexaazaisowurtzitane[J].
Chinese Journal of Explosives & Propellants, 2013, 36(5): 41-48. |
Glycocluril (GU) was prepared in the presence of hydrochloric acid by microwave heating with urea and glyoxal as raw materials. Through fuming nitric acid and acetic anhydride, tetranitroglycoluril (TNGU) was synthesized from nitration of GU. Thermal analysis of TNGU was studied by DSC.



