铝粉作为金属燃料, 具有相对高的体积燃烧焓和较高的能量密度, 广泛应用于推进剂、炸药和烟火药等领域[1-2]。然而, 使用铝粉还有一些问题亟待解决, 如燃烧不完全、燃烧速率低和点火温度高等[3-4], 这些缺陷限制了铝粉的进一步应用。因此, 为了解决铝粉应用中遇到的问题, 可以往铝中添加活性易燃的金属, 形成合金, 改善铝粉的性能。研究人员一般通过机械合金化法(Mechanical alloying, MA)往铝中添加第二种元素, 制备铝基二元合金, 达到改善铝粉活性的目的。目前, 国内外研究较多的铝基二元合金燃料有Al-Mg、Al-Ti、Al-Li等[5-6]。
Dreizin E L等[7-8]使用MA法制备了Mg含量为10%~50%的5种Al-Mg粉末, 并对其进行了点火和氧化行为分析。研究发现, Al-Mg粉末的点火温度在950~1060K范围变化, 明显低于铝的点火温度; Al-Mg合金粉具有两次明显不同的氧化过程, 分别发生在550~660 ℃和900~1200 ℃, 这些放热的氧化过程对改善合金粉的点火和燃烧性能起着至关重要的作用, 不过当Mg含量低于30%时, 氧化反应并不完全, Mg含量为30%的合金在1300 ℃时增重也只有72%左右。王毅等人[9]同样使用MA法制备了纳米级的Mg含量20%的Al-Mg合金粉, 该合金在Al熔点前就能发生氧化反应, 但在1100 ℃时增重也只有69.13%。Zhu X等人[10-11]也对MA法制备的Al-Ti合金粉的点火和氧化过程进行了分析, 发现该合金粉点火温度显著降低是由于Al-Ti合金中亚稳的L12相的放热转变引起的, 同时观察到了三个氧化放热峰, 并发现球磨过程引入了杂质碳元素。总体来说, 铝基二元合金粉的活性还是优于纯铝。但是采用MA法制备铝基合金粉时容易引入杂质, 污染合金, 导致产物纯度的降低, 并且该法制备的铝基二元合金粉大多进行多次氧化放热反应, 使得能量释放较为分散, 不能集中放热。另外, 在含能材料领域, 对于铝基三元合金燃料的研究还未见有报道。
由于Zr具有高的放热活性和能量密度, 同时在应用时还可以增加固体载荷和提高体系的体积比冲, 故本研究设计了一种新型金属燃料, 将Zr加入到Al-Mg合金中, 通过一种新的制备方法—紧耦合气雾化法(Close-coupled gas atomization, CCGA)制备了不同质量分数的Al-Mg-Zr三元合金燃料, 并对它们的热反应性能以及氧化机制进行了分析。以期为研制可用于火炸药领域的高活性合金燃料的可能性提供参考。
2 实验部分 2.1 试剂与仪器纯铝锭、纯镁锭和Al-Zr中间合金, 徐州华中铝业有限公司; 氢氟酸, 分析纯, 国药集团化学试剂有限公司; 环氧树脂, 分析纯, 国药集团化学试剂有限公司。
紧耦合气雾化设备, 英国Phoenix Scientific Industries Ltd (PSI)公司; X’Pert PRO型多功能X射线衍射仪(XRD), 荷兰帕纳科公司; Diamond TG/DTA同步热分析仪, 铂金-埃尔默仪器有限公司; 带有X射线能谱(EDS)的Sirion 200扫描电子显微镜(SEM), 荷兰FEI公司; 325目试样筛, 浙江上虞市纱筛厂; Ecomet300/Automet300自动研磨抛光机, 美国标乐有限公司。
2.2 实验过程 2.2.1 Al-Mg-Zr合金粉的制备纯Al、纯Mg和Al-Zr中间合金用作原料制备Al98-xMgxZr2 (x=5, 10, 15, 20, 25, 30)合金粉末。将各成分按照相应的质量比率投入到CCGA设备的坩埚中, 然后将设备抽真空至10-2 Pa时充入保护气体氩气。通过高频感应加热炉升温至900 ℃左右, 待Al-Mg-Zr母合金熔化均匀后, 开始雾化。纯氩用作雾化气体, 实验压强为3.5 MPa, 雾化时间为90 s。待粉末冷却后收集, 并将各合金粉末过325目筛。本研究对象为粒径小于45 μm的粉末。
2.2.2 合金粉的测试及表征将过325目筛的粉末进行XRD和SEM/EDS表征分析。使用TG/DTA同步热分析仪测试粉末的热反应特性, 测试条件为:常温~1300 ℃, 氧气气氛, 气体流速为20 mL·min-1, 加热速率为20 ℃·min-1, 试样质量为2 mg左右。粉末在一定温度下氧化后产物的形貌和物相分别通过SEM和XRD表征, 部分粉末经过环氧树脂固化、抛光和酸腐蚀后观察其截面形貌。
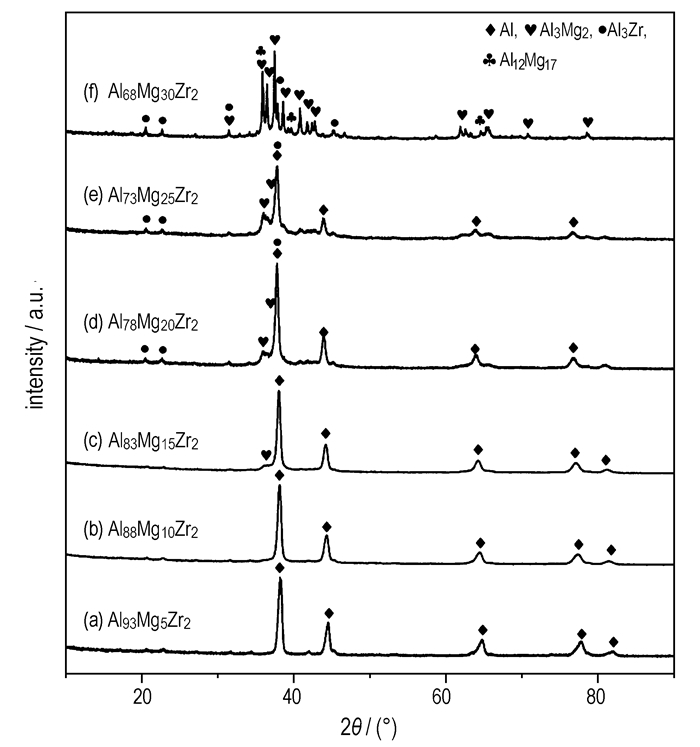
3 结果与讨论 3.1 Al-Mg-Zr粉末XRD分析气雾化制备的不同质量分数的Al-Mg-Zr合金的XRD如图 1所示。从图 1中可以看出, 对于Mg含量为5%和10%的粉末来说, 只观察到了Al峰的出现。当Mg含量增加到15%时, 开始出现Al3Mg2相, 并且当Mg含量增加到30%时, 该相依然存在。当Mg含量继续增加时, Al3Mg2的衍射峰逐渐增强, 而Al的衍射峰逐渐减弱。当Mg含量为20%时, 出现了Al3Zr相。Ichikawa和Babkin[12-13]研究认为, 在Al-Zr合金中, 即使Al含量增加一小部分, Zr的溶解度都会发生明显的减少, 并且与Mg相互平衡的必是Al3Zr, 故在Al-Mg-Zr合金中, 随着Mg含量的增加, Al含量减少, 则Al3Zr的衍射峰逐渐增强。对于Al78Mg20Zr2和Al73Mg25Zr2合金来说, 平衡相基本一样, 都是Al, Al3Mg2和Al3Zr, 两者之间唯一的区别在于对应物相的峰强度不一样。对于Al68Mg30Zr2粉末, 其物相组成出现了明显变化, 单质Al峰消失了, 开始出现Al12Mg17, 这与前人的研究结果是一致[12]的, 其余相为Al3Mg2和Al3Zr。
|
图 1 不同组分Al-Mg-Zr合金粉的XRD图 Fig.1 XRD patterns of Al-Mg-Zr alloy powder with different compositions |
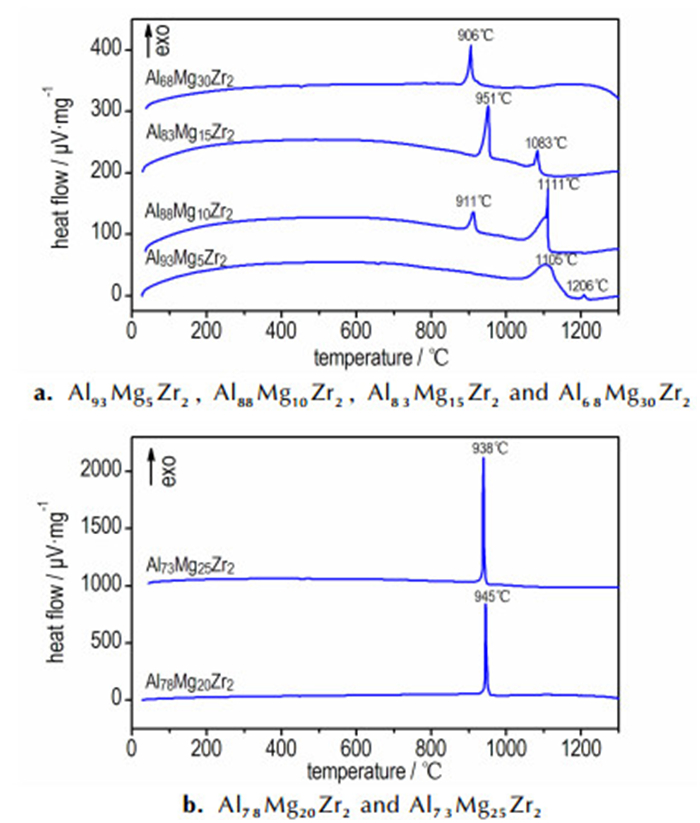
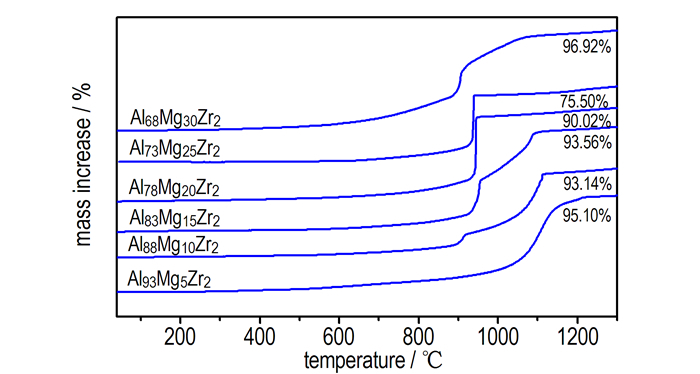
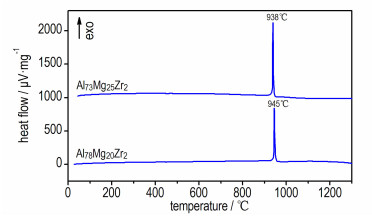
Al98-xMgxZr2 (x=5, 10, 15, 20, 25, 30)合金粉在氧气气氛下的DTA和TG热分析曲线分别如图 2和图 3所示。从中可以看出, 合金粉随着Mg含量的变化, 其DTA-TG曲线发生显著改变。Al93Mg5Zr2、Al88Mg10Zr2和Al83Mg15Zr2粉末共同的特点是有两个氧化放热峰, 而Al78Mg20Zr2、Al73Mg25Zr2和Al68Mg30Zr2则是单峰集中热释放, 且都有因Al熔化或Al-Mg共晶熔化导致的吸热峰出现, 不过有的合金因为放热峰太强的缘故显示得并不清楚。
|
图 2 不同组分Al-Mg-Zr合金粉的DTA曲线 Fig.2 DTA curves of Al-Mg-Zr alloy powder with different compositions |
|
图 3 不同组分Al-Mg-Zr合金粉的TG曲线 Fig.3 TG curves of Al-Mg-Zr alloy powder with different compositions |
图 2a中Al93Mg5Zr2粉末的第一个放热峰出现在一个比较宽的温度范围(1046~1162℃), 远超过Al的熔点, 这是由于表面氧化层破裂后Al氧化引起的。发生在1206 ℃的第二个放热峰峰明显弱于第一个氧化峰, 但峰型较尖锐, 应该与剩余的Al氧化有关。从TG曲线可看出, Al93Mg5Zr2粉末在1000 ℃后开始出现明显增重, 由于该合金粉的Mg含量太少, 其氧化过程类似同粒径的微米铝粉。Al88Mg10Zr2粉末在911 ℃发生第一次明显的氧化反应, 而在1111 ℃发生的第二次氧化则更为剧烈。Al83Mg15Zr2粉末的放热峰强弱趋势正好与Al88Mg10Zr2粉末相反, 其发生在951℃的第一次氧化反应比发生在1083 ℃的第二次氧化反应更加剧烈, 表现为第一个放热峰更强, 峰型更加尖锐, 第一次氧化增重曲线斜率更大。Al93Mg5Zr2、Al88Mg10Zr2和Al83Mg15Zr2都进行了两步氧化, 不同的是发生氧化反应的温度逐渐降低, 且第一次氧化反应比第二次更剧烈, 主要原因是Mg含量的增加使得易燃的Al3Mg2相和Mg蒸气增加, 从而使氧化更容易。
当粉末中Mg含量达到一定值时, 颗粒中Al3Mg2和Al3Zr的含量也发生改变, 从而使得粉末氧化行为发生显著变化, 这主要反映在Al78Mg20Zr2和Al73Mg25Zr2粉末的剧烈集中氧化现象中, 如图 2(b)所示。Al78Mg20Zr2和Al73Mg25Zr2粉末分别在945 ℃和938 ℃单峰集中热释放, 且峰型异常尖锐。这两组粉末在对应温度发生氧化时, TG曲线(图 3)几乎是垂直上升的变化, 可见反应之剧烈, 且从TG曲线变化可知反应基本完全。对于Al68Mg30Zr2粉末, 在906 ℃发生单峰集中氧化, 但是峰强显著弱于Al78Mg20Zr2和Al73Mg25Zr2粉末, 由于该合金粉中并没有单质Al相, 且因Mg的能量密度远低于Al, 故其能量释放量将低于其他合金粉末。
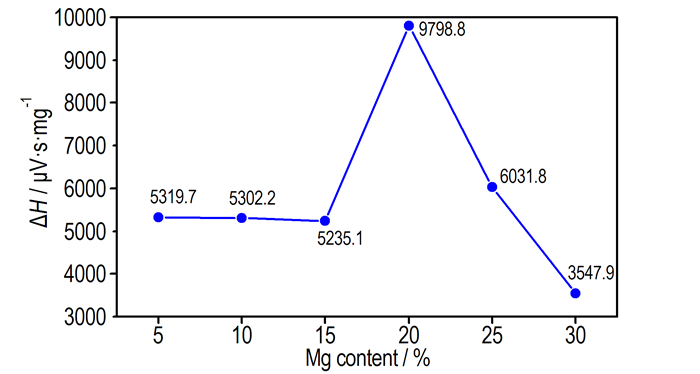
用DTA曲线中的放热峰面积[14]来衡量粉末的氧化放热焓ΔH, 其单位为μV·s·mg-1。从图 2的DTA曲线中获得各合金粉的氧化放热焓数据, 作出Al-Mg-Zr合金粉能量释放量随Mg含量的变化图, 见图 4所示。从图 2、图 3和图 4可以看出, 随着Mg含量的增加, 合金粉末发生氧化反应的温度逐渐降低, 且由多步氧化过程逐渐转变为一步氧化过程, 能量释放量先增后减。这与机械合金化法制备的Al-Mg[15]和Al-Ti[11]合金的氧化过程具有明显不同。除了粉末粒径的影响以外, 还可能是由于制备方法和相组成的差异引起的氧化行为不同。因为机械合金化制备的合金粉包含有亚稳的合金相, 而气雾化法制备的合金粉则是晶态的金属间化合物; 从物相组成上来说, 最大的区别是有无Al3Zr相。根据Al-Mg-Zr的相图可知, 在气雾化制备粉末的过程中, Al3Zr是第一个凝固成核的相, 然后熔融的Al和Al3Mg2开始凝固并包覆Al3Zr颗粒。因此, 形成了一个核壳包覆结构, 这将在粉末的SEM表征中得到证实。
|
图 4 Al-Mg-Zr合金粉能量释放量随着Mg含量的变化 Fig.4 Changes in the energy releasing amount of Al-Mg-Zr alloy powder with Mg content |
从图 4可知, 对于低Mg含量的Al93Mg5Zr2、Al88Mg10Zr2和Al83Mg15Zr2合金粉, 它们的能量释放量相近, 然而当Mg含量为20%时, 粉末氧化放热量急剧升高, 达到最高值, 为9798.8 μV·s·mg-1, 并且该粉末的能量释放非常集中。随着Mg含量继续升高, 氧化放热量下降, 这是由于Mg的能量密度远低于Al。因此, 从合金粉的氧化行为和氧化放热量来看, Al78Mg20Zr2和Al73Mg25Zr2合金粉都具有很高的热反应活性, 在较低温度下能量能够集中完全释放, 可提高能量利用率, 避免热损失, 且作为微米粉末, 并没有纳米铝那样在低温易氧化, 易团聚等缺陷, 而却有纳米铝的高活性[16], 故作为合金燃料应用于含能材料领域应该很有前景。鉴于Al78Mg20Zr2粉末优异的热反应活性, 以下研究主要以该粉末为例对其性质表征并分析其氧化过程。
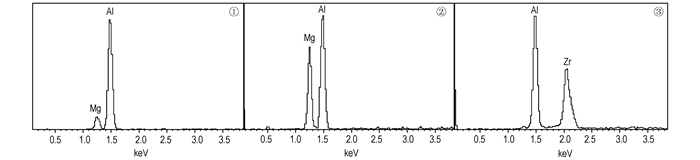
3.3 Al78Mg20Zr2粉末的SEM表征图 5为粒径小于45 μm的Al78Mg20Zr2粉末的表面和截面形貌图。从图 5a中可以看出粉末具有良好的球形度, 且粉末表面非常的光滑, 较少有细小的粉末粘附在大粒径粉末上, 粉末团聚的倾向也很低, 从图 5b中可看出粉末颗粒内的各相分布非常明显。图 6为图 5b中粉末试样在对应区域的EDS能谱图, 结合图 1的XRD结果可以得出, 图 5b中亮灰色的相(即类似①的区域)应该主要是Al相, 暗灰色的相(即类似②的区域)主要是Al3Mg2相, 白色的相(即类似③的区域)主要是Al3Zr相。所以在Al78Mg20Zr2粉末颗粒中, Al和Al3Mg2相粉末分布比较均匀, 并包覆Al3Zr相, 形成类似核壳包覆结构。

|
图 5 Al78Mg20Zr2粉末的表面和截面形貌图 Fig.5 Surface morphology of Al78Mg20Zr2 powder and cross-section morphology |
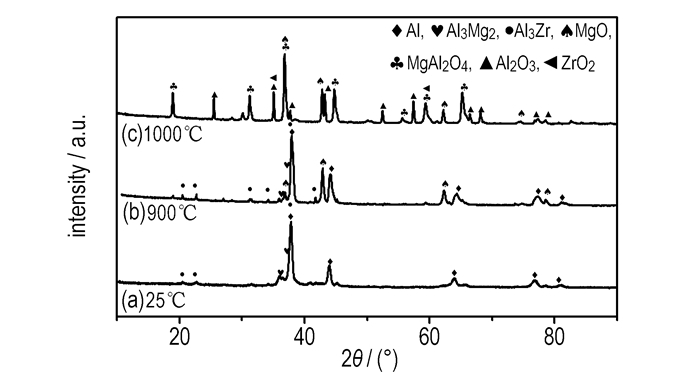
为了研究Al78Mg20Zr2粉末的氧化过程, 将粉末在O2气氛下以20 ℃·min-1升温速率分别升温至900 ℃和1000 ℃, 退火后得到氧化产物, 然后对获得的氧化产物分别进行XRD和SEM表征。图 7为不同温度氧化后粉末试样的XRD图。从图 7中可以看出, 与常温下(25 ℃)的原料粉末相比, 加热到900 ℃退火后的试样XRD中开始出现MgO峰, Al3Mg2峰变弱, 而Al和Al3Zr峰变得更强。因此可知, 粉末试样烧结到900 ℃时, Al和Al3Zr并没有出现氧化或者氧化非常少, 只有Mg选择性氧化成了MgO。而对于加热到1000 ℃(即经过了945 ℃的剧烈氧化反应)的粉末试样退火后产物全是氧化物, 为MgAl2O4、Al2O3、MgO和ZrO2。这些氧化物的出现, 表明在945 ℃发生的唯一的一次氧化放热反应基本完全。
|
图 7 Al78Mg20Zr2粉末在不同温度氧化后的XRD图 Fig.7 XRD patterns of Al78Mg20Zr2 powder oxidized at different temperatures |
图 8为Al78Mg20Zr2粉末试样在900 ℃氧化后的表面和截面形貌。从图 8可知, 粉末颗粒表面具有明显的氧化层, 有些颗粒表面有些许破裂, 但是绝大多数的粉末依然保持了较为完整的球形, 这说明虽然粉末在氧气气氛下加热到了900 ℃的高温, 但是依然没有达到粉末发生剧烈反应的程度。另外, 图 8b中依然可见清晰的Al3Zr相(即白色相), 没有发生任何变化。图 9为粉末1000 ℃氧化后的形貌图, 可以看到粉末颗粒经过剧烈反应后已经完全破裂, 颗粒基本成空壳状态。从图 9b可推知在粉末颗粒未破裂前有可能是中空结构, 剧烈氧化反应后产物主要以细小的粉末状形式存在。

|
图 8 Al78Mg20Zr2粉末试样900 ℃氧化后的形貌 Fig.8 Surface morphology of Al78Mg20Zr2 powder oxidized and cross-section morphology at 900 ℃ |

|
图 9 Al78Mg20Zr2粉末1000 ℃氧化后的形貌 Fig.9 SEM images ofAl78Mg20Zr2 powder oxidized at 1000 ℃ |
Al78Mg20Zr2和Al73Mg25Zr2粉末都发生了集中的剧烈氧化现象, 故传统的扩散氧化机制并不能很好地解释该现象。根据实验结果, 本研究提出了一个氧化机制模型, 示意图如图 10所示, 探讨粉末发生集中氧化现象的原因。
|
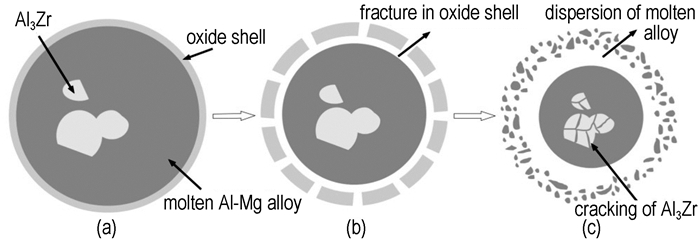
图 10 Al-Mg-Zr合金粉集中氧化过程示意图 Fig.10 Schematic diagram of intensive oxidation of Al-Mg-Zr alloy powders |
图 10a所示为合金粉末在900 ℃之前的颗粒形态, 此时的球形颗粒内部充满Al-Mg熔体, Al3Zr固体颗粒散布于熔体中, 颗粒表面氧化层是Al2O3和MgO。随着温度的升高, 表面氧化层逐渐增厚, 且颗粒内部可能会形成中空结构, 类似于球形铝粉氧化时的情况[17]。这时, 粉末颗粒将会过热, 颗粒内部的温度急剧升高, 由于熔体和氧化层的热膨胀系数不一样, 从而产生巨大的内应力。同时, 因熔化导致的颗粒体积改变和高的氧化层强度会在Al-Mg熔体中形成高压, 高压又导致了Mg的蒸发, Mg蒸气分散聚集于氧化层表面, Mg蒸气越多越利于颗粒的点火引燃[18]。巨大的应力和Mg蒸气在氧化层表面的反应共同导致了合金表面氧化层的快速破裂, 如图 10b所示。氧化层剥裂后, 颗粒表面和内部的不平衡压强将产生一种卸载波, 该卸载波将合金熔体冲击分散成大量的更小的合金液滴[19-20], 如图 10c所示, 这些由熔融的Al和Al3Mg2组成的合金液滴完全暴露在O2环境中, 从而发生剧烈的氧化反应。并且, 此时因合金熔体的氧化反应产生大量热量以及Al3Zr固体颗粒自身的氧化, 引起了Al3Zr颗粒的内部过热和崩裂[21-22]。Al3Zr颗粒的爆裂进一步的将合金熔体彻底冲击分散成更为细小的颗粒。最后, 合金粉末颗粒变成了大量的更加细小的颗粒, 从而使得氧化反应变得异常剧烈, 导致Al78Mg20Zr2和Al73Mg25Zr2粉末集中氧化现象的出现。
从实验数据和以上分析可知, Mg含量对Al-Mg-Zr合金氧化具有重要影响:直接影响易燃相Al3Mg2的含量、氧化时Mg的蒸发量、Al3Zr的含量和表面氧化层的结构等, 这些因素在粉末的氧化过程中起着重要的作用, 显著影响Al-Mg-Zr合金的氧化行为。
4 结论(1) 采用紧耦合气雾化法制备了Mg含量为5%~30%的系列Al-Mg-Zr三元合金燃料。制备的合金燃料具有良好的球形度, 主要物相有Al、Al3Mg2、Al3Zr和Al12Mg17。
(2) 随着Mg含量的升高, Al-Mg-Zr合金粉发生氧化反应的温度明显降低, 氧化过程由多步氧化逐渐转变为一步氧化, 能量释放量先增后减。其中Al93Mg5Zr2, Al88Mg10Zr2和Al83Mg15Zr2三种粉末在900 ℃后主要发生了两次氧化反应, 而Al78Mg20Zr2和Al73Mg25Zr2粉末分别在945 ℃和938 ℃发生集中氧化放热反应。
(3) 在制备的Al-Mg-Zr三元合金粉中, Al78Mg20Zr2粉末具有最大的氧化放热焓, 为-9798.8 μV·s·mg-1, 且该粉末唯一的一次氧化反应比较完全, 其优异的反应活性, 使得该合金作为燃料在火炸药领域具有潜在的应用前景。
| [1] |
Palaszewski B, Powell R. Launch vehicle performance using metallized propellants[J].
Journal of Propulsion and Power, 1994, 10(6): 828-833. DOI:10.2514/3.23821 |
| [2] |
Rosenband V, Gany A. Activated metal powders as potential energetic materials[J].
International Journal of Energetic Materials and Chemical Propulsion, 2009, 8(4): 291-307. DOI:10.1615/IntJEnergeticMaterialsChemProp.v8.i4 |
| [3] |
李颖, 宋武林, 谢长生, 等. 纳米铝粉在固体推进剂中的应用进展[J].
兵工学报, 2005, 26(1): 121-125. LI Ying, SONG Wu-lin, XIE Chang-sheng, et al. Progress in the application of nano aluminum powder in solid propellants[J]. Acta Armamentarii, 2005, 26(1): 121-125. |
| [4] |
Brooks K P, Beckstead M W. Dynamics of aluminum combustion[J].
Journal of Propulsion and Power, 1995, 11(4): 769-780. DOI:10.2514/3.23902 |
| [5] |
赵庆华, 王莉莉, 刘欣, 等. 合金燃料在固体推进剂中的应用[J].
化学推进剂与高分子材料, 2011, 9(1): 50-54. ZHAO Qing-hua, WANG Li-li, LIU Xin, et al. Application of alloy fuel in solid propellant[J]. Chemical Propellants & Polymeric Materials, 2011, 9(1): 50-54. |
| [6] |
Carlo B, Schoenitz M, Dreizin E L. Mechanically alloyed Al-Ti powders prepared by mechanical milling at cryogenic temperatures [R]. 45th AIAA/ASME/SAE/ASEE Joint Propulsion Conference & Exhibit, AIAA 2009-5078, 2009.
|
| [7] |
Shoshin Y L, Mudryy R S, Dreizin E L. Preparation and characterization of energetic Al-Mg mechanical alloy powders[J].
Combustion and Flame, 2002, 128(3): 259-269. DOI:10.1016/S0010-2180(01)00351-0 |
| [8] |
Schoenitz M, Dreizin E L. Oxidation processes and phase changes in metastable Al-Mg alloys[J].
Journal of propulsion and power, 2004, 20(6): 1064-1068. DOI:10.2514/1.9024 |
| [9] |
WANG Yi, JIANG Wei, LIU Hong-ying, et al. Thermal reactivity of nanostructure Al0.2 alloy powder used in thermites[J].
Rare Metal Materials and Engineering, 2012, 41(1): 9-13. DOI:10.1016/S1875-5372(12)60021-6 |
| [10] |
Shoshin Y L, Trunov M A, Zhu X, et al. Ignition of aluminum-rich Al-Ti mechanical alloys in air[J].
Combustion and Flame, 2006, 144(4): 688-697. DOI:10.1016/j.combustflame.2005.08.037 |
| [11] |
Zhu X, Schoenitz M, Dreizin E L. Oxidation of Mechanically alloyed Al-rich Al-Ti powders[J].
Oxidation of Metals, 2006, 65(5): 357-376. |
| [12] |
Babkin V M. Solubility of zirconium in liquid magnesium and the ML5 alloy[J].
Metal Science and Heat Treatment, 1968, 10(3): 221-223. DOI:10.1007/BF00666869 |
| [13] |
Ichikawa R, Ohashi T. Age hardening of chilled castings of Al-0.2-2wt.% Zr alloys[J].
Journal of Japan Institute of Light Metals, 1968, 18(6): 314-319. DOI:10.2464/jilm.18.314 |
| [14] |
Joshi P B, Marathe G R, Murti N S S, et al. Reactive synthesis of titanium matrix composite powders[J].
Materials Letters, 2002, 56(3): 322-328. DOI:10.1016/S0167-577X(02)00476-7 |
| [15] |
Dreizin E L, Schoenitz M. Structure and properties of Al-Mg mechanical alloys[J].
Materials Research Society, 2003, 18(8): 1827-1836. DOI:10.1557/JMR.2003.0255 |
| [16] |
Trunov M A, Umbrajkar S M, Schoenitz M, et al. Oxidation and melting of aluminum nanopowders[J].
The Journal of Physical Chemistry B, 2006, 110(26): 13094-13099. DOI:10.1021/jp0614188 |
| [17] |
Zhang S, Dreizin E L. Reaction interface for heterogeneous oxidation of aluminum powders[J].
The Journal of Physical Chemistry C, 2013, 117(27): 14025-14031. DOI:10.1021/jp402990v |
| [18] |
Mebarki N, Kumar N R, Blandin J J, et al. Correlation between ignition and oxidation behaviours of AZ91 magnesium alloy[J].
Materials Science and Technology, 2005, 21(10): 1145-1151. DOI:10.1179/174328405X58904 |
| [19] |
Levitas V I. Mechanochemical mechanism for reaction of aluminium nano-and micrometre-scale particles[J].
Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences, 2013, 371(2003): 20120215 DOI:10.1098/rsta.2012.0215 |
| [20] |
Levitas V I, Pantoya M L, Dean S. Melt dispersion mechanism for fast reaction of aluminum nano-and micron-scale particles: Flame propagation and SEM studies[J].
Combustion and Flame, 2014, 161(6): 1668-1677. DOI:10.1016/j.combustflame.2013.11.021 |
| [21] |
Geẞwein H, Binder J R, Hauẞelt J, et al. Reaction-diffusion model for the reaction bonding of alumina-zirconia composites using the intermetallic compound ZrAl3[J].
Thermochimica Acta, 2006, 451(1): 139-148. |
| [22] |
Geẞwein H, Binder J R. Thermokinetic study of the oxidation of ZrAl3 powders[J].
Thermochim Acta, 2006, 444(1): 6-12. DOI:10.1016/j.tca.2006.02.010 |
Ternary Al-Mg-Zr alloy fuels with Mg content ranging from 5% to 30% were prepared by close-coupled gas atomization and the most reactive powder among the prepared alloy powders was identified