为满足日益增长的军事和民用领域的各种需求, 设计研发具有优良爆轰性能, 环境友好以及安全钝感等特点的新型高能量密度含能材料(HEDMs)显得尤为重要[1-4]。由四唑及其衍生物构成的高氮四唑类含能材料, 因其具有良好的氧平衡, 且分解产物主要为N2、对环境污染小等特点, 已成为国内外重点研究方向之一[5-8]。含能配合物一般具有强烈爆炸特性, 在起爆药、固体推进剂催化剂领域应用较多, 其中以四唑类为配体的过渡金属含能配合物, 由于其结构多样, 且具有良好的能量性质, 受到研究者的广泛关注[9-11]。
相对于5-氨基四唑, 1, 5-二氨基四唑(DAT)氮含量高达84%, 其分解温度高达197 ℃, 热稳定性较好。除1位N原子外, DAT分子中其他N原子均有形成配位键之可能, 尤其是4位N原子[12-14]。本课题组合成出了一系列不同的含能配合物, 如(ClO4)2, (ClO4)2, (ClO4)2, (PA)2·4H2O, 等, 并研究了其晶体结构、热性能及感度性能, 结果表明这些含能配合物有望应用于含能材料领域[15-19]。
基于此, 本研究以DAT和硝酸银为原料, 合成了新型高氮含能配合物—[Ag2(DAT)4](NO3)2, 并采用元素分析、傅里叶变换红外光谱(FTIR)对其进行表征。利用X-射线单晶衍射仪(XRD)对其晶体结构进行测定。采用差示扫描量热(DSC)技术研究其热分解性能, 计算得到其非等温动力学参数和热爆炸临界温度等热力学参数。利用氧弹量热技术测定其燃烧热, 并计算其标准生成焓。最后测试其撞击、摩擦和火焰感度等, 为其后续应用提供基础数据。
2 实验部分 2.1 试剂和仪器试剂: AgNO3、氨基硫脲、氧化铅、乙醇等, 国药集团化学试剂有限公司, 分析纯; DAT为实验室参照文献[20]方法自制, 精制后用于后续实验, 实验用水为去离子水。
仪器及测试条件: Thermo Electron SPA公司Flash EA 1112全自动微量元素分析仪; Nicolet公司傅里叶变换红外光谱仪: KBr压片, 扫描范围4000~400 cm-1, 分辨率6 cm-1; Bruker SMART APEX CCD单晶衍射仪; Perkin-Elmer公司Pyris-1型热分析仪:流动N2气氛, 流速20 mL·min-1; Parr公司6200氧弹量热仪。
2.2 合成过程称取DAT 0.41 g (5 mmol)溶解于20 mL去离子水中作为底液, 在75 ℃下加热搅拌, 称取AgNO3 0.34 g (2 mmol)溶于5 mL去离子水中并缓慢滴加入底液, 反应60 min后冷却至室温, 过滤, 去离子水洗涤两遍, 乙醇洗涤两遍并干燥, 得到白色粉末产物0.64 g, 收率86%。母液在室温下缓慢蒸发, 4天后得到可用于结构测定的透明块状晶体。IR (KBr, ν/cm-1): 3324, 3153, 1657, 1383, 1110, 1077, 1003, 935, 699, 605。Anal. calcd for C4H16Ag2N26O6 (740.17): C 6.49, H 2.18, N 49.21; found C 6.47, H 2.15, N 49.26。
2.3 晶体结构分析选取尺寸为0.10 mm×0.15 mm×0.17 mm的晶体, 采用Bruker SMART APEX CCD单晶衍射仪, 以石墨单色器单色化的Mo Kα射线(λ=0.071073 nm)为光源, 通过ω-θ扫描方式在90(2)K, 2.07°≤θ≤27.50°下收集11692个衍射点, 其中2526个独立衍射点, 所有强度数据进行Lp因子及经验吸收校正。晶体结构通过直接法由SHELXS-97解析得到[21], 并由全矩阵最小二乘法精修由SHELXL-97程序完成[22]。非氢原子由直接法获得, 氢原子通过理论加氢获得。详细参数见表 1。该晶体CIF文件已保存在剑桥晶体结构数据中心(CCDC No. 913276)。
| 表 1 [Ag2(DAT)4](NO3)2的晶体结构数据和结构精修参数 Tab.1 Crystal data and structure refinement details for [Ag2(DAT)4](NO3)2 |
高氮含能配合物[Ag2(DAT)4](NO3)2属于单斜晶系, P21/n空间群, 其结构及堆积图分别见图 1和图 2。表 2、表 3和表 4分别列出该配合物晶体结构的部分键长键角以及氢键数据。
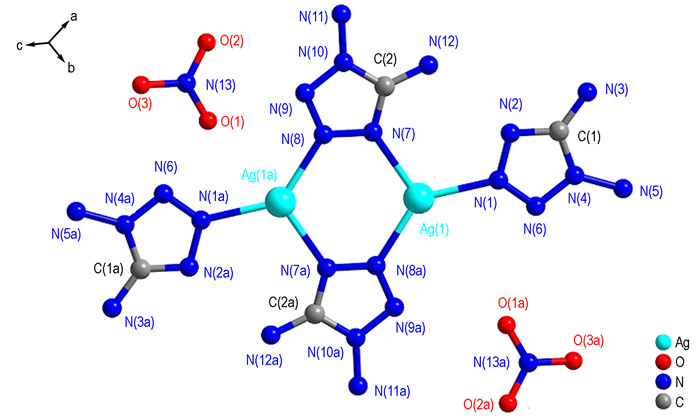
|
图 1 [Ag2(DAT)4](NO3)2的分子结构 Fig.1 Molecular structure of (DAT)4][Ag2(DAT)4](NO3)2 |
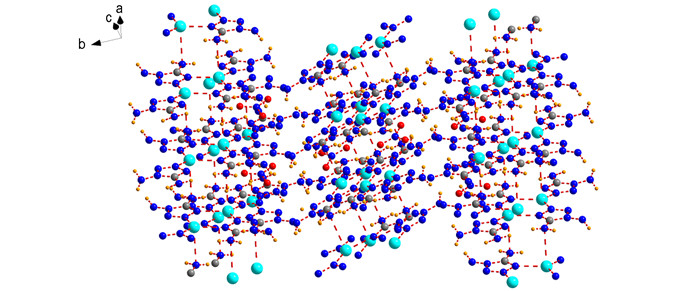
|
图 2 [Ag2(DAT)4](NO3)2的堆积图 Fig.2 Packing diagram of [Ag2(DAT)4](NO3)2 |
| 表 2 [Ag2(DAT)4](NO3)2的部分键长 Tab.2 Selected bond lengths for [Ag2(DAT)4](NO3)2 |
| 表 3 [Ag2(DAT)4](NO3)2的部分键角 Tab.3 Selected bond angles for [Ag2(DAT)4](NO3)2 |
| 表 4 [Ag2(DAT)4](NO3)2的部分氢键 Tab.4 Selected hydrogen bonds for [Ag2(DAT)4](NO3)2 |
配合物[Ag2(DAT)4](NO3)2的分子单元中含有2个Ag+, 4个DAT分子和2个NO3-。中心金属Ag(1)表现为三配位, 呈sp2杂化, 分别与3个来自不同DAT分子中的N原子形成配位键, 键长分别为2.259, 2.285, 2.231Å;键角N(1)—Ag(1)—N(7), N(1)—Ag(1)—N(8a)#1, N(7)—Ag(1)—N(8a)#1分别为109.8°, 135.6°, 113.9°, 配位形成了以Ag+为顶点的畸变四面体结构, 其Ag—N配位键较Zn(DAT)6(ClO4)2[18]中Zn—N键(2.218 Å)长, 较Mn(DAT)6(ClO4)2[23]中Mn—N键(2.291 Å)短。4个DAT分子以两种配位形式参与中心离子Ag+的配位, 其中两个DAT分子作为桥联配体, 由四唑环上3, 4位氮原子N(7)、N(8)以及N(7a)、N(8a)分别与两个Ag+形成配位键, 来自这两个DAT分子中的四个N原子和两个Ag+构成共平面的六元环状结构, 另有两个DAT分子作为单齿配体, 分别提供四唑环上3位N原子N(1)和N(1a)与中心金属Ag+形成配位键。由表 2可知, DAT配体分子的N—N键的键长为1.290~1.402 Å, 介于N—N单键(1.454 Å)和N=N双键(1.245 Å)之间; C—N键的键长为1.330~1.347 Å, 介于C—N单键(1.47 Å)和C=N双键(1.27 Å)之间。这说明由于存在离域大π键作用, 使四唑环的键长趋于平均, 且DAT配体分子中各原子共面性较好, 形成一个大的共轭体系, 与已报道的DAT含能配合物结构中DAT分子情况类似[19-23]。
配合物分子中含有一定数量的氢键, 如表 4所示。其中具有DAT配体分子间存在的氢键, 如N(12)—H(12A)…N(2);此外多数是外界NO3-中的O原子和DAT配体中氨基N原子形成的分子间氢键, 如N(3)—H(3A)…O(1), N(11)—H(11A)…O(2), N(3)—H(3B)…O(2)等, 这些氢键的存在对提高配合物稳定性有重要作用。由图 2可以看出, 在DAT配体分子和NO3-离子间存在的分子间氢键作用下, 配合物形成二维层状结构, 片层之间也是通过DAT配体分子和NO3-离子间的分子间氢键连接起来形成晶体结构。以上分析表明, NO3-离子对于目标配合物晶体结构的形成和稳定具有重要作用, 分子内及分子间氢键共同作用, 形成稳定的配合物结构。
3.2 热行为分析10 ℃·min-1时含能配合物[Ag2(DAT)4](NO3)2的DSC曲线如图 3所示。由图 3可知, 目标配合物的热分解行为包含一个吸热过程和一个放热过程, 其吸热过程起始于188 ℃, 其尖锐吸热峰温度为196.2 ℃, 该过程为[Ag2(DAT)4](NO3)2的晶体熔化过程。熔化后该配合物立即放热分解, 放热峰出现在202~256 ℃之间, 其放热峰温度为228.6 ℃。
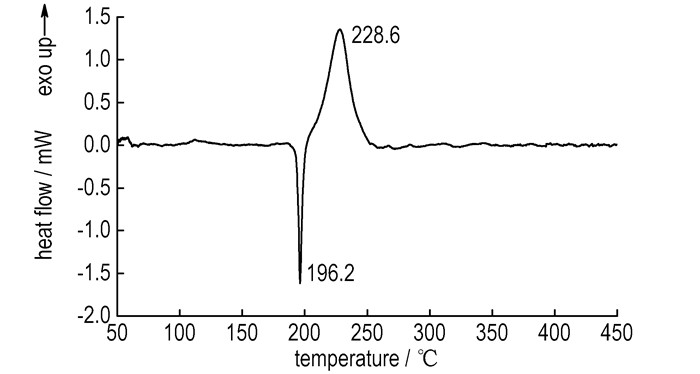
|
图 3 [Ag2(DAT)4](NO3)2的DSC曲线(10 ℃·min-1) Fig.3 DSC curve of [Ag2(DAT)4](NO3)2 at heating rate of 10 ℃·min-1 |
测定[Ag2(DAT)4](NO3)2在5、10、15、20 ℃·min-1四种线性升温速率下的DSC曲线, 得到其在不同升温速率下放热峰的峰温数据, 列于表 5。根据Kissinger法[24]和Ozawa-Doyle[25]法计算其放热分解反应的表观活化能Ea和指前因子A, 两种方法的计算公式如式(1)和式(2)所示:
| 表 5 [Ag2(DAT)4](NO3)2的放热分解峰温度及非等温动力学参数 Tab.5 Peak temperatures and non-isothermal kinetic parameters for the exothermic decomposition of [Ag2(DAT)4](NO3)2 |
| $ \ln \left( {\frac{\beta }{{T_{\rm{p}}^2}}} \right) = \ln \left( {\frac{{{A_{\rm{K}}}R}}{{{E_{\rm{K}}}}}} \right)-\frac{{{E_{\rm{K}}}}}{R}\frac{1}{{{T_{\rm{p}}}}} $ | (1) |
| $ \log \beta + \frac{{0.4567{E_{\rm{a}}}}}{{R{T_{\rm{p}}}}} = C $ | (2) |
式中,Tp为放热分解峰温, ℃, 由DSC曲线得到; R为气体常数, 8.314 J·mol-1·℃-1; β为线性升温速率, ℃·min-1; C为常数, 应用两种方法计算得到的非等温动力学参数同样列于表 5。
由表 5可以看出, 通过两种方法所计算得到的[Ag2(DAT)4](NO3)2表观活化能结果相近, 分别为204.9 kJ·mol-1和202.8 kJ·mol-1, 且可以得到其热分解的Arrhenius方程为: lnk=19.54-203.9×103/RT, 其中k为非等温动力学反应速率常数。
3.3 标准生成焓及热爆炸临界温度计算对新型含能配合物, 燃烧热和生成焓是评价其含能特性的重要参数。选择Parr公司1104型氧弹, 充氧1 min, 使内部气压达到3.0 MPa, 测试条件为室温25 ℃, 相对湿度30%, 药量500 mg。平行测试5次, 测定[Ag2(DAT)4](NO3)2的定容燃烧热(Qv)为-4177.59 kJ·mol-1。通过其燃烧反应方程式(3)和计算式(4)得到其定压燃烧热(ΔH)为-4149.08 kJ·mol-1。
| $ \begin{array}{l} {{\rm{C}}_{\rm{4}}}{{\rm{H}}_{{\rm{16}}}}{\rm{A}}{{\rm{g}}_{\rm{2}}}{{\rm{N}}_{{\rm{26}}}}{{\rm{O}}_{\rm{6}}}\left( {\rm{s}} \right){\rm{ + 11/2}}{{\rm{O}}_{\rm{2}}}\left( {\rm{g}} \right){\rm{ = A}}{{\rm{g}}_{\rm{2}}}{\rm{O}}\left( {\rm{s}} \right){\rm{ + 4C}}{{\rm{O}}_{\rm{2}}}\left( {\rm{g}} \right){\rm{ + }}\\ \;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;\;{\rm{8}}{{\rm{H}}_{\rm{2}}}{\rm{O}}(\mathit{l}){\rm{ + 13}}{{\rm{N}}_{\rm{2}}}\left( {\rm{g}} \right) \end{array} $ | (3) |
| $ \Delta H = {Q_p} = {Q_v} + \Delta nRT $ | (4) |
通过已知的标准生成焓ΔfH298Θ[Ag2O, s]=-30.54 kJ·mol-1, ΔfH298Θ[H2O, l]=-285.8 kJ·mol-1, ΔfH298Θ(CO2, g)=-393.5 kJ·mol-1[26], 通过下式计算[Ag2(DAT)4](NO3)2的标准生成焓为ΔfH298Θ=258.14 kJ·mol-1。
| $ \begin{gathered} {\Delta _{\rm{f}}}H_{298}^\Theta \left( l \right) = {\Delta _{\rm{f}}}{H^\Theta }\left( {{\rm{A}}{{\rm{g}}_{\rm{2}}}{\rm{O, s}}} \right) + 8{\Delta _{\rm{f}}}{H^\Theta }\left( {{{\rm{H}}_{\rm{2}}}{\rm{O}}, l} \right) + \hfill \\\;\;\;\;\;\;\; 4{\Delta _{\rm{f}}}{H^\Theta }\left( {{\rm{C}}{{\rm{O}}_{\rm{2}}}{\rm{, g}}} \right)-{\Delta _{\rm{c}}}{H^\Theta }\left( {\rm{s}} \right) \hfill \\ \end{gathered} $ | (5) |
通常采用热爆炸临界温度(Tbp)来评估含能材料的热安全性。根据热爆炸临界温度估算式[27-29], 当升温速率β→0时, 所对应的分解峰值温度可通过下式进行估算:
| $ {T_{{\rm{p}}\mathit{i}}} = {T_{{\rm{p0}}}} + a\beta + b{\beta ^2} + c{\beta ^3} $ | (6) |
式中, Tpi为升温速率βi时的峰温, ℃; a、b、c为常数。通过待定系数拟合方程求得升温速率β→0时对应的峰温为Tp0=214.2 ℃。然后根据方程(7), 求得目标配合物的热爆炸临界温度Tbp=224.4 ℃:
| $ {T_{{\rm{bp}}}} = \frac{{E - \sqrt {{E^2} - 4ER{T_{{\rm{p}}0}}} }}{{2R}} $ | (7) |
同时由下述方程可计算得到热力学参数ΔS≠, ΔH≠和ΔG≠的值[27-29]:
| $ A = \frac{{{K_{\rm{B}}}T}}{h}{{\rm{e}}^{\Delta S \ne \mathit{/R}}} $ | (8) |
| $ \Delta {H^ \ne } = E-RT $ | (9) |
| $ \Delta {G^ \ne } = \Delta {H^ \ne }-T\Delta {S^ \ne } $ | (10) |
式中,E为Ozawa方法计算得到的活化能, kB为玻尔兹曼常数, 1.381×10-23 J·K-1; h为普朗克常数, 6.626×10-34 J·s-1。最终计算得到的热力学参数分别为ΔS≠= -86.54 J·K-1·mol-1; ΔH≠= 200.85 kJ·mol-1; ΔG≠=243.02 kJ·mol-1。
3.4 感度性能研究按照GJB5891.22-2006、GJB5891.24-2006、GJB5891.25-2006, 测试[Ag2(DAT)4](NO3)2的撞击感度、摩擦感度和火焰感度。采用CGY-1型机械撞击感度仪, 测试条件为药量0.02 g, 压药压强39.2 MPa, 落锤800 g, 升降法测试[Ag2(DAT)4](NO3)2的撞击感度H50为0, 表明其对撞击钝感; 采用MGY-1摆式摩擦感度仪, 测试条件为药量0.02 g, 摆锤1.5 kg, 摆角90°, 表压1.96 MPa, 测试结果表明[Ag2(DAT)4](NO3)2摩擦感度发火率为40%;采用HGY-1型火焰感度仪, 测试条件为药量0.02 g, 压药压强58.8 MPa, 标准黑药柱(WJ636)点火, 升降法测试[Ag2(DAT)4](NO3)2的火焰感度H50为0, 表明其对火焰钝感。
由上述结果可知, [Ag2(DAT)4](NO3)2对外界摩擦刺激较敏感, 对机械撞击和火焰刺激钝感, 属于钝感含能材料。
4 结论(1) 以1, 5-二氨基四唑及AgNO3为起始原料合成新型高氮含能配合物[Ag2(DAT)4](NO3)2, 收率86%, 并通过元素分析、红外光谱对其结构进行了表征。
(2) [Ag2(DAT)4](NO3)2的单晶分析结果表明, 该配合物属于双核结构, 中心Ag+和来自三个DAT分子的六个N原子配位形成畸变四面体结构, 同时一个结构单元中两个Ag+和四个N原子形成平面六元环结构。此外分子中含有一定数量的氢键, 有助于提高其结构稳定性。
(3) DSC分析表明[Ag2(DAT)4](NO3)2分解过程经历一个吸热过程和一个放热过程, 放热峰温为228.6 ℃。运用Kissinger法和Ozawa-Doyle法计算得其表观活化能分别为204.9 kJ·mol-1和202.8 kJ·mol-1, 其标准生成焓为258.14 kJ·mol-1, 热爆炸临界温度Tbp=224.4 ℃, 其热力学参数分别为ΔS≠=-86.54 J·K-1·mol-1; ΔH≠=200.85 kJ·mol-1; ΔG≠=243.02 kJ·mol-1。
(4) 感度测试表明该配合物对摩擦刺激较敏感, 但对撞击和火焰刺激钝感, 属于钝感含能材料。
| [1] |
Klapötke T M, Petermayer C, Piercey D C, et al. 1, 3-Bis(nitroimido)-1, 2, 3-triazolate anion, the N-nitroimide moiety, and the strategy of alternating positive and negative charges in the design of energetic materials[J].
Journal of the American Chemical Society, 2012, 134(51): 20827-20836. DOI:10.1021/ja310384y |
| [2] |
Klapötke T M, Stierstorfer J. The CN7- anion[J].
Journal of the American Chemical Society, 2009, 131(3): 1122-1134. DOI:10.1021/ja8077522 |
| [3] |
Ye C F, Gard G L, Winter R W, et al. Synthesis of pentafluorosulfanylpyrazole and pentafluorosulfanyl-1, 2, 3-trizole and their derivatives as energetic materials by click chemistry[J].
Organic Letters, 2007, 9(19): 3841-3844. DOI:10.1021/ol701602a |
| [4] |
Sun Q, Li Z, Xu K Z, et al. Synthesis and characterization of a new cadmium complex based on 1, 1-diamino-2, 2-dinitroethylene[J].
Journal of Coordination Chemistry, 2014, 67(15): 2576-2582. DOI:10.1080/00958972.2014.951343 |
| [5] |
Gao H X, Shreeve J M. Azole-based energetic salts[J].
Chemical Review, 2011, 111(11): 7377-7436. DOI:10.1021/cr200039c |
| [6] |
Klapötke T M, Karaghiosoff K, Mayer P, et al. Synthesis and characterization of 1, 4-dimethyl-5-aminotetrazolium 5-nitrotetrazolate[J].
Propellants, Explosives, Pyrotechnics, 2006, 31(3): 188-195. DOI:10.1002/(ISSN)1521-4087 |
| [7] |
Klapotke T M, Sabate C M, Stierstorfer J. Neutral 5-nitrotetrazoles: easy initiation with low pollution[J].
New Journal of Chemistry, 2009, 33(1): 136-147. DOI:10.1039/B812529E |
| [8] |
Joo Y-H, Shreeve J M. Nitroimino-tetrazolates and oxy-nitroimino-tetrazolates[J].
Journal of the American Chemical Society, 2010, 132(42): 15081-15090. DOI:10.1021/ja107729c |
| [9] |
Joo Y-K, Twamley Brendan, Shreeve J M. Carbonyl and oxalyl bridged bis(1, 5-diaminotetrazole)-based energetic salts[J].
Chemistry A European Journal, 2009, 15(36): 9097-9104. DOI:10.1002/chem.v15:36 |
| [10] |
Fischer N, Klapötke T M, Piercey D G, et al. Hydroxylammonium 5-nitriminotetrazolated[J].
Z.Anorg.Allg.Chem, 2012, 638(2): 302-310. DOI:10.1002/zaac.201100479 |
| [11] |
Klapötke T M, Piercey D G. 1, 1'-Azobis(tetrazole): a highly energetic nitrogen-rich compound with a N10 chain[J].
Inorgnic Chemistry, 2011, 50(7): 2732-2734. DOI:10.1021/ic200071q |
| [12] |
Li Z M, Zhang J G, Yang W, et al. Synthesis and strucutre characterization of a new 1D polymeric energetic complex [Hg(DAT)6]n (DAT=1, 5-diaminotetrazole)[J].
Chinese Journal of Strucutre Chemistry, 2013, 32(5): 653-658. |
| [13] |
齐书元, 张同来, 杨利, 等. 1, 5-二氨基四唑及其系列化合物研究进展[J].
含能材料, 2009, 17(4): 486-490. QI Shu-yuan, ZHANG Tong-lai, YANG Li, et al. Progress in 1, 5-diamino-1H-tetrazole and its derivatives[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(4): 486-490. |
| [14] |
Zhai Q G, Li S N, Gao X, et al. Self-assembly of a novel 3D copper-tetrazolate supramolecular framework via interpenetration porous 2D double-layer motifs[J].
Inorganic Chemistry Communications, 2010, 13(1): 211-214. DOI:10.1016/j.inoche.2009.11.027 |
| [15] |
Cui Y, Zhang J G, Zhang T L, et al. Synthesis, structural investigation, thermal decomposition mechanism and sensitivity properties of an energetic compound (ClO4)2 (DAT=1, 5-diamiontetrazole)[J].
Journal of Hazardous Materials, 2008, 160(1): 45-50. DOI:10.1016/j.jhazmat.2008.02.078 |
| [16] |
Cui Y, Zhang T L, Zhang J G. Study on crystal structure and thermal decomposition mechanism of a novel coordination compound (PA)2·2H2O[J].
Propellants, Explosives, Pyrotechnics, 2008, 33(6): 437-442. DOI:10.1002/prep.v33:6 |
| [17] |
Cui Y, Zhang J G, Zhang T L, et al. ..5H2O (DAT=1, 5-diamiontetrazole)Synthesis, structural investigation and thermal analyses of a novel coordination compound (HTNR)2·3[J].
Journal of Molecular Structure, 2008, 889(1-3): 177-185. DOI:10.1016/j.molstruc.2008.01.044 |
| [18] |
尚静, 张建国, 崔燕, 等. 含能配合物(ClO4)2 (DAT=1, 5-二氨基四唑)的合成、晶体结构及性能[J].
化学学报, 2010, 68(3): 233-236. SHANG Jing, ZHANG Jian-guo, CUI Yan, et al. Synthesis, crystal structure, and properties of an energetic compound (ClO4)2[J]. Acta Chimica Sinica, 2010, 68(3): 233-236. |
| [19] |
Bi Y G, Feng Y A, Zhang T L, et al. Synthesis, structure, and ermal decomposition of two copper coordination compounds and with nitrogen rich 1, 5-diaminotetrazole(DAT)[J].
Journal of Coordination Chemistry, 2015, 68(1): 181-194. DOI:10.1080/00958972.2014.981167 |
| [20] |
Gálvez-Ruiz J C, Holl G, Klapötke, T .M. Derivatives of 1, 5'-diamino-1h-tetrazole: a new family of energetic heterocyclic-based sals[J].
Inorgnic Chemistry, 2005, 44(12): 4237-4253. DOI:10.1021/ic050104g |
| [21] |
Sheldrick G M, SHELXS-97, Program for solution of crystalstructures, University of Gottingen, Germany, 1990.
|
| [22] |
Sheldrick G M, SHELXL-97, Program for refinement of crystalstructures, University of Gottingen, Germany, 1997.
|
| [23] |
齐书元, 张建国, 张同来, 等. 含能配合物(ClO4)2的合成、晶体结构、热行为及感度性质[J].
高等学校化学学报, 2009, 30(10): 1935-1939. QI Shu-yuan, ZHANG Jian-guo, ZHANG Tong-lai, et al. Synthesis, crystal structure, thermal behavior and sensitivity propertse of a new energetic compound (ClO4)2[J]. Chemical Journal of Chinese Universities, 2009, 30(10): 1935-1939. DOI:10.3321/j.issn:0251-0790.2009.10.005 |
| [24] |
Kissinger H E. Reaction kinetics in differential thermal analysis[J].
Anal Chem, 1957, 19: 1702-1706. |
| [25] |
Ozawa T. A new method of analyzing thermogravimetric data bull[J].
Chem Soc Jpn, 1965, 38: 1881-1886. DOI:10.1246/bcsj.38.1881 |
| [26] |
Li F G, Bi Y G, Zhang T L, et al. Nitrogen-rich salts based on the energetic anion: a promising design in the development of new energetic materials[J].
Inorgnic Chemistry, 2015, 54: 2050-2057. DOI:10.1021/ic503021c |
| [27] |
胡拥鹏, 赵旭芳, 赵宁宁, 等. DNGTz的非等温热分解动力学及热安全性[J].
含能材料, 2014, 22(6): 767-773. HU Yong-peng, ZHAO Xu-fang, ZHAO Ning-ning, et al. Non-isothermalthermal decomposition kinetics and thermal safety of DNGTz[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2014, 22(6): 767-773. DOI:10.11943/j.issn.1006-9941.2014.06.011 |
| [28] |
ZHANG Tong-lai, HU Rong-zu, XIE Yi, et al. The estimation of critical temperature of thermal explosion for energetic materials using non-isothermal DSC[J].
Thermochimica Acta, 1994, 244(2): 171-176. |
| [29] |
Zhang Hang, Xu Kang-zhen, Gao Shuai, et al. Characterization and thermal properties of 2-(dinitromethylene)-1, 3-diazacyclopentane guanidine salt[J].
Indian Journal of Chemistry, 2013, 52: 473-479. |
A novel energetic complex of [Ag2(DAT)4](NO3)2 has been synthesized. Its structure was characterized by X-ray single-crystal diffraction. The thermal decomposition of the compound was studied by DSC, and the non-isothermal kinetic parameters were calculated. The heat of formation and the critical temperature of thermal explosion were determined. The sensitivities were also tested.




