含能材料直接关系到武器装备的射程、威力、安全性等关键性能, 为了适应不同战场环境对武器系统的特殊需求, 现代武器系统对含能材料的爆轰性能和安全性提出了更高的要求, 虽然军用单组份炸药的研究范围和种类不断扩大, 但有实际应用价值的单组份仍很少。含能材料合成研究者一直在寻找能量密度高、感度低、热稳定性好的新型含能材料, 多硝基氮杂环含能化合物成为含能材料研究领域的热点, 这类化合物能形成类苯结构的大共轭体系, 是一类静电、撞击和摩擦感度低、爆轰性能良好的单质炸药, 具有良好的潜在应用前景[1-4]。4, 4′, 5, 5′-四硝基-2, 2′-联咪唑 (TNBI) 是多硝基氮杂环含能化合物的一个代表, 其密度为1.80 g·cm-3, 爆速为7840 m·s-1, 爆压为27.6 GPa, 生成热232 kJ·mol-1, 撞击感度5.7 J, 摩擦感度351 N, 分解温度290 ℃[5]。1990年, Cromer等[6-7]首次报道了TNBI及其铵盐的晶体结构。随后, 各国含能材料研究者相继开展了关于TNBI结构与性能的理论研究、TNBI金属盐 (钠盐、钾盐、锂盐) 及TNBI富氮含能离子盐 (铵盐、肼盐、羟胺盐、胍盐、氨基胍盐、二氨基胍盐、三氨基胍盐及氮杂环盐等) 的合成及性能研究, 期望消除和解决TNBI分子结构中存在的酸性问题, 并开展了部分应用探索研究。[5, 8-14]
文献[11]报道的TNBI合成过程, 需在亚硝酸钠/尿素/浓硫酸体系、85~90 ℃高温反应16 h, 该操作工艺反应温度高、反应时间长、过程较为剧烈、危险性高。基于此, 本研究对TNBI的合成工艺进行了改进, 以80%硝酸/浓硫酸体系代替硝酸钠/尿素/浓硫酸体系、45 ℃反应4 h, 反应过程温和平稳; 利用TNBI和不同有机胺的复分解、中和等反应制备了七种未见文献报道的TNBI含能离子盐; 培养了TNBI·H2O单晶, 并进行了单晶结构解析; 用DSC、TG等方法研究了七种含能离子盐的热性能。
2 实验部分 2.1 试剂与仪器乙酸铵、乙二醛 (37%~40%)、甲醇、乙醇、氢氧化钠, 分析纯, 成都市科龙化工试剂厂; 浓硫酸 (95%~98%)、浓硝酸 (98%), 工业级, 西安福晨化学试剂有限公司; 二氨基呋咱、二肼基四嗪、4-氨基-1, 2, 4-三氮唑、80%硝酸, 均为实验室自制; 草酰肼、缩二胍盐酸盐、脒基脲硝酸盐、尿素, 分析纯, 济南伟都化工试剂有限公司。
NEXUS 870型傅里叶变换红外光谱仪, 美国热电尼高力公司; AV 500型 (500MHz) 超导核磁共振仪, 瑞士BRUKER公司; VARIO-EL-3型元素分析仪, 德国EXEMENTAR公司; LC-2010A型高效液相色谱仪 (归一化法), 日本岛津公司; Q-200差示扫描量热仪, 美国TA公司; TA 2950热重仪, 美国Nicolet公司; Smart APEXⅡCCD衍射仪, 瑞士BRUKER公司。
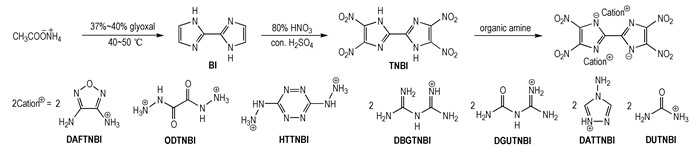
2.2 合成路线以乙酸铵和乙二醛为原料, 经环化、硝化反应合成了4, 4′, 5, 5′-四硝基-2, 2′-联咪唑 (TNBI), TNBI与有机胺发生复分解、中和等反应制备了七种有机含能离子盐, 合成路线如Scheme 1所示。
|
Scheme1 Synthetic routes of TNBI and its energetic ion salts |
室温下, 依次将79.7 g (1.03 mol) 乙酸铵、50.0 mL蒸馏水加入反应瓶中, 搅拌溶解, 体系升温至45℃, 保持温度在45 ℃滴加56.1 g (37.2 mmol) 质量分数为37%~40%乙二醛水溶液, 滴加完毕后, 在45 ℃保温反应3 h, 过滤、水洗、乙醇洗、干燥得灰色固体8.5 g, 收率49.2%, 纯度99.0%(HPLC)。
1H NMR (DMSO-d6, 500 MHz) δ: 7.066(s, 4H, 4CH), 12.66(s, 2H, 2NH); 13C NMR (DMSO-d6, 125 MHz) δ: 139.83; IR (KBr, ν/cm-1): 3143, 3074, 3001, 2896, 2805, 1678, 1545, 1436, 1404, 1333, 1217, 1144, 1104, 939, 915, 887, 828, 763, 747, 689。Anal.Calcd. for C6H6N4(%): C 53.72, H 4.51, N 41.77; Found C 53.63, H 4.56, N 41.84。
2.3.2 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑 (TNBI) 的合成搅拌下, 在温度20~25 ℃, 将1.0 g (7.46 mmol) 2, 2′-联咪唑加入到10.0 mL质量分数为95%~98%的浓硫酸中, 升温至45 ℃, 滴加13.0 mL质量分数为80%的硝酸和13.0 mL质量分数为95%~98%的浓硫酸混合溶液, 加完后在45 ℃反应4 h, 将反应液倒入40.0 g碎冰中, 过滤、冷水洗、干燥得黄色固体1.35 g, 收率为51.7%, 纯度99.2%(HPLC)。
1H NMR (DMSO-d6, 500 MHz) δ: 7.308(s, 2H, 2NH); 13C NMR (DMSO-d6, 125 MHz) δ: 138.67, 139.05; IR (KBr, ν/cm-1): 3608, 3538, 2474, 1844, 1589, 1537, 1485, 1412, 1368, 1320, 1287, 1229, 919, 853, 809, 745, 690。Anal.Calcd. for C6H2N8O8·2H2O (%): C 20.58, H 1.73, N 32.00; Found C 20.67, H 1.69, N 32.08。
2.3.3 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑二氨基呋咱盐 (DAFTNBI) 的合成室温下, 向装有温度计、搅拌及冷凝器的25 mL三口瓶中, 依次加入0.175 g (0.5 mmol) TNBI和10.0 mL甲醇, 搅拌溶解后, 加入0.1 g (1 mmol) 二氨基呋咱, 升温至50 ℃反应4 h, 自然冷却至室温析出固体, 过滤、甲醇洗、干燥得黄色固体0.19 g, 收率71.4%, 纯度98.9%。
1H NMR (DMSO-d6, 500 MHz) δ: 6.596(s, 10H, 2(AFH+)); 13C NMR (DMSO-d6, 125 MHz) δ: 138.68, 139.09, 150.17; IR (KBr, ν/cm-1): 3609, 3537, 3438, 3328, 1846, 1627, 1589, 1536, 1484, 1412, 1367, 1321, 1287, 1229, 919, 853, 809, 744, 689。Anal.Calcd. for C10H10N16O10·H2O (%): C 22.56, H 2.27, N 42.10; Found C 22.47, H 2.32, N 42.04。
2.3.4 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑草酰肼盐 (ODTNBI) 的合成室温下, 向装有温度计、搅拌及冷凝器的25 mL三口瓶中, 依次加入0.175 g (0.5 mmol) TNBI和10.0 mL甲醇, 搅拌溶解后, 加入0.059 g (0.5 mmol) 草酰肼, 升温至60 ℃反应3 h, 自然冷却至室温析出固体, 过滤、甲醇洗、干燥得黄色固体0.18 g, 收率83.3%, 纯度98.7%。
1H NMR (DMSO-d6, 500 MHz) δ: 8.552(s, 8H, ODH2+); 13C NMR (DMSO-d6, 125 MHz) δ: 140.11, 142.79, 157.78; IR (KBr, ν/cm-1): 3356, 3291, 3247, 2986, 1702, 1617, 1580, 1539, 1512, 1493, 1451, 1405, 1307, 1269, 1232, 1132, 1053, 980, 951, 856, 815, 793, 700。Anal.Calcd. for C8H8N12O10(%): C 22.23, H 1.87, N 38.89; Found C 22.27, H 1.92, N 38.94。
2.3.5 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑二肼基四嗪盐 (HTTNBI) 的合成室温下, 向装有温度计、搅拌及冷凝器的25 mL三口瓶中, 依次加入0.175 g (0.5 mmol) TNBI和10.0 mL甲醇, 搅拌溶解后, 加入0.071 g (0.5 mmol) 二肼基四嗪, 升温至70 ℃反应2 h, 自然冷却至室温析出固体, 过滤、甲醇洗、干燥得橘红色固体0.22 g, 收率96.5%, 纯度98.9%。
1H NMR (DMSO-d6, 500 MHz) δ: 9.381(s, 6H, 2NH3+), 10.67(s, 2H, 2NH); 13C NMR (DMSO-d6, 125 MHz) δ: 139.96, 142.48, 161.80; IR (KBr, ν/cm-1): 3210, 1595, 1549, 1498, 1466, 1402, 1363, 1313, 1274, 1233, 1118, 1051, 945, 854, 811, 754, 701。Anal.Calcd.for C8H8N16O8(%): C 21.06, H 1.77, N 49.12; Found C 21.12, H 1.82, N 49.08。
2.3.6 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑缩二胍盐 (DBGTNBI) 的合成室温下, 向装有温度计、搅拌及冷凝器的25 mL三口瓶中, 依次加入0.175 g (0.5 mmol) TNBI、8.0 mL甲醇、2.0 mL蒸馏水和0.04 g (1 mmol) 氢氧化钠, 搅拌溶解后, 升温至50 ℃, 加入0.138 g (1 mmol) 缩二胍盐酸盐, 在50℃保温反应4 h, 冷却至室温析出固体, 过滤、甲醇洗、干燥得橘红色固体0.24 g, 收率93.0%, 纯度99.2%。
1H NMR (DMSO-d6, 500 MHz) δ: 6.810(s, 16H, 2BGH+); 13C NMR (DMSO-d6, 125 MHz) δ: 140.95, 144.78, 160.18; IR (KBr, ν/cm-1): 3457, 3381, 3353, 3130, 1676, 1638, 1579, 1553, 1510, 1486, 1458, 1388, 1370, 1307, 1196, 1100, 857, 810, 754, 699。Anal.Calcd. for C10H16N18O8(%): C 23.26, H 3.12, N 48.83; Found C 23.22, H 3.18, N 48.88。
2.3.7 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑脒基脲盐 (DGUTNBI) 的合成室温下, 向装有温度计、搅拌及冷凝器的25 mL三口瓶中, 依次加入0.175 g (0.5 mmol) TNBI、8.0 mL甲醇、2.0 mL蒸馏水和0.04 g (1 mmol) 氢氧化钠, 搅拌溶解后, 升温至55 ℃, 加入0.165 g (1 mmol) 脒基脲硝酸盐, 在55 ℃保温反应3 h, 冷却至室温析出固体, 过滤、甲醇洗、干燥得黄色固体0.24 g, 收率92.7%, 纯度99.3%。
1H NMR (DMSO-d6, 500 MHz) δ: 7.200(s, 4H, 2C=NH2+), 8.352(s, 8H, 4NH2), 9.685(s, 2H, 2NH); 13C NMR (DMSO-d6, 125 MHz) δ: 140.79, 144.28, 154.98, 155.95; IR (KBr, ν/cm-1): 3466, 3375, 1736, 1703, 1667, 1604, 1530, 1471, 1397, 1382, 1349, 1311, 1264, 1198, 1113, 856, 812, 754, 642。Anal.Calcd. for C10H16N18O8(%): C 23.17, H 2.72, N 43.24; Found C 23.21, H 2.78, N 43.18。
2.3.8 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑4-氨基-1, 2, 4-三唑盐 (DATTNBI) 的合成室温下, 向装有温度计、搅拌及冷凝器的25 mL三口瓶中, 依次加入0.175 g (0.5 mmol) TNBI和10.0 mL甲醇, 搅拌溶解后, 加入0.084 g (1 mmol) 4-氨基-1, 2, 4-三唑, 升温至60 ℃反应3 h, 自然冷却至室温析出固体, 过滤、甲醇洗、干燥得橘红色固体0.23 g, 收率95.4%, 纯度98.9%。
1H NMR (DMSO-d6, 500 MHz) δ: 9.226(s, 4H, 4CH); 13C NMR (DMSO-d6, 125 MHz) δ: 139.32, 140.72, 144.54; IR (KBr, ν/cm-1): 3325, 3242, 3107, 1645, 1523, 1499, 1465, 1395, 1351, 1303, 1265, 1228, 1113, 1075, 1002, 958, 856, 815, 756, 699。Anal.Calcd. for C10H10N16O8(%): C 24.90, H 2.09, N 46.47; Found C 24.94, H 2.13, N 46.41。
2.3.9 4, 4′, 5, 5′-四硝基-2, 2′-联咪唑尿素盐 (DUTNBI) 的合成室温下, 向装有温度计、搅拌及冷凝器的25 mL三口瓶中, 依次加入0.175 g (0.5 mmol) TNBI和5.0 mL甲醇, 搅拌溶解后, 加入0.06 g (1 mmol) 尿素, 升温至40 ℃反应3 h, 冰水浴冷却至0~5 ℃析出固体, 过滤、干燥得黄色固体0.19 g, 收率87.6%, 纯度98.8%。
1H NMR (DMSO-d6, 500 MHz) δ: 7.809(s, 10H, 2UH+); 13C NMR (DMSO-d6, 125 MHz) δ: 138.82, 139.44, 161.04; IR (KBr, ν/cm-1): 3478, 3388, 3050, 1679, 1546, 1496, 1404, 1382, 1349, 1315, 1280, 1118, 994, 853, 813, 751, 677。Anal.Calcd. for C8H10N12O10(%): C 22.13, H 2.32, N 38.71; Found C 22.16, H 2.28, N 38.66。
2.4 TNBI·H2O单晶培养称取1.0 g纯度为99.7%的TNBI自制样品, 将其分散于适量的蒸馏水中, 加热至50 ℃, 使TNBI完全溶解, 得到黄色澄清溶液, 冷却至室温, 过滤出不溶物, 滤液置于干净的锥形瓶中, 室温 (20~25 ℃) 下放置1周后, 得到淡黄色柱状晶体。
2.5 TNBI·H2O晶体结构测定选取尺寸为0.35 mm×0.25 mm×0.13 mm的单晶, 在Smart APEXⅡCCD衍射仪上, 用Mo Kα射线 (λ=0.071073 nm)、石墨单色器。在296(2) K温度下, 以ω扫描方式扫描, 扫描范围: 2.69°≤θ≤25.09°, -6≤h≤6, -10≤k≤8, -18≤ l ≤16, 共收集衍射点3142个, 其中独立衍射点1146个, 选取Ⅰ>2σ(Ⅰ) 的11146个点用于结构测定和修正, 全部数据均经Lp因子和半经验吸收校正, 所有计算均用SHELXTL-97程序包完成。
3 结果与讨论 3.1 TNBI·H2O的晶体结构解析TNBI·H2O晶体的分子结构和分子在晶胞中的堆积分别示于图 1和图 2。

|
图 1 TNBI·H2O的分子结构 Fig.1 Molecular structure of TNBI·H2O |
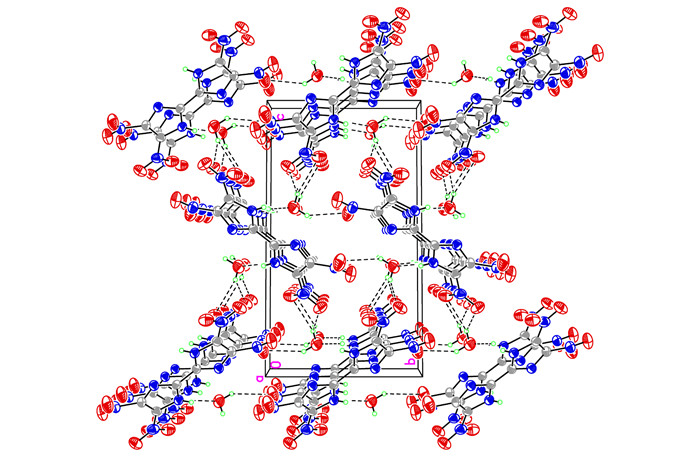
|
图 2 TNBI·H2O的晶胞堆积图 Fig.2 Packing diagram of the unit cell of TNBI·H2O |
晶体分析结果表明, 该晶体为单斜晶系, 空间群为P2(1)/n。晶体学参数为: a=0.5051(17) nm, b=0.8528(3) nm, c=1.5270(5) nm, β=96.948(6)°, V=0.6529(4) nm3, Z=4, Dc=1.781 g·cm-3, μ=0.170 mm-1, F(000)=356。该晶体结构由Patterrson直接法[15]解出, 原子位置均由差值Fourier合成法得到。分子结构用117个参数, 由块矩阵最小二乘法进行优化 (对于氢原子采用各向同性热参数, 对于非氢原子采用各向异性热参数)。对于Ⅰ>2σ(Ⅰ) 数据的最终偏差因子R1=0.0441, wR2=0.0945;对所有数据的偏差因子R1=0.0807, wR2=0.1110, 最佳拟合度s=1.003, 最终差值电子云密度的最高峰为174 e·nm-3, 最低峰为-161 e·nm-3。
分析以上结果可以看出, TNBI分子属于中心对称结构, 由于C (1)—N (3)—C (3)—C (3)#1的二面角为179.5(3)°, C (2)—N (4)—C (3)—C (3)#1的二面角为-179.2(3)°, C (3)—N (3)—C (1)—N (1) 二面角为177.4(2)°, C (3)—N (4)—C (2)—N (2) 二面角为177.3(2)°, N (1)—C (1)—C (2)—N (2) 二面角为5.7(5)°, 故联咪唑环以及四个硝基N原子的所有原子几乎处在同一平面上。在TNBI分子结构中, 联咪唑环和四个硝基之间形成了一个大的离域共轭体系, 从而使该化合物表现出良好的热稳定性。同时, 由于TNBI分子结构中的亚氨基含有活泼氢, 在以水为溶剂培养TNBI单晶时, 由于TNBI和水分子之间存在分子间氢键, 一分子TNBI结合了一分子水 (从晶胞堆积图可以看出), 从而也使该物质的晶体密度小于其实测密度。
3.2 TNBI含能离子盐的热性能研究在动态氮气气氛, 压力0.1 MPa, 温度25~500 ℃, 升温速率10 ℃·min-1, 试样量约0.5~1.0 mg, 试样皿为铝盘的条件下分别研究了七种TNBI有机胺含能离子盐的热性能, 其DSC和TG实验结果分别如图 3、图 4所示。

|
图 3 TNBI含能离子盐的DSC曲线 Fig.3 The DSC curves of TNBI′s energetic ion salts |
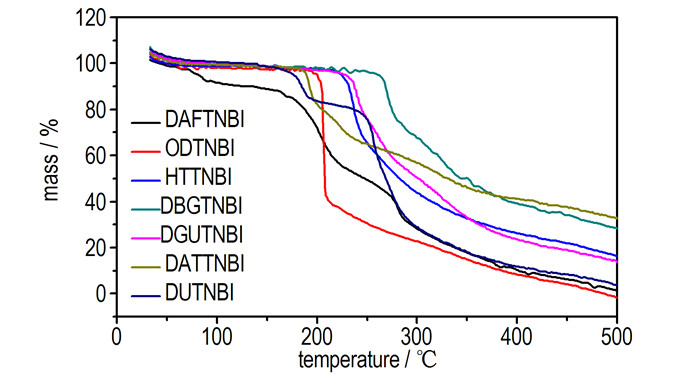
|
图 4 TNBI含能离子盐的TG曲线 Fig.4 The TG curves of TNBI′s energetic ion salts |
从图 3可以看出, 由于TNBI有机胺盐结构中存在体积较大的阴、阳离子部分, 热分解过程可能涉及的官能团比较多, 故部分化合物热分解过程比较复杂, 存在多个放热分解峰。化合物DAFTNBI、DUTNBI分别都有一个明显的吸热峰和至少一个放热峰, 其中依次在171.15, 172.77 ℃处的吸热峰分别为各物质的熔化峰, 即为各物质的熔点; 其中DAFTNBI在88.68 ℃处的吸热峰为该物质结晶水的吸热峰; 在199.23, 260.19 ℃处的放热峰分别为各物质的第一阶段热分解放热峰, 随着温度的升高, 化合物进一步热分解, 表明这些化合物的热分解过程是经历了液相分解过程。而化合物ODTNBI、HTTNBI、DBGTNBI、DGUTNBI、DATTNBI没有明显的吸热峰, 只存在一个或两个明显的放热分解峰, 表明这些物质不存在明确的熔点, 故其后经历的热分解过程是不经过吸热熔化的相变过程, 而是固相直接热分解过程, 在204.52, 230.13, 266.96, 240.63, 187.98 ℃处的放热峰分别为各物质的第一阶段热分解放热峰, 而311.82, 216.64 ℃处的放热峰分别为DBGTNBI和DATTNBI第二阶段热分解放热峰。部分TNBI有机胺含能离子盐的热分解比较复杂, 分解过程存在不止一个热分解峰, 且所有化合物的第一阶段热分解峰温都高于187 ℃, 表明此类化合物的具有较好的热稳定性。
从图 4可知, 合成的TNBI有机含能离子盐化合物 (DAFTNBI除外) 在175 ℃之前, 其热分解累积质量损失均小于5%, 如: ODTNBI、HTTNBI、DBGTNBI、DGUTNBI、DATTNBI和DUTNBI在200.00, 224.14, 260.13, 228.45, 190.09, 177.80 ℃处的累积质量损失分别为4.72%,4.57%,4.71%,4.87%,4.88%,4.72%, 热分解质量损失较小, 表明上述化合物在175 ℃之前的热稳定性较好, 且化合物DAFTNBI、DBGTNBI、DATTNBI和DUTNBI都存在两个热失重过程, 经历了至少两个热分解阶段; 从图 4还可以看出, 所有化合物的最大热分解失重峰温都在200 ℃以上, 随着温度的继续升高, 各个物质进一步分解, 最后剩余一定量难以分解的“残渣”。
4 结论(1) 改进了4, 4′, 5, 5′-四硝基-2, 2′-联咪唑 (TNBI) 的合成工艺, 以80%硝酸/浓硫酸体系代替文献的硝酸钠/尿素/浓硫酸体系, 反应温度由85~90 ℃降低到45 ℃、反应时间从16 h缩短至4 h, 反应过程平稳温和, 为其进一步工艺放大奠定基础。
(2) 以自制的TNBI为原料, 合成了TNBI的二氨基呋咱盐 (DAFTNBI)、草酰肼盐 (ODTNBI)、二肼基四嗪盐 (HTTNBI)、缩二胍盐 (DBGTNBI)、脒基脲盐 (DGUTNBI)、4-氨基-1, 2, 4-三唑盐 (DATTNBI)、尿素盐 (DUTNBI) 等七种新型含能离子盐, 收率分别为71.4%,83.3%,96.5%,93.0%,92.7%,95.4%和87.6%。
(3) 获得了TNBI·H2O单晶, 晶体结构解析表明, TNBI·H2O为单斜晶系, 空间群为P2(1)/n, TNBI分子结构中联咪唑环及四个硝基彼此间形成一个大的离域共轭体系。
(4) 采用差示扫描量热 (DSC)、热重 (TG) 研究了TNBI七种含能离子盐的热性能, 结果表明, 此类化合物具有较好的热稳定性, 所有化合物的第一阶段热分解峰温均高于187 ℃。
| [1] | Zhang Y, Parrish D A, Shreeve J M. 4-Nitramino-3, 5-dinitropyrazole-based energetic salts[J]. Chemistry-A European Journal, 2012, 18: 987-994. DOI:10.1002/chem.v18.3 |
| [2] | Huang Y, Zhang Y, Shreeve J M. Nitrogen-rich salts based on energetic nitroaminodiazido 1, 3, 5-triazine and guanazine[J]. Chemistry-A European Journal, 2011, 17: 1538-1546. DOI:10.1002/chem.v17.5 |
| [3] | HUO Huan, WANG Bo-zhou, ZHAI Lian-jie, et al. An insensitive energetic compound 5, 7-diamino-4, 6-dinitrobenzotriazol-3-ium-1-oxide: synthesis, characterization and performances[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2016, 24(9): 857-861. |
| [4] |
吴军鹏, 曹端林, 王建龙, 等. 3, 4, 5-三硝基吡唑及其衍生物的研究进展[J].
含能材料, 2016, 24(11): 1121-1130. WU Jun-peng, CAO Duan-lin, WANG Jian-long, et al. Progress on 3, 4, 5-trinitro-1H-pyrazole and its derivatives[J]. Chinese Journal of Energetic Materials (Hanneng Cailiao), 2016, 24(11): 1121-1130. DOI:10.11943/j.issn.1006-9941.2016.11.016 |
| [5] | Liu L, Zhang Y, Zhang S, Fei T. Heterocyclic energetic salts of 4, 4′, 5, 5′-tetranitro-2, 2′-biimidazole[J]. Journal of Energetic Materials, 2015, 33: 202-214. DOI:10.1080/07370652.2014.970246 |
| [6] | Cromer D T, Storm C B. Structure of 4, 4′, 5, 5′-Tetranitro-2, 2′-biimidazole dihydrate[J]. Acta Crystallogr, Sect C: Cryst Struct Commun, 1990, 46: 1957-1958. DOI:10.1107/S0108270189013843 |
| [7] | Cromer D T, Storm C B. Structure of thediammonium salt of 4, 4′, 5, 5′-tetranitro-2, 2′-biimidazole, C6N8O8·2NH4[J]. Acta Crystallogr, Sect C: Cryst Struct Commun, 1990, 46: 1959-1960. DOI:10.1107/S0108270190004292 |
| [8] | Cho S G, Cho J R, Goh E M, et al. Synthesis and characterization of 4, 4′, 5, 5′-tetranitro-2, 2′-bi-1H-imidazole (TNBI)[J]. Propellants, Explosives, Pyrotechnics, 2005, 30(6): 445-449. DOI:10.1002/(ISSN)1521-4087 |
| [9] | Cho S G, Goh E M, Cho J R, et al. Theoretical studies on molecular and explosive properties of 4, 4′, 5, 5′-tetranitro-2, 2′-bi-1H-imidazole (TNBI)[J]. Propellants, Explosives, Pyrotechnics, 2006, 31(1): 33-37. DOI:10.1002/(ISSN)1521-4087 |
| [10] | Chavez D E, Parrish D, Preston D N, et al. Synthesis and energetic properties of 4, 4′, 5, 5′-tetranitro-2, 2′-biimidazolate (N4BIM) salts[J]. Propellants, Explosives, Pyrotechnics, 2012, 37: 647-652. DOI:10.1002/prep.201200040 |
| [11] | Klap tke T M, Preimesser A, Stierstorfer J. Energetic derivatives of 4, 4′, 5, 5′-tetranitro-2, 2′-bisimidazole (TNBI)[J]. Z Anorg Allg Chem, 2012, 638(9): 1278-1286. DOI:10.1002/zaac.201200188 |
| [12] | Kim S H, Kim J S. High nitrogen energetic salts of 4, 4′, 5, 5′-tetranitro-2, 2′-biimidazole[J]. Bull Korean Chem Soc, 2013, 34(8): 2503-2506. DOI:10.5012/bkcs.2013.34.8.2503 |
| [13] | Lewczuk R, Wasilewska M, Szala M. Synthesis and properties of some new salts of 4, 4′, 5, 5′-tetranitro-2, 2′-bi-1H-imidazole[C]//New Trends in Research of Energetic Materials, Pardubice, Czech Republic, April, 2014: 825-810. |
| [14] | Paraskos A J, Cooke E D, Caflin K C. Bishydrazinium and diammonium salts of 4, 4′, 5, 5′-tetranitro-2, 2′-biimidazolate (TNBI): synthesis and properties[J]. Propellants, Explosives, Pyrotechnics, 2015, 40: 46-49. DOI:10.1002/prep.v40.1 |
| [15] | Sheldrick G M. SHELXS-97, Program for Crystal Structure Solution[CP], University of G ttingen, Germany, 1997. |
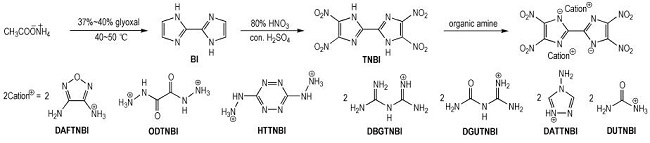
4, 4′, 5, 5′-Tetranitro-2, 2′-biimidazole and its energetic ion salts were synthesized. The structures of all compounds were confirmed by IR, 1H NMR, 13C NMR and elemental analysis. The single crystal of TNBI·H2O was obtained in the water system. The thermal properties of seven energetic ion salts were studied.



