2. 氟氮化工资源高效开发与利用国家重点实验室, 陕西 西安 710065
2. State Key Laboratory of Fluorine & Nitrogen Chemicals, Xi′an 710065, China
高能量密度材料(HEDM)是武器系统的毁伤威力来源和动力能源, 可提高推进剂、炸药和发射药的能量, 在各类武器系统中发挥着至关重要的作用[1-4]。近年来, 呋咱类含能化合物因其具有能量密度高、标准生成焓大、熔点低、氢含量少(或者无氢)、氧含量高等特点, 受到世界各国含能材料研究者的高度关注[5-8]。相比于呋咱或异呋咱, 氧化呋咱结构单元具有更为优异的综合性能, 如更高的生成焓以及更高的氧平衡。实验研究发现, 一个氧化呋咱基代替一个硝基, 可使化合物的密度提高0.06~0.08 g·cm-3, 相应的爆速可提高300 m·s-1以上[9-12]。其中最具有代表性是3, 3′-二硝基-4, 4′-偶氮氧化呋咱, 其熔点为128 ℃, 密度为2.002 g·cm-3, 生成焓ΔH f为667.8 kJ·mol-1, 实测爆速大于10000 m·s-1, 是继六硝基六氮杂异伍兹烷(CL-20) 之后的又一种新型高能炸药。但由于其合成路线长、收率低、感度高等缺点, 限制了其在武器装备中大规模应用[13-14]。
3-氰基-4-硝基氧化呋咱具有典型氧化呋咱结构单元, 引入硝基使得该化合物分子能量、氧含量进一步提高, 引入氰基能够大大增加化合物分子稳定性以及降低感度。Kulikov等人[15]首次报道了其合成方法, 该方法以乙酰乙酸乙酯为原料, 经过六步反应得到3-氰基-4-硝基氧化呋咱, 反应总收率仅为6.0%。该方法反应步骤长, 后处理繁琐, 且反应收率低。
基于此,本研究以丙二腈为原料, 经重氮化、氰基加成、氧化四步合成了3-氰基-4-硝基氧化呋咱, 采用红外、碳谱、氮谱对其结构进行了表征, 确定了环外配位氧原子位置。同时在6-31+G(d, p)基组水平上优化了其几何构型, 采用Kamlet-Jacbos方程预估了爆速和爆压。
2 实验部分 2.1 实验仪器与试剂NEXUS870型傅里叶变换红外光谱仪, 美国热电尼高力公司; AV500型(500 MHz)超导核磁共振仪, 瑞士BRUKER公司; Vario EL-Ⅲ型元素分析仪, 德国EXEMENTAR公司; LC-2010A液相色谱仪, 日本岛津公司; X-6型显微熔点测定仪, 北京泰克仪器有限公司; Q-200型差示扫描量热仪, 美国TA公司。
浓硫酸, 30%双氧水, 分析纯, 西安福晨化学仪器有限公司; 丙二腈, 亚硝酸钠, 盐酸羟胺, 二水合钨酸钠, 均为分析纯, 天津化学试剂有限公司; 冰醋酸, 乙醚, 二氧化铅, 均为化学纯, 成都科龙化学试剂厂。
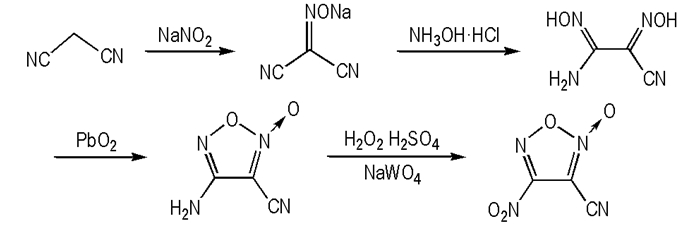
2.2 实验原理合成路线见Scheme 1。
|
Scheme1 Synthetic route of 3-cyano-4-nitrofuroxan |
丙二腈肟钠盐以及1-氨基-2-氰基二肟依据文献[16]合成。
2.3.1 3-氰基-4-氨基氧化呋咱的合成室温下, 将5.3 g (42 mmol)1-氨基-2-氰基二肟加入到125 mL乙醚和10 mL乙酸的混合溶液中, 搅拌均匀后分批加入35 g (146 mmol)二氧化铅, 升温到35 ℃并保温反应。薄层色谱法监测反应, 直到原料消失后, 过滤除去滤饼, 滤液用冰水洗至中性。然后将乙醚蒸干最后得淡黄色固体2.9 g, 收率55.1%, 纯度97.4%。m.p.: 116~117 ℃; 1H NMR (DMSO-d6, 500 MHz), δ: 6.55 (s, 2H, NH2); 13C NMR (DMSO-d6, 125 MHz), δ:156.66(C—NH2), 106.93 (C≡N), 95.65(C—CN); IR (KBr, ν/cm-1): 3400, 3322, 3248, 3189, 2253, 1637, 1595, 1567, 1489, 1412, 1167, 1002, 854, 775, 676; Anal.Calcd. for C3H2N4O2(%): C 28.58, N 44.44, H 1.60; Found C 28.32, N 44.17, H 1.96。
2.3.2 3-氰基-4-硝基氧化呋咱的合成-5 ℃下, 将39 g(390 mmol)浓硫酸缓慢滴加到钨酸钠二水合物3.3 g(10 mmol)和30%双氧水31 g(489 mmol)中, 加入完毕后升温至25 ℃, 再分批加入3-氰基-4-氨基氧化呋咱1.80 g(14.2 mmol), 加完后在30 ℃保温反应2.5 h。然后中止反应, 降至15 ℃后, 用二氯甲烷(25 mL)萃取并水洗3次, 随后用无水硫酸镁干燥、过滤, 滤液经减压蒸馏得3-氰基-4-硝基氧化呋咱1.86 g, 收率83.8%, 纯度99.4%。m.p.: 49 ℃; 13C NMR (DMSO-d6, 125 MHz), δ: 155. 00 (C—NO2), 102.01(C≡N), 92.5(C—CN); 15N NMR (DMSO-d6), δ: -9.94, -15.96, -41.84, -92.01; IR (KBr, ν/cm-1): 2258, 1667, 1582, 1526, 1359, 1279, 1081, 1050, 815; Anal.Calcd. for C3N4O4(%): C 23.09, N 35.90; Found C 23.05, N 35.68。
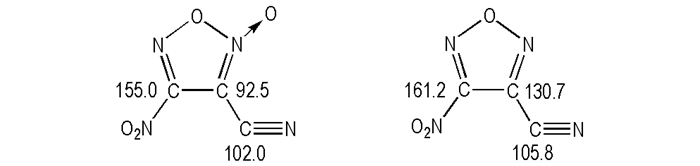
3 结果与讨论 3.1 13C和15N核磁谱对于不对称氧化呋咱分子, 确定环外配位氧原子的位置具有一定难度。某些氧化呋咱化合物, 如3-氨基-4-硝基氧化呋咱, 在某些有机溶剂中会自动发生异构化反应, 生成一定量的3-硝基-4-氨基氧化呋咱[17]。在没有晶体结构的情况下, 核磁谱是判断环外配位氧原子位置的有效途径。通过与3-氰基-4-硝基呋咱碳谱对比研究[18], 化学位移在δ 102.0处为3-氰基-4-硝基氧化呋咱中氰基信号峰(Scheme 2), 氧化呋咱环对其影响较小; 与硝基相连的碳原子化学位移出现在δ 155.0, 相比3-氰基-4-硝基呋咱产生了一定的影响; 而变化最大是与氰基相连的碳, 其化学位移是δ 92.5, 由此也可以判断氧化呋咱环外氧原子在氰基这一侧。
|
Scheme2 Comparative study on 13C chemical signals |
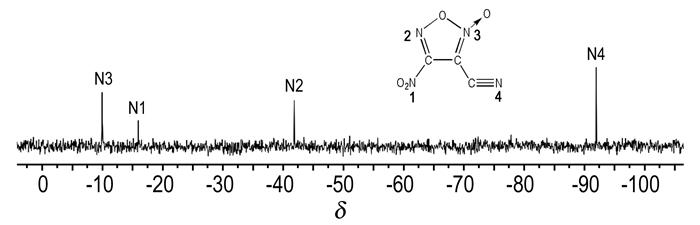
另外, 由于目标分子具有较好的溶解性, 研究了其在氘代二甲基亚砜溶液中的15N谱图特征。根据文献中类似化合物分子结构对3-氰基-4-硝基氧化呋咱氮谱进行了归属[19-20], 如图 1所示。从中可以清楚观察到四条谱线, 且为单峰, 这与分子结构一致。氧化呋咱环上氮原子信号峰分别在δ -9.94, -41.84处, 硝基和氰基分别出在δ -15.96, -92.01处。
|
图 1 3-氰基-4-硝基氧化呋咱在氘代二甲基亚砜溶液中15N谱 Fig.1 15N spectrum of compound 3-cyano-4-nitrofuroxan in DMSO-d6 |
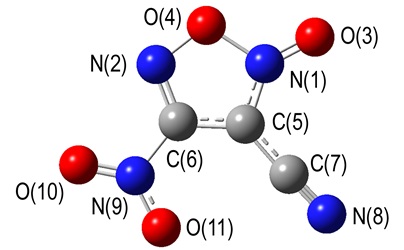
采用密度泛函理论(DFT)的B3LYP方法[21], 在6-31+G(d, p)基组水平上对3-氰基-4-硝基氧化呋咱的结构进行了全优化, 经振动频率分析发现无虚频, 表明优化结构为势能面上的极小点, 为稳定构型。优化后的几何构型及原子编号见图 2, 键长、键角和二面角数据见表 1。
|
图 2 3-氰基-4-硝基氧化呋咱优化几何构型 Fig.2 The optimized geometry of 3-cyano-4-nitrofuroxan |
| 表 1 3-氰基-4-硝基氧化呋咱的几何构型及键级 Tab.1 The optimized geometries and bond order of 3-cyano-4-nitrofuroxan |
由表 1可见, 目标分子中硝基以及氰基键长处于正常的N═O双键、C≡N三键范围内; 硝基、氰基与氧化呋咱环均处于同一平面, 说明硝基和氰基与氧化呋咱环共轭效应明显, 有助于增加分子的稳定。而氧化呋咱环上的N(1)—O(4) 和N(2)—O(4) 键长分别为1.48 Å和1.35 Å, N(1)—O(4) 键长显著长于一般N—O单键; 环外N(1)—O(3) 键长则处于氮氧双键键长范围内, 正是由于环外N═O双键影响, 致使氧化呋咱环内氮氧单键差别较大。对优化构型进行自然键级轨道(NBO)分析, 得到的C、H、N和O之间的键级(表 1)。由表 1可知, 3-氰基-4-硝基氧化呋咱分子中键级最小键分别为N(1)—O(4) (0.84) 和C(6)—N(9) (0.91), 说明该键最易断裂, 引发分解, 这与键长数据一致。
3.2.2 爆轰性能预估在B3LYP/6-31+G(d, p)水平优化构型基础上, 用Monte-Carlo法[22]计算分子体积, 为了减小误差, 取100次计算值的平均值为3-氰基-4-硝基氧化呋咱的摩尔体积(Vm), 得Vm =89.47 cm3, 进而求得其理论密度为1.74 g·cm-3。使用原子化方案[23], 利用完全基组方法(CBS-4M)[24]计算了298 K时3-氰基-4-硝基氧化呋咱的焓H° (Molecule, 298 K), 进而求得算得气相生成焓为439.1 kJ·mol-1。利用静电势参数和Politzer等[25]提出的公式计算了3-氰基-4-硝基氧化呋咱的升华焓ΔHsub (86.5 kJ·mol-1), 进而求得固相生成焓ΔfH (s, M, 298 K)为352.6 kJ·mol-1。
采用Kamlet-Jacbos[26]公式预估了3-氰基-4-硝基氧化呋咱的爆速与爆压, 并与增塑剂三羟甲基乙烷三硝酸酯(TMETN)做了对比, 结果见表 2。由表 2可知, 目标化合物(TM)密度、爆速和爆压均优于TMETN。
| 表 2 3-氰基-4-硝基氧化呋咱的物化性能 Tab.2 Physical properties of 3-cyano-4-nitrofuroxan |
(1) 以丙二腈为原料, 经重氮化、氰基加成、环化、氧化合成了3-氰基-4-硝基氧化呋咱, 其中环化和氧化两步收率分别为55.1%和83.8%, 并通过红外、核磁、元素等分析方法进行了表征。
(2) 探讨了3-氰基-4-硝基氧化呋咱13C和15N谱, 通过与3-氰基-4-硝基呋咱对比研究确定了配位氧原子在氰基一侧; 分析了目标分子15N谱, 完成了分子中N信号的全归属。
(3) 通过量子化学手段研究计算其固相生成焓为352.6 kJ·mol-1, 密度1.74 g·cm-3, 爆速8352.0 m·s-1, 爆压30.9 GPa, 是一种具有较高能量水平的化合物, 有望作为增塑剂使用。
| [1] |
董海山. 高能量密度材料的发展及对策[J].
含能材料, 2004, 12(增刊): 1-12. DONG Hai-shan. The development and countermeasure of high energy density materials[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2004, 12(Suppl.): 1-12. |
| [2] |
张德雄, 张衍, 王伟平, 等. 高能量密度材料(HEDM)研究开发现状及展望[J].
固体火箭技术, 2005, 28(4): 284-288. ZHANG De-xiong, ZHANG Yan, WANG Wei-ping, et al. Present status and prospects of high energy density materials[J]. Journal of Solid Rocket Technology, 2005, 28(4): 284-288. |
| [3] |
张志忠, 王伯周, 姬月萍, 等. 部分新型高能量密度材料的国内研究进展[J].
火炸药学报, 2008, 31(2): 93-98. ZHANG Zhi-zhong, WANG Bo-zhou, JI Yue-ping, et al. Study progress of several high energy density materials(HEDM)[J]. Chinese Journal of Explosives & Propellants, 2008, 31(2): 93-98. |
| [4] | Badgujar D M, Talawar M B, Asthana S N, et al. Advances in science and technology of modern energetic materials: an overview[J]. Journal of Hazardous Materials, 2008, 151(2): 289-305. |
| [5] |
李战雄, 唐松青, 欧育湘, 等. 呋咱含能衍生物合成研究进展[J].
含能材料, 2002, 10(2): 59-65. LI Zhan-xiong, TANG Song-qin, OU Yu-xiang, et al. Synthesis status of furazano energetic derivatives[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2002, 10(2): 59-65. |
| [6] |
张德雄, 张衍, 王琦. 呋咱系列高能量密度材料的发展[J].
固体火箭技术, 2004, 27(1): 32-36. ZHANG De-xiong, ZHANG Yan, WANG Qi. Advances in high energy density matter of furazan series[J]. Journal of Solid Rocket Technology, 2004, 27(1): 32-36. |
| [7] | Pivina T S, Sukhachev D V, Evtushenko A V. Comparative characteristic of energy content calculating methods for the furazan series as an example of energetic materials[J]. Propellants, Explosives, Pyrotechnics, 1995, 20(1): 5-10.DOI:10.1002/(ISSN)1521-4087 |
| [8] |
王锡杰, 廉鹏, 葛忠学, 等. 3, 3′-二硝基双呋咱醚(FOF-1) 合成、晶体结构及理论研究[J].
化学学报, 2010, 68(6): 557-563. WANG Xi-jie, LIAN Peng, GE Zhong-xue, et al. Synthesis, crystal structure and theoretical research of 3, 3′-dinitrodifurazanyl ether(FOF-1)[J]. Acta Chim Sinica, 2010, 68(6): 557-563. |
| [9] | ZHAI Lian-jie, FAN Xue-zhong, WANG Bo-zhou, et al. Facial synthesis and crastal structure of 3, 4-bis(1H-tetrazolyl)furoxan[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2015, 23(12): 1172-1175. |
| [10] | LIANG Li-xuan, WANG Kai, BIAN Cheng-ming, et al. 4-Nitro-3-(5-tetrazole)furoxan and its salts: synthesis, characterization, and energetic properties[J]. Chemistry-A European Journal, 2013, 19(44): 14902-14910.DOI:10.1002/chem.201301042 |
| [11] | Fischer D, Klapötke T M, Stierstorfer J. Synthesis and characterization of diaminobisfuroxane[J]. European Journal of Inorganic Chemistry, 2014(34): 5808-5811. |
| [12] | HE Chun-lin, Shreeve J M. Potassium 4, 5-bis(dinitromethyl)furoxanate: a green primary explosive with a positive oxygen balance[J]. Angewandte Chemie International Edition, 2016, 55(2): 772-775.DOI:10.1002/anie.201509209 |
| [13] |
何金选, 卢艳华, 雷晴, 等. 3, 3′-二硝基-4, 4′-偶氮氧化呋咱的合成及性能[J].
火炸药学报, 2011, 34(5): 9-12. HE Jin-xuan, LU Yan-hua, LEI Qing, et al. Synthesis and properties of high energetic compound 3, 3, -dinitro-4, 4′-azofuroxan[J]. Chinese Journal of Explosives & Propellants, 2011, 34(5): 9-12. |
| [14] |
洪伟良, 田德余, 刘剑洪, 等. 含二硝基偶氮氧化呋咱推进剂的能量特性研究[J].
固体火箭技术, 2001, 24(2): 41-44. HONG Wei-liang, TIAN De-yu, LIU Jian-hong, et al. Study on the energy characteristic of propellant containing dinitroazofuroxan[J]. Journal of Solid Rocket Technology, 2001, 24(2): 41-44. |
| [15] | Kulikov A S, Ovchinnikov I V, Molotov S I, et al. Synthesis of furoxan derivatives based on 4-aminofuroxan-3-carboxylic acid azide[J]. Russian Chemical Bulletin, International Edition, 2003, 52(8): 1822-1828.DOI:10.1023/A:1026073108494 |
| [16] |
罗义芬, 马玲, 王伯周, 等. 3, 3′-二氰基-4, 4′-偶氮氧化呋咱合成与表征[J].
含能材料, 2010, 18(5): 538-540. LUO Yi-fen, MA Ling, WANG Bo-zhou, et al. Synthesis and characterization of 3, 3′-dicyano-4, 4′-azofuroxan[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2010, 18(5): 538-540. |
| [17] | Godovikova T I, Rakitin O A, Golova S P, et al. 3, 4-Dinitrofuroxan-the first example of a pernitro heterocycle[J]. Mendeleev Communications, 1993, 3(5): 209-210.DOI:10.1070/MC1993v003n05ABEH000296 |
| [18] |
范艳杰, 王伯周, 来蔚鹏, 等. 3, 3′-二氰基二呋咱基醚(FOF-2) 的合成、表征及量子化学研究[J].
有机化学, 2009, 29(4): 614-620. FAN Yan-jie, WANG Bo-zhou, LAI Wei-peng, et al. Synthesis, characterization and quantum chemistry study on 3, 3′-dicyan-difurazanyl ether (FOF-2)[J]. Chinese Journal of Organic Chemistry, 2009, 29(4): 614-620. |
| [19] | Fischer D, Klapötke T M, Reymann M. Energetic alliance of tetrazole-1-oxides and 1, 2, 5-oxadiazoles[J]. New Journal Chemistry, 2015, 8(3): 1619-1627. |
| [20] | Dippold A A, Izsak D, Klapötke T M, et al. Combining the advantages of tetrazoles and 1, 2, 3-Triazoles: 4, 5-bis(tetrazol-5-yl)-1, 2, 3-triazole, 4, 5-bis(1-hydroxytetrazol-5-yl)-1, 2, 3-triazole, and their energetic derivatives[J]. Chemistry-A European Journal, 2016, 22(5): 1768-1778.DOI:10.1002/chem.201504624 |
| [21] | Becke A D. Density-functional thermochemistry. Ⅲ. The role of exact exchange[J]. Journal of Chemical Physics, 1993, 98(7): 5648-5652.DOI:10.1063/1.464913 |
| [22] | Rice B M, Hare J J, Byrd E F E. Accurate predictions of crystal densities using quantum mechanical molecular volumes[J]. Journal of Chemical Physics A, 2007, 111(42): 10874-10879.DOI:10.1021/jp073117j |
| [23] | Curtiss L A, Raghavachari K, Redfern P C, et al. Assessment of Gaussian-2 and density functional theories for the computation of enthalpies of formation[J]. Journal of Chemical Physics, 1997, 106(3): 1063-1079.DOI:10.1063/1.473182 |
| [24] | Ochterski J W, Petersson G A, Montgomery J A. A complete basis set model chemistry V. extension to six or more heavy atoms[J]. Journal of Chemical Physics, 1996, 104(7): 2598-2679.DOI:10.1063/1.470985 |
| [25] | Politzer P, Murray J S, Grice M E, et al. Calculation of heats of sublimation and solid phase heats of formation[J]. Molecular Physics, 1997, 91(5): 923-928.DOI:10.1080/002689797171030 |
| [26] | Kamlet M J, Jacobs S J. Chemistry of detonation Ⅰ. a simple method for calculating detonation properties of CHNO explosives[J]. Journal of Chemical Physics, 1968, 48(1): 23-35.DOI:10.1063/1.1667908 |




