近年来,氮杂芳环化合物(如吡唑、咪唑、三唑、四唑、三嗪、四嗪、呋咱等)因具有高氮含量、高生成焓、产气量大、爆轰产物清洁等优点,成为各国含能材料研究者普遍关注的热点之一[1-5]。由于此类高氮化合物分子中所含氮、氧原子的电负性较高、大多具有未使用的孤电子对,从而使整个杂环体系容易形成类似苯环的大л键共轭结构。因此,具有热稳定性好、对摩擦、撞击刺激钝感等特点,国内外研究者已经设计并合成出多种富氮杂环含能化合物,大多具有较好的爆轰性能[6-10]。氟偕二硝甲基基团作为一种非常重要的新型高能量密度含能官能团,已应用于多种含能化合物的分子结构设计与合成中,含有该官能团的化合物大多具有较好的热稳定性和较低的感度,和传统含偕二硝甲基官能团的含能化合物相比,含氟偕二硝甲基基团的化合物大多具有较高的密度、适宜的感度、较高的氧平衡和良好的爆轰性能[11-12]。因此,将富氮的三唑环引入分子结构中,可以增加化合物的氮含量; 而将氟偕二硝甲基基团引入分子结构中,可以有效改善化合物的密度和氧平衡,提升含能化合物的爆轰性能。
基于此,本研究以3-氰基-1, 2, 4-三唑为原料,设计并合成了未见文献报道的新型含能化合物——3-氟偕二硝甲基-1, 2, 4-三唑(FDNMT),优化并确定了肟化反应的适宜条件; 采用Gaussian 09程序[13]中的CBS-4M方法和Kamlet-Jacobs爆轰方程[14]预估了目标化合物的爆轰性能,为进一步开展此类化合物的设计、合成提供借鉴。
2 实验部分 2.1 试剂与仪器五氧化二氮,自制; 3-氰基-1, 2, 4-三唑,化学纯,济南伟都化工试剂有限公司; 盐酸羟胺、氢氧化钠、亚硝酸钠、碘化钾、二氯甲烷、三氯甲烷、甲醇、乙腈,分析纯,成都市科龙化工试剂厂; 浓盐酸(36%~38%),工业级,西安福晨化学试剂有限公司。
ZF-Ⅱ型三用紫外仪,上海市安亭电子仪器厂; NEXUS 870型傅里叶变换红外光谱仪,美国热电尼高力公司; AV500型(500MHz)超导核磁共振仪,瑞士BRUKER公司; GCMS-QP2010型质谱仪,日本岛津公司; VARIO-EL-3型元素分析仪,德国EXEMENTAR公司; LC-2010A型高效液相色谱仪(归一化法),日本岛津公司; SMART APEX Ⅱ CCD X-射线单晶衍射仪,德国Bruker公司。
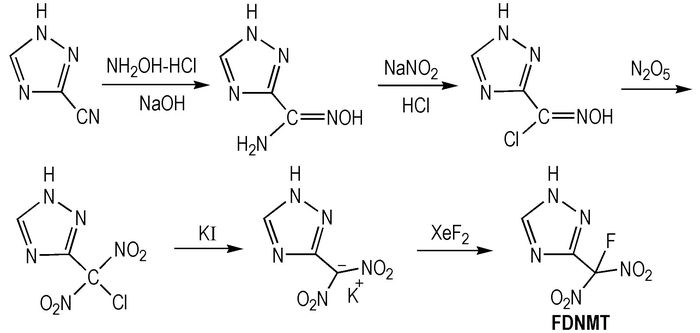
2.2 合成路线以3-氰基-1, 2, 4-三唑和盐酸羟胺为原料,经肟化、重氮化-氯化、硝解、还原、氟化等反应合成了3-氟偕二硝甲基-1, 2, 4-三唑,合成路线如Scheme 1所示。
|
Scheme1 Synthetic route of FDNMT |
搅拌下,将10.0 g(0.106 mol) 3-氰基-1, 2, 4-三唑加入100.0 mL去离子水中,分批加入9.6 g(0.138 mol)盐酸羟胺,用30%(质量分数)的氢氧化钠水溶液将反应液的pH值调节至8,在70~75 ℃反应2.5 h,冷却、过滤反应液、水洗滤饼至中性,干燥滤饼得白色固体3-偕氨基羟亚氨基甲基-1, 2, 4-三唑6.6 g,收率为48.8%,纯度为99.1%(HPLC)。
1H NMR(DMSO-d6, 500 MHz) δ: 5.831(s, 2H, NH2), 8.323(s, 1H, CH), 9.956(s, 1H, NH), 14.281(s, 1H, OH); 13C NMR(DMSO-d6, 125 MHz) δ: 143.79(s), 147.76(s), 151.84 (s); IR(KBr, ν/cm-1): 3472, 3453, 3360, 3336, 3143, 1655, 1472, 1390, 1292, 1151, 932; Anal.calcd for C3H5N5O(%): C 28.35, H 3.96, N 55.10; found C 28.37, H 4.01, N 55.29; MS(EI) m/z: 127[M+]。
2.3.2 3-偕氯羟亚氨基甲基-1, 2, 4-三唑的合成搅拌下,将4.0 g(0.031 mol)3-偕胺肟基-1, 2, 4-三氮唑加入9.5 mL浓盐酸和30 mL蒸馏水的混合溶液中,缓慢加热使其完全溶解,然后将反应液冷却到5 ℃以下析出白色粉晶,滴加2.1 g(0.031 mol)亚硝酸钠水溶液,过程中加入0.5 mL CH2Cl2消泡,然后在5 ℃以下保持反应3.0 h,升温到30 ℃反应1.5 h,冷却、过滤、水洗至中性,干燥得白色固体3-偕氯羟亚氨基甲基-1, 2, 4-三唑3.6 g,收率为78.1%,纯度98.9%(HPLC)。
1H NMR(DMSO-d6, 500 MHz) δ: 8.604(s, 1H, CH), 12.605(s, 1H, NH), 14.408(s, 1H, OH); 13C NMR(DMSO-d6, 125 MHz) δ: 128.36, 145.95, 154.79; IR(KBr, ν/cm-1): 3237, 1619, 1477, 1370, 1279, 1040, 937, 748; Anal.calcd for C3H3N4OCl(%): C 24.59, H 2.064, N 38.23; found C 24.79, H 2.050, N 37.70; MS(ESI-) m/z:145, 147[M-H]-。
2.3.3 3-氯偕二硝甲基-1, 2, 4-三唑的合成搅拌下,依次将1.5 g(0.01 mol) 3-偕氯肟基-1, 2, 4-三唑、75.0 mL三氯甲烷加入到烧瓶中,分批加入1.5 g(0.053 mol)五氧化二氮,加完后升温至45 ℃反应45 min,减压蒸除三氯甲烷,干燥得3-氯偕二硝甲基-1, 2, 4-三唑1.95 g,收率为91.9%,纯度为98.6%(HPLC)。
1H NMR(DMSO-d6, 500 MHz) δ: 8.988(s, 1H, CH), 9.114(s, 1H, NH); 13C NMR(DMSO-d6, 125 MHz) δ: 144.49, 147.49, 153.09; IR(KBr, ν/cm-1): 3152, 3103, 3025, 1537, 1476, 1385, 1348, 1326, 1279, 1052; Anal.calcd for C3H2N5O4Cl(%): C 17.36, H 0.97, N 33.75; found C 17.33, H 0.92, N 33.80; MS(ESI-) m/z: 206, 208[M-H]-。
2.3.4 3-偕二硝甲基-1, 2, 4-三唑钾盐的合成搅拌下,依次将0.5 g(2.4 mmol) 3-氯偕二硝甲基-1, 2, 4-三唑、10.0 mL甲醇加入到烧瓶中,滴加10.0 mL含1.0 g(6.0 mmol)碘化钾的甲醇溶液,加完后在25 ℃反应1 h,过滤、甲醇洗、干燥得3-偕二硝甲基-1, 2, 4-三唑钾盐0.31 g,收率为61.0%,纯度为98.8%(HPLC)。
1H NMR(D2O-d2, 500 MHz) δ: 8.503(s, 1H, CH); 13C NMR(D2O-d2, 125 MHz) δ: 126.90, 146.17, 150.91; IR(KBr, ν/cm-1): 3150, 3097, 2879, 1538, 1520, 1463, 1377, 1359, 1323, 1243, 1099; Anal.calcd for C3H2N5O4K(%): C 17.06, H 0.95, N 33.16; found C 17.13, H 0.91, N 33.22; MS(ESI-) m/z: 172[M-K]-。
2.3.5 3-氟偕二硝甲基-1, 2, 4-三唑(FDNMT)的合成搅拌下,依次将0.15 g(0.71 mmol)3-偕二硝甲基-1, 2, 4-三唑钾盐、8.0 mL乙腈加入到烧瓶中,然后分批向体系中加入0.25 g(1.49 mmol)二氟化氙,加完后在25 ℃保持反应48 h,过滤,滤液蒸干溶剂、干燥得3-氟偕二硝甲基-1, 2, 4-三唑0.077 g,收率为56.6%,纯度为98.0%(HPLC)。
1H NMR(DMSO-d6, 500 MHz) δ: 8.961(s, 1H, CH), 9.061(s, 1H, NH); 13C NMR(DMSO-d6, 125 MHz) δ: 124.68, 147.18, 153.09; 19F NMR(DMSO-d6, 470.5MHz) δ: -95.25; IR(KBr, ν/cm-1): 3142, 2908, 1520, 1463, 1348, 1314, 1267, 1052; Anal.calcd for C3H2N5O4F(%): C 18.86, H 1.06, N 36.65; found C 18.83, H 1.11, N 36.72; MS(ESI-) m/z: 190[M-H]-。
2.4 FDNMT的单晶培养称取0.1 g纯度大于98.0%的3-氟偕二硝甲基-1, 2, 4-三唑样品,将其分散于适量的无水乙腈中,加热至40℃使其完全溶解,得到无色澄清溶液,冷却至室温,过滤出不溶物,滤液置于干净的烧杯中,室温(20~25 ℃)下缓慢挥发7天,得到无色晶体,挑选合适尺寸的单晶颗粒进行晶体结构测试。
2.5 FDNMT晶体结构测定选取尺寸为0.33 mm×0.26 mm×0.14 mm的单晶,在Smart APEXⅡCCD衍射仪上,用Mo Kα射线(λ=0.71073 nm)、石墨单色器。在296(2) K温度下,以ω扫描方式扫描,扫描范围: 1.05°≤θ≤25.10°,-8≤h≤8,-11≤k≤11,-46≤l≤41,共收集衍射点12967个,其中独立衍射点2522个,选取I>2σ(I)的2522个点用于结构的测定和修正,全部数据均经Lp因子和半经验吸收校正,所有计算均用SHELXTL—97程序包[15]完成。
3 结果与讨论 3.1 合成条件优化在碱性条件下,3-氰基-1, 2, 4-三唑与盐酸羟胺反应生成3-偕胺肟基-1, 2, 4-三唑,实验中分别考察了3-氰基-1, 2, 4-三唑与盐酸羟胺摩尔比(n1:n2)、反应温度、pH值和反应时间对合成3-偕胺肟基-1, 2, 4-三唑反应收率的影响。结果见表 1,由表 1确定该反应的较佳合成条件为: 3-氰基-1, 2, 4-三唑/盐酸羟胺的料比为1:1.15,反应温度为60 ℃,pH值为8,反应时间为2 h,收率为49.0%。
| 表 1 合成条件对收率的影响 Tab.1 Influence of synthetic conditions on yield |
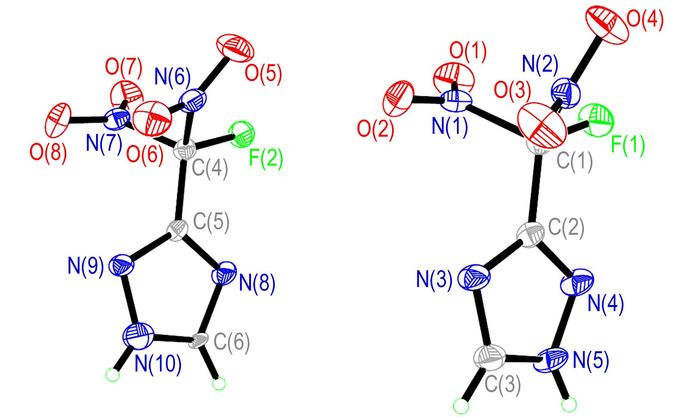
FDNMT晶体的分子结构和分子在晶胞中的堆积分别如图 1、图 2所示。测试结果表明,该晶体为正交晶系,空间群为Pbcn。晶体学参数为: a=7.4821(11) Å,b=9.8106(15) Å,c=38.683(6) Å,α=β=γ=90°,V=2839.5(7) Å3,Z=16,μ=0.178 mm-1,F(000)=1536,CCDC号: 1434789。该晶体结构由Patterrson直接法解出,原子位置均由差值Fourier合成法得到。分子结构用235个参数,由块矩阵最小二乘法进行优化(对于氢原子采用各向同性热参数,对于非氢原子采用各向异性热参数)。对于I>2σ(I)数据的最终偏差因子R1=0.0796,wR2=0.2402;对所有数据的偏差因子R1=0.0823,wR2=0.2437,最佳拟合度s=1.000,最终差值电子云密度的最高峰为539 e·nm-3,最低峰为-675 e·nm-3。
|
图 1 FDNMT的单晶结构 Fig.1 Single crystal structure of FDNMT |
|
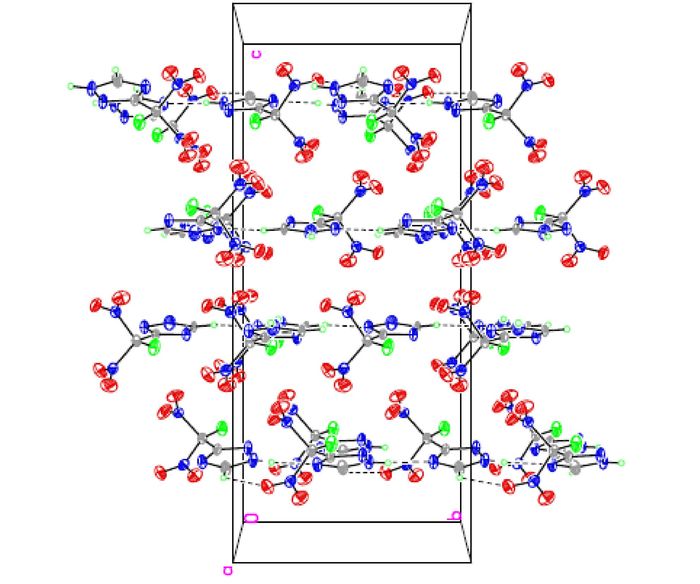
图 2 FDNMT的晶胞堆积图 Fig.2 Packing program of FDNMT |
由图 1和图 2可知,在一个FDNMT晶体单胞中包含两个FDNMT分子,其中F(1)—C(1)—C(2)—N(3)、F(1)—C(1)—C(2)—N(4)、F(2)—C(4)—C(5)—N(8) 和F(2)—C(4)—C(5)—N(9) 的二面角分别为-178.8(4)°、0.4(5)°、-2.1(5)°和-179.0(3)°,表明氟-碳键和三唑环上的所有原子几乎处在同一平面; 分子中两个硝基基团与该平面的分别呈一定的夹角,且两个硝基基团以该平面近似呈镜面对称分布,如N(1)—C(1)—C(2)—N(3)、N(2)—C(1)—C(2)—N(3)、N(6)—C(4)—C(5)—N(9) 和N(7)—C(4)—C(5)—N(9) 的二面角分别为-58.7(5)°、58.6(5)°、59.2(5)°和-59.2(5)°; N(1)—C(1)、N(2)—C(1)、N(6)—C(4) 和N(7)—C(4) 键的键长分别为1.553(5)Å、1.541(5)Å、1.548(5)Å和1.547(5)Å,大于正常N—N单键(1.460 Å)的键长,这可能是由于碳原子上硝基的强吸电子效应导致的结果; 在三唑环单元中,所有的碳氮键和氮氮键的键长都处于N—N单键(1.460 Å)和N= N双键(1.250 Å)、C—N单键(1.470 Å)和C= N双键(1.220 Å)之间,三唑环本身形成一个独立的共轭体系。
3.3 FDNMT的性能预估3-氟偕二硝甲基-1, 2, 4-三唑是一种白色粉状晶体,可溶于二甲基亚砜、N, N-二甲基甲酰胺、甲醇、乙醇等; 微溶于二氯甲烷、水、乙醚、石油醚、环己烷等。采用Gaussian 09程序[13]中的CBS-4M方法计算了该化合物的生成热,基于晶体密度和计算生成热,利用Kamlet-Jacobs爆轰方程[14]预估该化合物的爆轰性能; 采用ZBL-B撞击感度仪测试了FDNMT的感度, 并与TNT、RDX的性能对比,结果见表 2。
| 表 2 FDNMT、TNT和RDX的性能比较 Tab.2 Performance of FDNMT、TNT and RDX |
从表 2可以看出,FDNMT的爆轰性能明显优于TNT,爆速和爆压等性能参数略低于RDX,而爆热明显高于TNT和RDX,撞击感度测试结果表明,FDNMT是一种较RDX更为钝感的新型含能材料。
4 结论(1) 以3-氰基-1, 2, 4-三唑为原料,经肟化、重氮化-氯化、硝化、还原、氟化等反应合成了新型含能化合物——3-氟偕二硝甲基-1, 2, 4-三唑(FDNMT),表征了化合物结构,培养了单晶并进行了晶体结构解析。
(2) 考察了肟化反应的影响因素,获得了最适宜的合成条件: 3-氰基-1, 2, 4-三唑和盐酸羟胺摩尔比为1:1.15,pH值为8,反应时间为2 h,反应温度为60 ℃,收率为49.0%。
(3) 采用Gaussian 09程序中的CBS-4M方法和Kamlet-Jacobs爆轰方程,预估该化合物的爆轰性能,其密度1.81 g·cm-3,爆速8365.0 m·s-1,爆压31.1 GPa,生成热-8.7 kJ·mol-1,爆热为5614.4 kJ·kg-1。
| [1] |
阳世清, 徐松林, 雷永鹏. 氮杂环含能化合物的研究进展[J].
含能材料, 2006, 14(6): 475-480. YANG Shi-qing, XU Song-lin, LEI Yong-peng. Development on nitrogen heterocyclic energetic compounds[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2006, 14(6): 475-480. |
| [2] | WANG Bo-zhou, ZHANG Guo-fang, HUO Huan, et al. Synthesis, characterization and thermal properties of energetic compounds derived from 3-amino-4-(tetrazol-5-yl)furazan[J]. Chin J Chem, 2011, 29: 2421-2427. DOI:10.1002/cjoc.v29.11 |
| [3] |
李玉川, 李生华, 祁才, 等. 新型多氮化合物1, 1′-偶氮-1, 2, 3-三唑的合成与性能研究[J].
化学学报, 2011, 69(18): 21595-2165. LI Yu-chuan, LI Sheng-hua, QI Cai, et al. Synthesis and performance of a novel poly-nitrogen compound 1, 1′-azobis-1, 2, 3-trizaole[J]. Acta Chimica Sinica, 2011, 69(18): 21595-2165. |
| [4] | Venugopal T, Shreeve J M. Synthesis and promising properties of a new family of high-density energetic salts of 5-nitro-3-trinitrometyl-1H-1, 2, 4-trizole and 5, 5′-bis(trinitrometyl)-3, 3′-zao-1H-1, 2, 4-triazole[J]. J Am Chem Soc, 2011, 133: 19982-19992. DOI:10.1021/ja208990z |
| [5] |
李亚南, 张志忠, 周彦水, 等. 3, 4-双取代氧化呋咱衍生物的合成、结构表征及热性能研究[J].
化学学报, 2011, 69(6): 701-708. LI Ya-nan, ZHANG Zhi-zhong, ZHOU Yan-shui, et al. Study on the synthesis, structure characterization and thermal performance of 3, 4-disubstituted furoxano derivatives[J]. Acta Chimica Sinica, 2011, 69(6): 701-708. |
| [6] | Gao H, Shreeve J M. Azole-based energetic salts[J]. Chem Rev, 2011, 111: 7377-7436. DOI:10.1021/cr200039c |
| [7] | Liu L, Zhang Y, Zhang S, Fei T. Heterocyclic energetic salts of 4, 4′, 5, 5′-tetranitro-2, 2′-biimidazole[J]. J Energ Mater, 2015, 33: 202-214. DOI:10.1080/07370652.2014.970246 |
| [8] | Yongxing Tang, Chunlin He, Haixiang Gao, et al. Energized nitro-substituted azoles through ether bridges[J]. J Mater Chem A, 2015, 3: 15576-15582. DOI:10.1039/C5TA03884G |
| [9] | Joo Y H, Shreeve J M. Nitroimino-tetrazolates and oxy-nitroimino-tetrazolates[J]. J Am Chem Soc, 2010, 132: 15081-15090. DOI:10.1021/ja107729c |
| [10] | Xin Yin, Jin-Ting Wu, Xin Jin, et al. Nitrogen-rich salts of 1-aminotetrazol-5-one: oxygen-containing insensitive energetic materials with high thermal stability[J]. RSC Adv, 2015, 5: 60005-60014. DOI:10.1039/C5RA07649H |
| [11] | Lianjie Zhai, Xuezhong Fan, Bozhou Wang, et al. A green high-initiation-power primary explosive: synthesis, 3D structure and energetic properties of dipotassium 3, 4-bis(3-dinitromethylfurazan-4-oxy)furazan[J]. RSC Adv, 2015, 5: 57833-57841. DOI:10.1039/C5RA09822J |
| [12] | Chunlin He, Shreeve J M. Potassium 4, 5-bis(dinitromethyl)furoxanate: a green primary explosive with a positive oxygen balance[J]. Angew Chem Int Ed, 2016, 55: 772-775. DOI:10.1002/anie.201509209 |
| [13] | Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 09[CP], Gaussian, Inc., Wallingford CT, 2009. |
| [14] | Hariharan P C, Pople J A. Influence of polarization functions on molecular-orbital hydrogenation energies[J]. Theor Chim Acta, 1973, 28: 213-222. DOI:10.1007/BF00533485 |
| [15] | Sheldrick G M. SHELXTS-97, Program for crystal structure solution[CP], University of Gttingen, Germany, 1997. |
| [16] | Zhang Y Q, Guo Y, Joo Y H, et al. 3, 4, 5-Trinitropyrazole-based energetic salts[J]. Chem Eur J, 2010, 16: 10778-10784. DOI:10.1002/chem.201001243 |
| [17] | Mayer R, Khler J, Homburg A. Explosive. 6th ed[CP]. Weinheim, Germany, Wiley-VCH, 2007. |
3-Fluorodinitromethyl-1,2,4-triazole(FDNMT) was synthesized using 3-cyano-1,2,4-triazole as starting material. The structure of FDNMT was confirmed by IR, 1H NMR, 13C NMR, elemental analysis and MS. The single crystal of FDNMT was obtained in the acetonitrile system. The detonation properties of FDNMT were calculated using Gaussian 09 program and Kamlet-Jacobs equations.



