2. 超重力化工过程山西省重点实验室, 山西 太原 030051
2. Shanxi Province Key Laboratory of Higee-Oriented Chemical Engineering, Taiyuan 030051, China
火炸药合成、石油、化工、造纸、塑料、医药等行业的含酚废水降解过程中会产生间苯二酚[1]。间苯二酚属于内分泌干扰物, 会造成生殖畸形, 发育异常[2]。目前间苯二酚废水的处理方法主要有超声降解法[3]、光催化法[2]、生物接触氧化法[4]和吸附法[5-7]等, 其中, 吸附法因工艺成熟, 不带入新的污染物和能耗低等特点, 已广泛用于水质净化和废水处理[8]。但传统的吸附工艺中, 吸附设备如接触式过滤吸附装置, 固定床, 流化床等, 都存在设备体积庞大, 吸附速率较小, 床层利用率较低等问题[9]。近年来, 超重力旋转填料床(RPB)因设备体积小, 投资和操作费用低, 传质效果好等优势而受到关注。2000年Lin等[9]研究了超重力场下颗粒活性炭对碱性黄色染料的吸附, 发现超重力场的存在促进了吸附传质。2004年Lin和Chen等[10]分别采用活性炭和锯屑为吸附剂, 对比研究了超重力场中乳化十二烷的吸附, 发现超重力可以强化传质, 增大吸附速率。2012年Chang等[11]采用活性炭为吸附剂, 研究了超重力场下转速, 流量和初始浓度对灭多威吸附动力学的影响, 发现RPB能提供更多的活性位点, 促进扩散过程和内部传质。2016年Kundu等[12]研究了超重力场下活性炭对直接红23的吸附, 并与恒温水浴振荡器就活性炭的吸附特性进行了对比。结果表明, 转速和流量是RPB中影响直接红23去除的重要参数, 且在相同条件吸附5 h后, RPB和振荡器中染料的去除率分别为93%和55%。以上研究大多集中于操作参数的选取, 并没有对超重力场下的吸附热力学进行研究, 且对吸附平衡和动力学研究也不太全面。
为此, 本研究以有机废水处理中常用的活性炭为吸附剂, RPB为吸附设备, 自制间苯二酚溶液模拟间苯二酚废水。采用单因素法考察了超重力因子、液体流量、温度、pH等对间苯二酚去除率的影响, 确定最佳条件, 通过模型拟合研究了超重力场下活性炭吸附间苯二酚的吸附平衡和吸附动力学及热力学性质。
2 实验部分 2.1 试剂与仪器间苯二酚, 分析纯, 天津市兴复科技发展有限公司; 活性炭, 工业纯, 柱状, 长度2~8 mm, 平均直径3 mm, 比表面积671.5 m2·g-1, 平均孔径0.5240 nm, 山西新华化工厂; 超纯水为实验室自制; 氢氧化钠, 分析纯, 天津市大陆化学试剂厂; 盐酸, 分析纯, 洛阳市化学试剂厂。
pH酸度计(上海先导科技PHS-3C型)、自动气体吸附仪(美国康塔)、高效液相色谱仪(美国戴安科技Ultimate 3000型)。
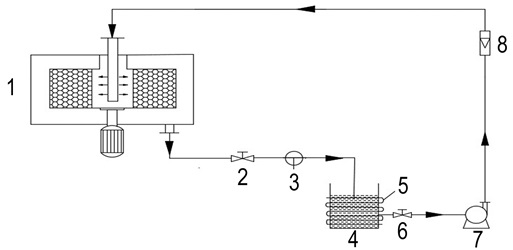
2.2 实验装置及工艺流程自制RPB尺寸为:转子内径、外径、高度分别为30, 65, 40 mm。实验流程如图 1所示:废水槽4内配制好的间苯二酚溶液, 经缠绕在废水槽4表面的加热带5加热, 达到指定温度(30, 40, 50 ℃)后, 溶液由液泵7经液体流量计8进入装填量为100 g左右的RPB 1中, 通过旋转填料床的转子中心的液体分布器, 将其均匀地喷到填料环内侧, 同时在超重力的作用下被剪切成极细的液丝、液膜, 沿径向由内向外运动, 与填料接触进行吸附传质, 完成吸附传质的废水经出液口3排出, 进入废水槽4中, 废水槽4中的液体再次进入1中进行循环处理。
|
图 1 RPB中活性炭吸附间苯二酚的实验流程图 1—RPB, 2, 6—阀门, 3—出液口, 4—废水槽, 5—加热带, 7—液泵, 8—液体流量计 Fig.1 Experiment progress flow of adsorption of resorcinol on activated carbon in RPB 1—rotating packed bed, 2, 6—valves, 3—outlet, 4—waste water tank, 5—heating zone, 7—liquid pump, 8—fluid flow meter |
活性炭预处理:为了除去吸附剂活性炭表面的灰分及杂质, 对其进行预处理:将活性炭煮沸40 min, 超纯水多次冲洗后置于鼓风干燥箱, 于110 ℃下干燥12 h, 然后储存在干燥器中, 待用。采用自动气体吸附仪测定活性炭的比表面积。
间苯二酚浓度测定:采用高效液相色谱仪测定间苯二酚浓度。测定条件如下: C18反相柱(250 mm×4.6 mm, 5 μm), 检测波长为277 nm, 流动相为甲醇/水=60/40, 进样量为20 μL, 温度为20 ℃, 流速为1 mL·min-1。
采用公式(1)和公式(2)分别计算间苯二酚去除率及平衡吸附量[13]:
| $ \eta = \frac{{\left( {{C_0} - {C_{\rm{e}}}} \right)}}{{{C_0}}} \times 100\% $ | (1) |
| $ {q_e} = \frac{{\left( {{C_0} - {C_{\rm{e}}}} \right)V}}{W} $ | (2) |
式中, C0是间苯二酚的初始浓度, mg·L-1; Ce是间苯二酚的平衡浓度, mg·L-1; V是溶液的体积, L; qe是平衡吸附量, mg·g-1; W是活性炭的质量, g。
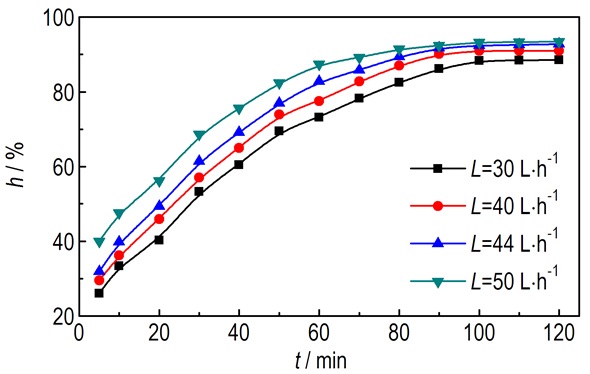
3 结果与讨论 3.1 液体流量对间苯二酚去除率的影响固定超重力因子为41.30, 间苯二酚废水初始浓度为900 mg·L-1, pH为5, 温度为20 ℃, 研究了液体流量对间苯二酚去除率的影响, 结果见图 2。由图 2可知, 间苯二酚去除率随着液体流量的增大而增大, 当液体流量从30 L·h-1增大到50 L·h-1, 间苯二酚的去除率从88.48%增大到93.38%。分析其原因可能为:增大液体流量, 活性炭润湿程度增加, Munjal等[13]曾指出润湿程度与传质有效面积成正比。所以增大液体流量, 单位体积内的液滴数目增多, 吸附质更易到达吸附剂表面, 固液接触面积增大, 促进了吸附传质过程。因此, 选择50 L·h-1为最优的液体流量。
|
图 2 液体流量对间苯二酚去除率的影响 Fig.2 Effect of liquid flow on the removal efficiency of resorcinol |
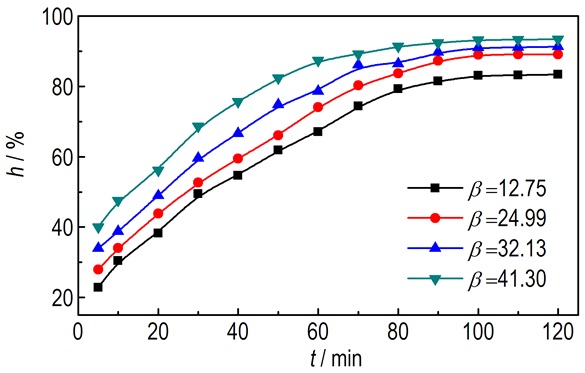
固定液体流量为50 L·h-1, 间苯二酚废水初始浓度为900 mg·L-1, pH为5, 温度为20 ℃, 研究了超重力因子(β)对间苯二酚去除率的影响见图 3。由图 3可知, 间苯二酚的去除率随着超重力因子的增大而增大。分析其原因可能为:一方面, 随着超重力因子的增大, RPB中溶液得到充分混合[11], 液体被分散为更多的细小液滴, 分布更均匀, 溶液中间苯二酚更易到达活性炭表面; 另一方面, 固液相界面的液膜被剪切的更薄, 传质阻力降低, 促进了活性炭对间苯二酚的吸附[12]。因此, 41.30为最优的超重力因子。
|
图 3 超重力因子对间苯二酚去除率的影响 Fig.3 Effect of supergravity factor on the removal efficiency of resorcinol |
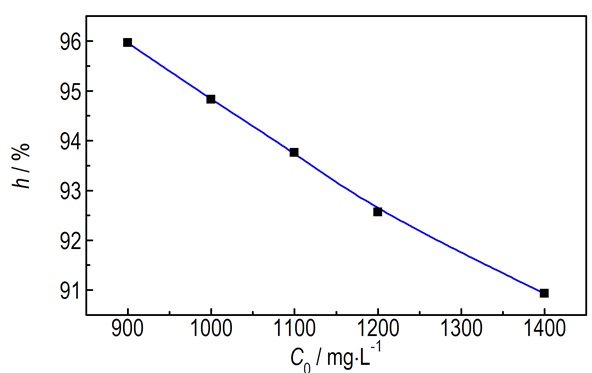
固定液体流量为50 L·h-1, 超重力因子为41.30, pH为5, 温度为20 ℃, 考察了间苯二酚初始浓度对间苯二酚去除率的影响见图 4。由图 4可知, 间苯二酚去除率随着初始浓度的增大而减小。分析其原因可能为:由于吸附剂质量一定, 废水中间苯二酚浓度越高, 传质阻力越大, 间苯二酚到达活性炭表面的速率减慢, 所以间苯二酚去除率越低[14]。因此, 900 mg·L-1为适宜的初始浓度。
|
图 4 初始浓度对间苯二酚去除率的影响 Fig.4 Effect of initial concentration on the removal efficiency of resorcinol |
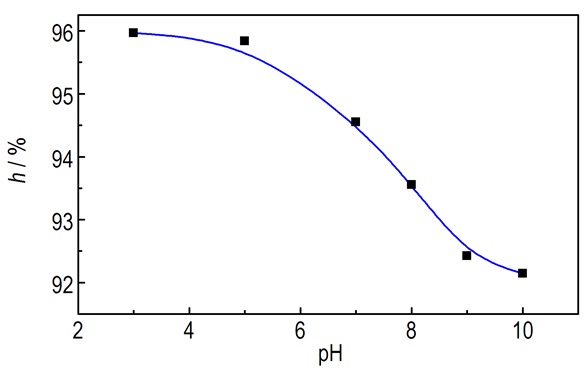
固定液体流量为50 L·h-1, 超重力因子为41.30, 间苯二酚废水初始浓度为900 mg·L-1, 温度为20 ℃, 研究了溶液pH对间苯二酚去除率的影响见图 5。由图 5可知间苯二酚去除率随着pH的增大而减小, 当pH小于7时, 间苯二酚去除率基本不变; 当pH值大于7时, 间苯二酚去除率明显降低。分析其原因可能为:间苯二酚属于弱酸, 当pH值小于7时, 间苯二酚在溶液中呈分子状态, 当pH值大于7时, 间苯二酚分子转化为间苯二酚盐, 增大了溶解能力, 此时间苯二酚在活性炭上以脱附为主, 导致间苯二酚去除率降低[15-16]。因此, 选择5为最优的pH值。
|
图 5 pH值对间苯二酚去除率的影响 Fig.5 Effect of pH value on the removal efficiency of resorcinol |
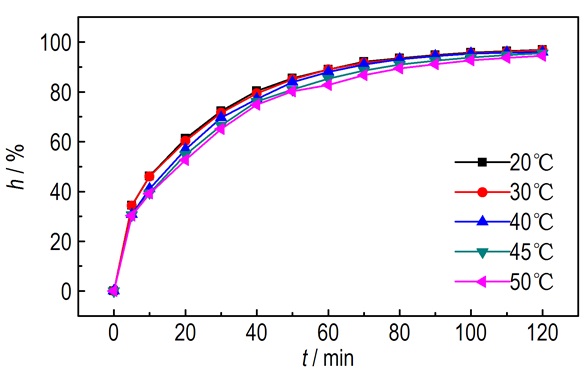
固定液体流量为50 L·h-1, 超重力因子为41.30, 间苯二酚废水初始浓度为900 mg·L-1, pH为5, 考察了溶液温度对间苯二酚去除率的影响见图 6。由图 6可知, 当温度从20 ℃增加到50 ℃时, 间苯二酚去除率从94.44%增长到96.86%, 但当吸附达到平衡时, 去除率相差不超过2.42%, 说明吸附速率随温度变化不显著, 符合物理吸附的特征。分析其原因可能为:吸附为放热反应, 降低温度利于吸附, 因此, 20 ℃为最优温度。
|
图 6 温度对间苯二酚去除率的影响 Fig.6 Effect of temperature on the removal efficiency of resorcinol |
综上所述, 适宜的操作条件为:液体流量为50 L·h-1, 超重力因子为41.30, pH值为5, 温度为20 ℃, 间苯二酚初始浓度为900 mg·L-1, 吸附时间为2 h。
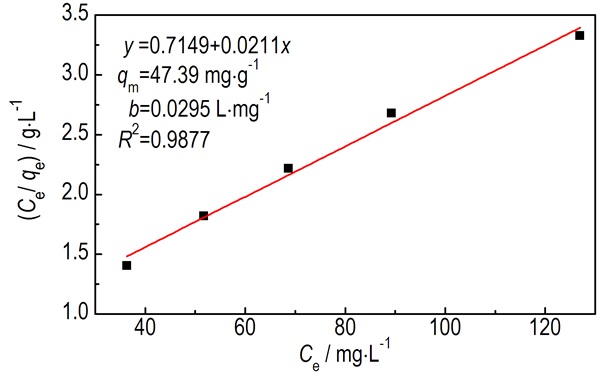
3.6 吸附平衡研究基于图 4, 利用公式(1)和(2)求得间苯二酚平衡浓度Ce和平衡吸附量qe。根据Langmuir[17]和Freundlich[17]模型利用最小二乘法分别对间苯二酚的吸附平衡数据进行拟合, 拟合图分别为图 7和图 8。通过比较相关系数R2确定超重力场下间苯二酚在活性炭上的等温吸附模型。
|
图 7 Langmuir模型的性拟合结果 Fig.7 Linear fitting result from Langmuir model |

|
图 8 Freundlich模型的性拟合结果 Fig.8 Linear fitting result from Freundlich model |
Langmuir模型:
| $ \frac{{{C_{\rm{e}}}}}{{{q_{\rm{e}}}}} = \frac{1}{{{q_{\rm{m}}}b}} + \frac{{{C_{\rm{e}}}}}{{{q_{\rm{m}}}}} $ | (3) |
Freundlich模型:
| $ {\rm{ln}}{q_{\rm{e}}} = {\rm{ln}}{k_{\rm{F}}} + \left( {\frac{1}{n}} \right){\rm{ln}}{C_{\rm{e}}} $ | (4) |
式中, Ce是间苯二酚的平衡浓度, mg·L-1; qe是平衡吸附量, mg·g-1; qm是活性炭的饱和吸附量, mg·g-1; b为Langmuir吸附常数, mg·L-1; kF和n均为Freundlich等温方程常数。
由图 7和图 8可知, 吸附平衡数据能很好地符合Langmuir和Freundlich模型, 由Freundlich模型拟合得到的相关系数R2优于Langmuir模型, 因此, Freundlich模型能较好的描述超重力场下间苯二酚在活性炭上的吸附行为。通常, Freundlich模型中, 1/n的数值一般在0~1之间, 其值的大小表示浓度对吸附量影响的强弱。1/n越小, 吸附性能越好, 0<1/n<0.5, 易于吸附, 1/n大于2则难于吸附[6]。由图 7可知, 1/n为0.3067, 小于0.5, 表明间苯二酚易吸附于活性炭上, 与Liao等结论一致[15]。分析其原因可能为Langmuir模型是一个理想的吸附模型, 它代表了单层表面吸附, 吸附分子彼此没有相互作用下, 吸附达到平衡时的规律, 对于具体体系还需修正。而Freundlich模型则是一个经验公式, 应用范围较广[18]。因此, 本实验采用Freundlich模型来描述超重力场下间苯二酚在活性炭上的吸附行为。
3.7 热力学及动力学研究 3.7.1 热力学研究采用Vant′ Hoff方程[19]对热力学进行研究:
| $ {\rm{ln}}\frac{1}{{{C_{\rm{e}}}}} = {\rm{ln}}{k_0} + \left( { - \frac{{\Delta H}}{{RT}}} \right) $ | (5) |
式中, Ce为平衡浓度, mol·L-1; ΔH为等量吸附焓变, kJ·mol-1; T为试验温度, K; k0为Van′t Hoff方程常数。根据图 6所得的数据, 以ln(1/Ce)对1/T作图, 得ΔH值为-14.65 kJ·mol-1, 小于0, 说明此吸附过程为放热过程, 低温有利于吸附。吸附过程中吸附热为14.65 kJ·mol-1, 介于物理吸附热2.1~20.9 kJ·mol-1 [20], 吸附热不高, 说明超重力场下活性炭吸附间苯二酚以物理吸附或表面吸附为主(范德华力等)。
3.7.2 动力学研究在上述适宜条件下, 研究了活性炭在固定床、磁力搅拌器与RPB中对间苯二酚去除率的影响, 结果如图 9。

|
图 9 不同反应器对间苯二酚去除率的影响 Fig.9 Effect of different reactors on the removal efficiency of resorcinol |
由图 9可知, 相同操作条件下, RPB、磁力搅拌器、传统固定床中, 间苯二酚的去除率分别为96.86%、83.3%和78.31%, RPB较传统固定床和磁力搅拌吸附法而言, 去除率分别提高了约20%和14%。
准一级动力学模型:
| $ {\rm{ln}}\left( {{q_{\rm{e}}} - {q_t}} \right) = {\rm{ln}}{q_{\rm{e}}} - {k_1}t $ | (6) |
准二级动力学模型:
| $ \frac{t}{{{q_t}}} = \frac{1}{{{k_2}{q_{\rm{e}}}^2}} + \frac{t}{{{q_{\rm{e}}}}} $ | (7) |
式中, qt和qe分别为t时刻和平衡态的吸附量, mg·g-1; k1为一级吸附速率常数, min-1; k2为二级吸附速率常数, g·mg-1·min-1。
基于图 9数据, 分别采用准一级[21]、准二级[22]动力学模型对其进行线性拟合, 即分别考察ln(qe-qt)、t/qt随t的变化, 并根据斜率求得k1、k2值, 拟合结果列于表 1。
| 表 1 适宜操作条件下RPB吸附间苯二酚的准一级、准二级模型拟合结果 Tab.1 Linear fitting results from the pseudo-first order kinetic model, the pseudo-second order kinetic model of resorcinol adsorption in a RPB under the optimum operation conditions |
由表 1可知, 三种反应器的准二级模型的线性相关系数R2均高于准一级, 说明实验和准二级动力学模型能较好地吻合。由表 1中拟合出的准二级动力学方程得RPB、磁力搅拌器和传统固定床的吸附速率常数k2分别为2.576×10-3, 1.584×10-3, 1.823×10-3 g·mg-1·min-1, RPB中k2是传统的固定床与磁力搅拌器的1.626和1.413倍, 说明超重力场的存在强化了液固之间的传质, 利于吸附的进行。分析其原因可能为:一般来说, 准一级模型仅能描述吸附的初始状态, 而准二级模型可以预测吸附的整个过程, 包括膜扩散及内扩散。因此, 采用准二级模型来进行吸附动力学研究。
为进一步了解吸附过程, 采用Weber-Morris(内扩散)动力学模型[23]对图 9数据进行拟合:
| $ {q_t} = {k_p}{t^{1/2}} + C $ | (8) |
式中qt为t时刻的吸附量, mg·g-1; kp为颗粒内扩散速率常数, mg·(g·min1/2)-1, C为与边界层厚度有关的常数。
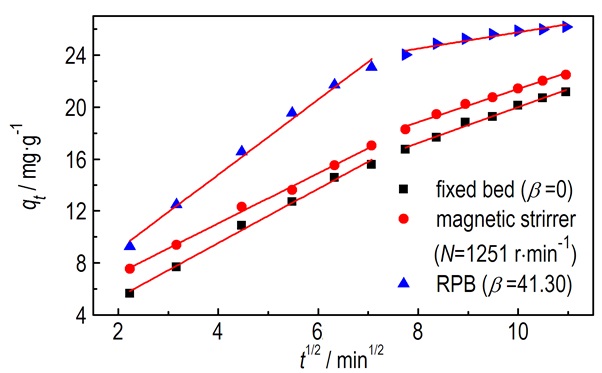
将qt对t1/2作图, 其斜率和截距分别为kp和C, 拟合结果如图 10。其中, 曲线的初始部分代表边界层扩散(膜扩散), 之后的部分代表内扩散[24]。由图 10可知, 在整个吸附过程中qt-t1/2并不满足线性关系。曲线偏离原点, 说明内扩散不是唯一的速率控制步骤, 在整个吸附过程中, 膜扩散和内扩散占主导地位[25]。通过对实验数据分段拟合后发现, 吸附初始阶段为膜扩散过程, 内扩散为速率控制步骤。即一开始, 由于吸附质与吸附剂之间的浓度差大, 推动力大, 膜扩散速率大, 间苯二酚易被活性炭的外表面吸附, 吸附速度非常快, 故内扩散为速率控制步骤。吸附中后期阶段, 膜扩散为速率控制步骤。即当外表面的吸附达到饱和时, 间苯二酚扩散到活性炭孔中, 此时, 膜扩散阻力增加, 导致膜扩散速率降低, 随着溶液中间苯二酚浓度的降低, 推动力减小, 膜扩散速率越来越低, 扩散过程达到平衡阶段。因此后阶段膜扩散为速率控制步骤, 符合Suresh等[26]采用颗粒活性炭吸附间苯二酚的机理研究, 且与活性炭吸附间苯二酚符合准二级动力学模型机理相一致。
|
图 10 Weber-Morris模型线的性拟合结果 Fig.10 Linear fitting results from Weber-Morris model |
(1) 通过单因素实验得出适宜操作条件:当液体流量为50 L·h-1, 超重力因子为41.30, pH值为5, 温度为20 ℃, 初始浓度为900 mg·L-1, 吸附2 h后, 间苯二酚去除率达到96.86%。相同操作条件下, 较传统固定床和磁力搅拌吸附而言, 去除率分别提高了约20%和14%。
(2) 吸附平衡与热力学研究表明:吸附平衡关系主要服从Freundlich模型, 且吸附过程中吸附热为14.65 kJ·mol-1, 即超重力场下, 间苯二酚在活性炭上的吸附过程主要为物理吸附过程。
(3) 动力学研究表明, 吸附过程主要符合准二级方程, 内扩散不是唯一的速率控制步骤。适宜条件下, RPB吸附法的动力学方程为y=-0.04254x+3.153, 吸附速率常数为2.576×10-3 g·mg-1·min-1, 是相同条件下固定床与磁力搅拌器吸附的1.626倍和1.413倍, 说明超重力强化了液固传质, 对吸附有利。
| [1] |
肖忠良, 胡双启, 吴晓青, 等.
火炸药的安全与环保技术[M]. 北京: 北京理工大学出版社, 2006: 79-86.
|
| [2] |
Pardeshi S K, Patil A B. Solar photocatalytic degradation of resorcinol a model endocrine disrupter in water using zinc oxide[J].
Journal of Hazardous Materials, 2009, 163(1): 403-409. DOI:10.1016/j.jhazmat.2008.06.111 |
| [3] |
卞炜, 朱志庆. 超声波降解间苯二酚水溶液研究[J].
应用化工, 2006, 35(9): 706-708. BIAN Wei, ZHU Zhi-qing. Study on degradation of resorcin aqueous solution by ultrasound[J]. Applied Chemical Industry, 2006, 35(9): 706-708. |
| [4] |
Sharma V, Srivastava V C, Kushwaha J P, et al. Studies on biodegradation of resorcinol in sequential batch reactor[J].
Internation Biodeterioration & Biodegradation, 2010, 64(8): 764-768. |
| [5] |
Kumar A, Kumar S, Kumar S. Adsorption of resorcinol and catechol on granular activated carbon:equilibrium and kinetics[J].
Carbon, 2003, 41(15): 3015-3025. DOI:10.1016/S0008-6223(03)00431-7 |
| [6] |
姜灵彦, 刘蕾, 崔节虎, 等. 粉末活性炭对模拟间苯二酚废水的吸附[J].
光谱实验室, 2011, 28(4): 1738-1743. JIANG Ling-yan, LIU Lei, CUI Jie-hu, et al. Adsorption of powdered activated carbon on simulate resorcinol wastewater[J]. Chinese Journal of Spectroscopy Laboratory, 2011, 28(4): 1738-1743. |
| [7] |
Rodrigaez E, Encinas A, Masa F J, et al. Influence of resorcinol chemical oxidation on the removal of resulting organic carbon by activated carbon adsorption[J].
Chemosphere, 2008, 70(8): 1366-1374. DOI:10.1016/j.chemosphere.2007.09.035 |
| [8] |
CHANG C F, CHANG C Y, Höll W. Investigating the adsorption of 2-mercaptothiazoline on activated carbon from aqueous systems[J].
Journal of Colloid and Interface Science, 2004, 272(1): 52-58. DOI:10.1016/j.jcis.2003.09.012 |
| [9] |
Lin C C, Liu H S. Adsorption in a centrifugal field: Basic dye adsorption by activated carbon[J].
Ind Eng Chem Res, 2000, 39(1): 161-167. DOI:10.1021/ie9902333 |
| [10] |
Lin C C, Chen Y S, Liu H S. Adsorption of dedecane from water in a rotating packed bed[J].
J Chin Inst Engrs, 2004, 35(5): 531-538. |
| [11] |
Chang C F, Lee S C. Adsorption behavior of pesticide methomyl on activated carbon in a high gravity rotating packed bed reactor[J].
Water Research, 2012, 46(9): 2869-2280. DOI:10.1016/j.watres.2012.02.041 |
| [12] |
Kundu A, Hassan L S, Redzwan G, et al. Application of a rotating packed bed contactor for removal of Direct Red 23 by adsorption[J].
Desalination and Water Treatment, 2016, 57(29): 13518-13526. DOI:10.1080/19443994.2015.1060165 |
| [13] |
Munjal S, Dudukovc M P, Ramachandran P. Mass transfer in rotating packed beds-Ⅱ.experimental results and comparison with theory and gravity flow[J].
Chemical Engineering Science, 1989, 44(10): 2257-2268. DOI:10.1016/0009-2509(89)85160-7 |
| [14] |
武晓娜, 刘有智, 焦纬洲. 旋转填料床中活性炭吸附含酚废水研究[J].
含能材料, 2016, 24(5): 509-514. WU Xiao-na, LIU You-zhi, JIAO Wei-zhou. Adsorption of phenol on activated carbon in rotating packed bed[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2016, 24(5): 509-514. DOI:10.11943/j.issn.1006-9941.2016.05.014 |
| [15] |
Liao Q, Sun J, Gao L. The adsorption of resorcinol from water using multi-walled carbon nanotubes[J].
Colloids and Surfaces A: Physicochem Eng Aspects, 2008, 312(2): 160-165. |
| [16] |
Kalavathy M H, Swaroop G, Padmini E, et al. A biosorbent for resorcinol adsorption-isotherm and kinetic studies[J].
Carbon Letters, 2009, 10(1): 23-32. DOI:10.5714/CL.2009.10.1.023 |
| [17] |
Richard D, Núnez-M L D, Schweich D. Adsorption of complex phenolic compounds on active charcoal: Adsorption capacity and isotherms[J].
Chemical Engineering Journal, 2009, 148(1): 1-7. |
| [18] |
王秀芳, 张会平, 肖新颜, 等. 苯酚在竹炭上的吸附平衡和动力学研究[J].
功能材料, 2005, 36(5): 746-749. WANG Xiu-fang, ZHANG Hui-ping, XIAO Xin-yan, et al. Adsorption equilibrium and dynamics of phenol on bamboo charcoals[J]. Functional Materials, 2005, 36(5): 746-749. |
| [19] |
Garcia R A, Cotouelo M L M, Rodriguez J J. Equilibrium study of single solute adsorption of anionic surfactants with polymeric XAD resins[J].
Separation Science and Technology, 1992, 27(7): 975 DOI:10.1080/01496399208019736 |
| [20] |
Suresh S, Srivastava V C, Mishra I M. Isotherm, thermodynamics, desorption, and disposal study for the adsorption of catechol and resorcinol onto granular activated carbon[J].
Journal of Chemical & Engineering Data, 2011, 56(4): 70-74. |
| [21] |
Aksu Z. Biosorption of reactive dyes by dried activated sludge: equilibrium and kinetic modeling[J].
Biochemical Engineering Journal, 2001, 7(1): 79-84. DOI:10.1016/S1369-703X(00)00098-X |
| [22] |
Ho Y S, Mc K G. Pseudo-second order model for sorpyion processes[J].
Process Biochemistry, 1999, 34(5): 451-465. DOI:10.1016/S0032-9592(98)00112-5 |
| [23] |
Weber W J, Morris J C.
Proceeding of international conference on water pollution symposium[M]. Oxford: Pergamon Press, 1962: 231 |
| [24] |
Walker G M, Hansen L, Hanna J A, et al. Kinetics of a reactive dye adsorption onto dolomitic sorbents[J].
Water Research, 2003, 37(9): 2081-2089. DOI:10.1016/S0043-1354(02)00540-7 |
| [25] |
TUNG H H, RICHARD S H. Modeling liquid mass transfer in higee separation process[J].
Chem Eng Commun, 1985, 39(1): 147-153. |
| [26] |
Suresh S, Srivastava V C, Mishra I M. Study of catechol and resorcinol adsorption mechanism through granular activated carbon characterization, pH and kinetic study[J].
Separation Science and Technology, 2011, 46(11): 1750-1766. DOI:10.1080/01496395.2011.570284 |
Effects of temperature, supergravity factor, pH value, liquid flow rate, and initial resorcinol concentration on the removal efficiency of resorcinol were studied. The adsorption equilibrium, thermal behavior and kinetic parameters were investigated. Weber-Morris model was adopted to study the adsorption mechanism of resorcinol on activated carbon.




