2. 中国工程物理研究院核物理与化学研究所中子物理学重点实验室, 四川 绵阳 621999
2. Key Laboratory of Neutron Physics, Institute of Nuclear Physics and Chemistry, CAEP, Mianyang 621999, China
奥克托今(HMX)是当今军事上使用的综合性能最优的含能材料之一, 具有密度高、爆轰性能优良、热安定性和贮存稳定性好等优点, 广泛应用于导弹、核武器以及高性能固体推进剂等方面, 在火炸药领域居重要地位[1-4]。自从1941年W. E.Bachmann等人分离并确定HMX的结构以来[5], 化学家对非氘代HMX进行了大量的合成、结构及性能等研究, 但鲜有氘代奥克托今(HMX-d8)的相关研究报道。HMX的主要合成方法包括乌洛托品直接硝解法、乌洛托品间接硝解法及小分子合成法等[6-9]。其中, 乌洛托品直接硝解法和小分子合成法存在产率低、副产物多等问题。乌洛托品间接硝解法则包括1, 5-二乙酰基-3, 7-二硝基-1, 3, 5, 7-四氮杂辛烷(DADN)法、1, 3, 5, 7-四乙酰基-1, 3, 5, 7-四氮杂环辛烷(TAT)法和1, 5-二乙酰基-3-硝基-7-亚硝基-1, 3, 5, 7-四氮杂辛烷(DANNO)法等, 具有杂质少、产率高等优点, 但工艺路线相对较长[10]。
中子衍射、中子散射等中子技术是最近几十年来发展起来的一种研究物质结构的新方法[11]。在含能材料领域, 中子技术是研究含能材料内部微观结构和内部应力等不可或缺的工具[12-14]。由于氢原子对中子衍射或散射等信号干扰较大, 测试前往往需要将样品氘代。目前, 由于缺乏HMX-d8, 其中子技术等研究尚未见报道。本研究采用DADN法合成了β-HMX-d8, 探索了氘代乌洛托品(HMTA-d12)、氘代1, 5-二乙酰基-3, 7-二硝基-1, 3, 5, 7-四氮杂辛烷(DADN-d8)和氘代奥克托今(β-HMX-d8)合成条件及优化, 以期制备适用于中子技术研究的HMX-d8材料。
2 实验部分 2.1 试剂与仪器多聚甲醛, 乌洛托品, 氨水(25%~28%), 去离子水(自制), 浓硫酸(98%), 甲苯, 叔丁醇, 乙醇, 乙腈, 乙酸, 乙酸酐, 无水硝酸(自制), 三氯甲烷, 四氢呋喃, 硝酸钾, 硝酸钠, 乙酸铵, 丙酮, 上述未提及纯度的试剂均为分析纯, 成都科龙化工试剂厂。氘代多聚甲醛(氘代率99.99%), 英国剑桥氘代实验室。
UV-1800PC型分光光度计, 扫描范围为200~650 nm; 美国Nicolet 5700型傅里叶变换红外吸收光谱仪, KBr压片, 扫描范围4000~400 cm-1; Varian 325-LC-MS质谱仪, 美国Agilent公司; Ultimate3000DGLC双三元、二维液相色谱仪, 美国Thermo Fisher Scientific公司, Zorbax SB-C18柱, 美国Agilent公司; 瑞士Brucker Avance 600型核磁共振波谱仪; 美国TA公司Q200 DSC测试仪; 美国TA仪器公司SDT Q600同步热分析仪; X Pert pro X-射线衍射仪, 荷兰帕纳科公司。
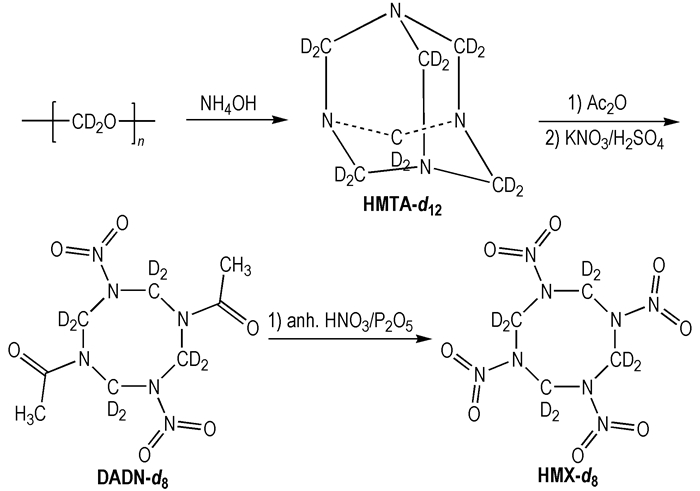
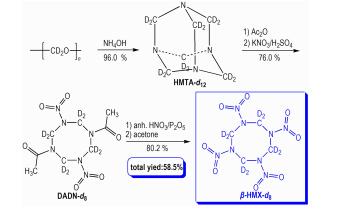
2.2 合成路线以氘代多聚甲醛为原料, HMX-d8合成路线见Scheme 1。
|
Scheme1 Synthetic route of HMX-d8 |
将氘代多聚甲醛(1.01 g, 31.6 mmol)置于25 mL两口圆底烧瓶中, 加入2.0 mL去离子水, 缓慢滴加氨水(3.0 mL, 浓度25%~28%), 加料过程中控温26~35 ℃。加料完毕后, 控温40 ℃左右反应68 h。反应完毕后, 往反应液里加入分批加入30 mL的叔丁醇, 在低于40 ℃条件下, 共沸蒸馏除去溶剂水, 得到白色氘代乌洛托品(HMTA-d12)粉末, 产率96.0%。
m.p. 265.1 ℃ (DSC); UV-vis (CHCl3) λmax: 244.3 nm; FT-IR (KBr, ν/cm-1): 3433, 2214, 2151, 2104, 2079, 1636, 1175, 1076, 908, 727, 638; MS (APCI) m/z: 153.1 [M+H]+。
2.3.2 1, 5-二乙酰基-3, 7-二硝基-1, 3, 5, 7-四氮杂环辛烷-d8(DADN-d8)的合成将HMTA-d12(4.70 g, 30.9 mmol)置于25 mL两口圆底烧瓶中, 加入乙酸铵(1.0 g, 13.3 mmol), 混合均匀后, 缓慢滴加乙酸酐(6.0 mL, 63.5 mmol), 滴加时控温5~10 ℃。滴加完毕后, 在该温度下反应1 h, 然后在室温下继续反应1 h。加热, 在30 ℃左右反应40 h。冷却得到3, 7-二乙酰基-1, 3, 5, 7-四氮杂环(3, 3, 1)壬烷-d10 (DAPT-d10)溶液。该溶液可不经纯化直接用于下步反应。
将60 mL浓硫酸(98%)加入250 mL两口圆底烧瓶中, 分批加入硝酸钾(17.0 g, 168.3 mmol), 加料完毕后, 搅拌至固体溶解, 降温至15~16 ℃。然后在剧烈搅拌下缓慢滴加上述DAPT-d10溶液, 加料过程中控温30~40 ℃。加料完毕后, 在该温度下继续反应1.5 h。冷却, 加入少量去离子水稀释, 置于室温下结晶, 过滤, 干燥, 即得到DADN-d8产品, 产率76.0%。
m.p. 276.5 ℃ (DSC); UV-vis (DMSO) λmax: 282.7 nm; 1H NMR (DMSO-d6, 600 MHz) δ: 2.30 (CH3O); FT-IR (KBr, ν/cm-1): 3436, 2950, 2850, 2279, 1681, 1529, 1447, 1382, 1334, 1262, 1205, 1158, 1134, 1061, 1029, 982, 896, 826, 705, 608, 590, 574, 501; MS (APCI) m/z: 295.9 [M-D]-。
2.3.3 氘代奥克托今(HMX-d8)的合成将2.4 mL无水硝酸置于50 mL干燥的两口圆底烧瓶中, 加入五氧化二磷(0.81 g, 5.6 mmol)。冰浴下, 缓慢加入干燥的DADN-d8(0.16 g, 0.5 mmol), 加料过程中控制温度低于20 ℃。加料完毕, 缓慢加热至60~70 ℃反应1 h。冷却至40 ℃以下, 倒入冰水混合物中焠灭反应, 放置过夜, 过滤析出的固体, 干燥, 得到HMX-d8白色固体, 产率80.2%。
m.p. 281.3 ℃ (DSC); UV-vis (acetone) λmax: 330.8 nm; 13C NMR (DMSO-d6, 150 MHz) δ: 63.20 (—CD2—); FT-IR (KBr, ν/cm-1): 3672, 3594, 2294, 1566, 1384, 1329, 1244, 1052; MS (APCI) m/z: 301.9 [M-D]-。
2.3.4 β氘代奥克托今(β-HMX-d8)制备在30~40 ℃下, 将制备得到的HMX-d8粉末溶于丙酮, 挥发结晶, 即得到β-HMX-d8产品。
3 结果与讨论 3.1 氘代乌洛托品(HMTA-d12)的合成及其结构表征 3.1.1 HMTA合成条件优化由于氘代多聚甲醛价格昂贵, 且不易购买, 实验中拟先以非氘多聚甲醛为原料, 对非氘代HMTA的合成条件进行探索研究。虽然HMTA已有大工业化生产, 但是实验室研究较少。由文献[15]可知, 反应温度和氨水的用量对HMTA的产率影响最大。本实验探究了反应温度和氨水用量对HMTA产率的影响, 为HMTA-d12的合成奠定了基础。
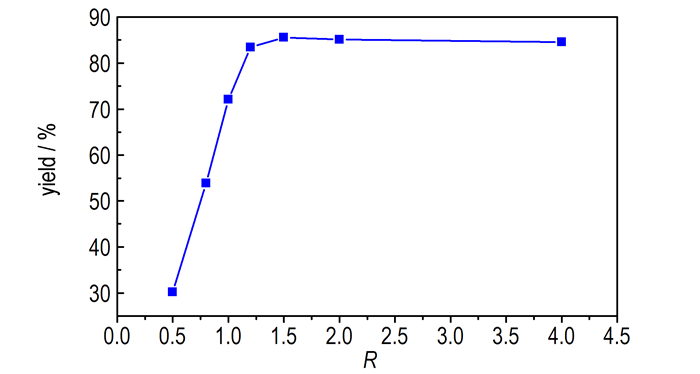
3.1.1.1 氨水的用量对合成HMTA产率的影响设定反应温度25 ℃, 反应时间40 h, 首先探究了氨水用量(氨水实际用量与理论用量的比值为R)对HMTA产率的影响, 结果见图 1。
|
图 1 氨水用量对乌洛托品产率的影响(R为氨水实际用量与理论用量的比值) Fig.1 Effects of ammonia dosages on the yields of HMTA(R is the molar ratio of actual ammonia dosage to theoretical ammonia dosage) |
由图 1可知, 随着氨水量增加, HMTA的产率逐步增加。当氨水实际用量与理论用量比(R)达1.2 :1时, 产率变化趋于平缓。当R为1.5:1时, 产率最高, 达85.6%。
3.1.1.2 反应温度对合成HMTA产率的影响设定反应时间40 h, 氨水实际用量与理论用量比为1.5:1, 探索反应温度对HMTA产率的影响, 结果见图 2。

|
图 2 温度对合成HMTA产率的影响 Fig.2 Effect of temperature on the yields of HMTA |
由图 2可知, 随着温度升高, HMTA的产率逐渐增加。当反应温度升到40 ℃左右时, HMTA的产率高达95.3%。若继续升高反应温度, HMTA的产率反而随之下降。原因在于, 温度过低时反应速度慢, 反应不充分, 反应产率较低; 而温度过高时, HMTA会发生部分水解, 反应产率也较低。
3.1.1.3 带水剂对合成HMTA产率影响HMTA在水中的溶解度很大, 难以采用溶剂萃取的方法将其从水溶液中提出。实验中, 可以采用蒸馏除去水的方法来得到固体HMTA产品。但如果蒸馏除水的温度较高的话, 则会导致所合成HMTA部分水解[16], 产率偏低。实验中, 拟通过加入带水剂的方式, 降低蒸馏温度, 从而提高反应产率。尝试加入乙醇、丙酮、甲苯、乙腈、氯仿或叔丁醇等可与水形成低沸点共沸物的有机溶剂, 研究了带水剂对合成乌洛托品产率的影响。结果表明, 叔丁醇可以大大降低蒸馏温度, 避免HMTA的水解, 产率高达95.3%。
3.1.2 HMTA-d12的合成参照HMTA最佳合成条件, 对HMTA-d12的合成进行了研究, 发现氘代多聚甲醛反应生成HMTA-d12的速度相对较慢, 需延长HMTA-d12的合成反应时间至60~70 h。在40 ℃下反应, 采用氨水实际用量与理论用量比为1.5:1, 利用叔丁醇带水的方法, 得到HMTA-d12产率最高达96.0%。
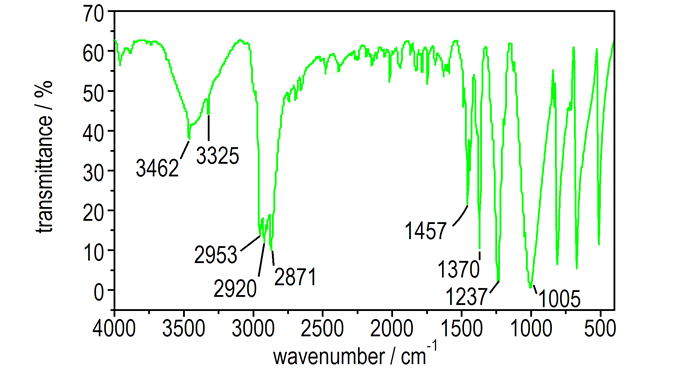
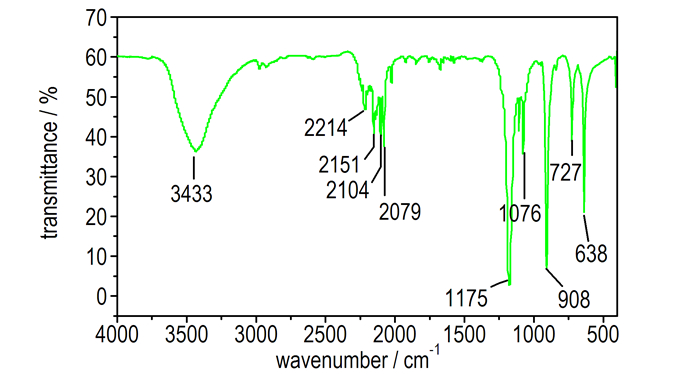
3.1.3 HMTA-d12结构表征 3.1.3.1 红外(FT-IR)光谱采用KBr压片, 得到非氘代乌洛托品(HMTA)和氘代乌洛托品(HMTA-d12)红外谱图(图 3和图 4)。图 3中, 2953, 2920, 2871, 1457, 1370 cm-1为HMTA的亚甲基C-H伸缩振动, 1237 cm-1为C—N键伸缩振动。氘代后, HMTA-d12的亚甲基C—D伸缩振动则蓝移到2214, 2151, 2104, 2079 cm-1处, 而C—N键骨架伸缩振动也受影响蓝移到1175 cm-1(图 4)。图 4中, 未见明显的C—H伸缩振动, 说明合成得到了HMTA-d12。
|
图 3 HMTA的傅里叶变换红外谱图 Fig.3 FT-IR spectrum of HMTA |
|
图 4 HMTA-d12的傅里叶变换红外谱图 Fig.4 FT-IR spectrum of HMTA-d12 |
从图 3和图 4可知, C—D的伸缩振动较C—H伸缩振动有所蓝移, 这是由于化学键振动波数γ与成键的两个原子质量存在如下关系[17]:
| $ \gamma = \frac{1}{{2{\rm{ \mathsf{ π} }}c}}\sqrt {\frac{k}{{\frac{{{m_1}{m_2}}}{{{m_1} + {m_2}}}}}} $ | (1) |
式中, c为光速, cm·s-1; k为力常数, N·m-1; m1为碳原子质量, kg; m2为D原子质量或者H原子质量, kg。由于D的质量较H的质量大, 所以C—D化学键振动波数要小于C—H化学键振动波数, 在谱图上显现为蓝移。
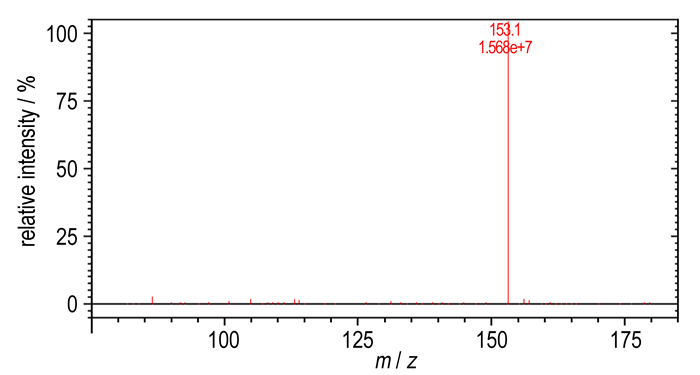
3.1.3.2 质谱(MS)采用APCI正离子模式, 测定了HMTA-d12的分子量, 如图 5所示。计算得到HMTA-d12的相对分子质量为152.2, 图 5中m/z=153.1为HMTA-d12的[M+H]+分子离子峰。
|
图 5 氘代乌洛托品的质谱图 Fig.5 APCI-MS spectrum of HMTA-d12 |
以HMTA为原料, 采用一锅法对DADN进行了合成研究[18]。首先, HMTA在醋酐作用下发生部分开环反应得到DAPT溶液[10]。该溶液不经分离纯化而直接用于下步硝解反应。实验中, 对其硝解温度进行了进一步探索。
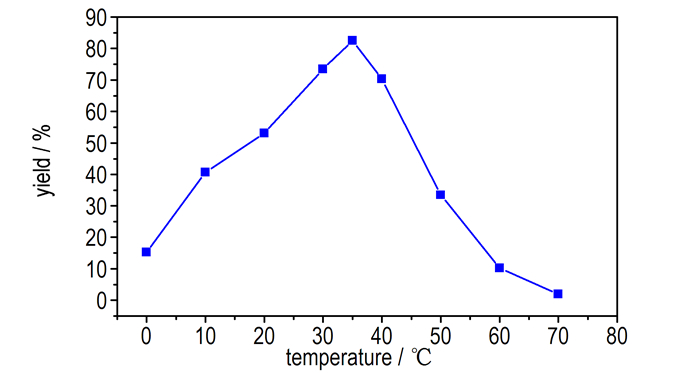
3.2.1.1 不同硝解温度对DADN产率的影响选取浓硫酸、硝酸钾与HMTA摩尔比为16.7:2.7:1, 反应时间为1 h, 探索了反应温度对DADN产率的影响, 结果见图 6。
|
图 6 硝解温度对DADN的产率影响 Fig.6 Effects of nitrolysis temperature on the yields of DADN |
如图 6所示, 随着温度升高, DADN的产率逐渐上升。当温度升至35 ℃左右时, 产率最高达82.0%, 继续升高反应温度, 则副反应增加, DADN的产率下降。
3.2.1.2 不同溶剂对合成DADN产率的影响虽然DADN的产率最高达82.0%(3.2.1.1), 但DAPT合成中涉及固液反应, 条件控制困难, 导致DADN产率波动性较大。为了避免DAPT合成中固液反应的问题, 尝试加入氯仿、乙酸、THF、乙腈或石油醚等不同有机溶剂来提高其传质和传热的效率, 达到稳定及提高产率的目的, 结果见表 1。
| 表 1 不同溶剂条件下的合成DADN产率 Tab.1 The yields of DADN synthesizied in different solvents |
由表 1可知, 采用氯仿、乙酸、乙腈和石油醚作为溶剂合成DAPT时, DADN的产率较低, 甚至为零。采用THF作为溶剂时, DADN的产率达69.7%, 且稳定性较好。THF溶剂法虽然操作简单, 产率稳定, 但较无溶剂法的产率偏低, 因而实验中仍然采用无溶剂法来合成DADN-d8。
3.2.2 DADN-d8合成在非氘代DADN的合成研究基础上, 以氘代乌洛托品为原料, 经乙酰化、硝解后合成得到DADN-d8, 产率达76.0%。
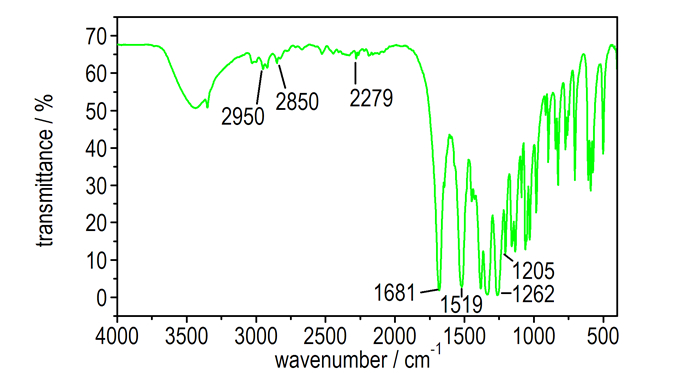
3.2.3 DADN-d8结构表征 3.2.3.1 红外(FT-IR)光谱采用KBr压片, 得到DADN-d8的红外谱图(图 7)。图 7中, 2950, 2850 cm-1为DADN-d8中甲基C—H伸缩振动, 1382 cm-1为甲基C—H弯曲伸缩振动, 2279 cm-1为DADN-d8中亚甲基C—D伸缩振动, 1681 cm-1为乙酰基C=O伸缩振动, 1205, 1158, 1134 cm-1为C—N伸缩振动, 1519, 1262 cm-1为—NO2伸缩振动峰。从红外来看, 乙酰化和硝解反应成功引入了乙酰基和硝基。
|
图 7 DADN-d8的傅里叶变换红外谱图 Fig.7 FT-IR spectrum of DADN-d8 |
采用APCI负离子模式, 测定了DADN-d8的分子量(图 8)。计算DADN-d8的分子量为298.2, 图 8中295.9为DADN-d8的[M-D]-分子离子峰, 297.1为DADN-d8的[M-H]-分子离子峰。从质谱数据来看, 所合成化合物的分子量正确。

|
图 8 DADN-d8质谱图 Fig.8 APCI-MS spectrum of DADN-d8 |
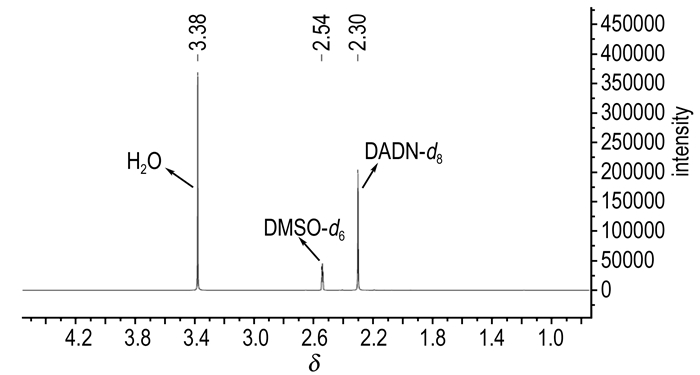
以DMSO-d6为溶剂, BRUKER 600核磁仪检测, 得到所合成DADN-d8的1H NMR图谱(图 9)。图 9中, 2.54处为DMSO-d6溶剂峰, 3.38处为水峰, 2.30处为DADN-d8的CH3CO—质子信号峰。由于亚甲基的氢已均被氘代, 因此核磁图中并未见到DADN-d8中亚甲基的质子信号。1H NMR图谱中, 除了溶剂和水峰以外, 只有DADN-d8的样品峰, 说明合成DADN-d8的纯度较高。
|
图 9 DADN-d8核磁共振氢谱 Fig.9 1H NMR spectrum of DADN-d8 |
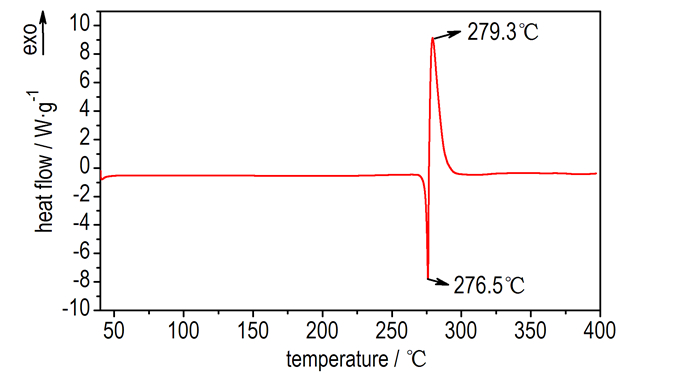
在N2气氛下, 升温速率10 K·min-1, 对DADN-d8进行TG和DSC测试(图 10和图 11)。图 10中, 276.5 ℃处为DADN-d8的熔融吸热峰, 279.3 ℃为其分解放热峰。从TG-DTG来看, DADN-d8只有一个失重阶段(250~350 ℃), 失重率为94.8%, 在295.1 ℃处达到最大分解速率(图 11)。
|
图 10 DADN-d8的DSC曲线(10 K·min-1, N2气氛) Fig.10 DSC curve of DADN-d8 (10 K·min-1, N2 atmosphere) |

|
图 11 DADN-d8的TG-DTG曲线(10 K·min-1, N2气氛) Fig.11 TG-DTG curve of DADN-d8 at 10 K·min-1 and N2 atmosphere |
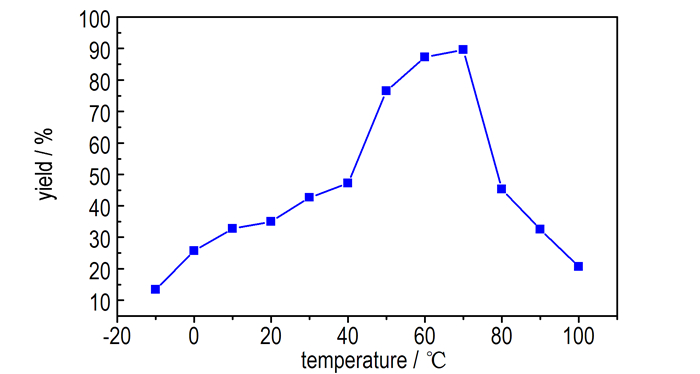
采用N2O5或无水硝酸来硝化DADN, 通常可以高产率地合成HMX[19-21]。本实验拟选用无水硝酸/P2O5来硝化DADN合成HMX。实验中, 研究了硝化温度对该反应的影响(图 12)。图 12表明, 采用无水硝酸/P2O5为硝化试剂, 最佳硝化温度为60~70 ℃, 产率达89.6%。
|
图 12 硝化温度对HMX产率的影响 Fig.12 Effects of nitration temperatures on the yields of HMX |
采用无水硝酸/P2O5为硝化试剂, 在60~70 ℃条件下硝化DADN-d8即可合成得到HMX-d8, 产率达80.2%。
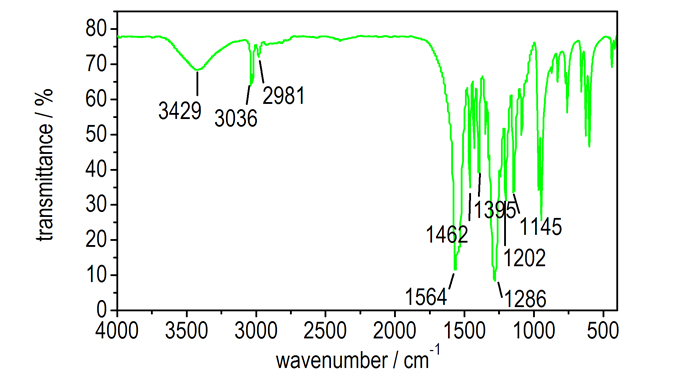
3.3.3 结构表征及分析 3.3.3.1 红外(FT-IR)采用KBr压片, 得到HMX和HMX-d8红外谱图(图 13和图 14)。图 13中, 3036 cm-1和2981 cm-1为HMX的亚甲基C—H伸缩振动峰, 1564 cm-1和1286 cm-1为—NO2的伸缩振动和弯曲振动峰; 图 14中, 氘代后HMX的亚甲基C—D伸缩振动峰位于2294, 1566 cm-1和1244 cm-1为HMX-d8中—NO2的伸缩振动和弯曲振动峰, 1172, 1150, 1137 cm-1和1052 cm-1为HMX-d8中C—N的伸缩振动。HMX-d8的红外谱图中, 未见明显的C—H伸缩振动峰, 说明HMX中亚甲基H几乎被全部氘代(图 14)。
|
图 13 HMX的傅里叶变换红外谱图 Fig.13 FT-IR spectrum of HMX |

|
图 14 HMX-d8的傅里叶变换红外谱图 Fig.14 FT-IR spectrum of HMX-d8 |
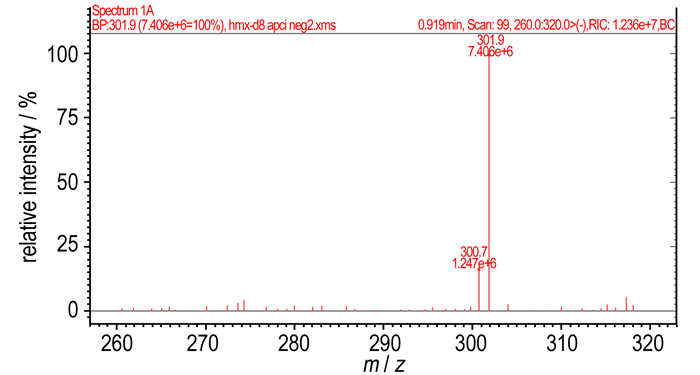
采用APCI负离子模式, 测定了HMX-d8的分子量(图 15)。计算HMX-d8的分子量为304.1, 图 15中301.9为HMX-d8的[M-D]-分子离子峰。从质谱数据可以确定所合成的HMX-d8分子量正确。
|
图 15 氘代奥克托今(HMX-d8)质谱图 Fig.15 APCI-MS spectrum of HMX-d8 |
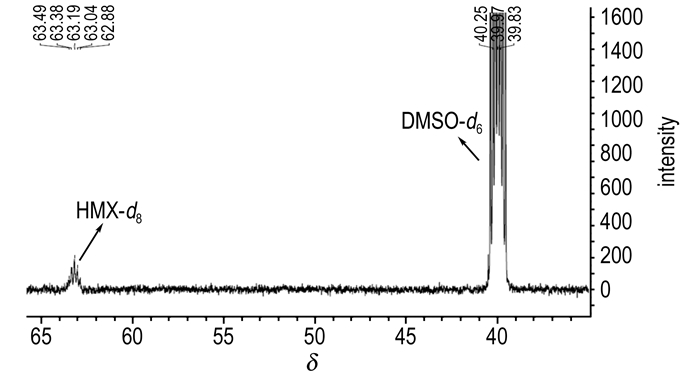
以DMSO-d6为溶剂, BRUKER 600核磁仪检测, 得到所合成HMX-d8的13C NMR图谱(图 16)。由于C—D的耦合作用, HMX-d8的核磁碳谱中产生了一个五重峰的碳信号(δ=63.20), 并且其化学位移与非氘代HMX的化学位移一致[22]。图 16中未见RDX等副产物的碳信号。
|
图 16 氘代奥克托今(HMX-d8)核磁共振碳谱 Fig.16 13C NMR spectrum of HMX-d8 |
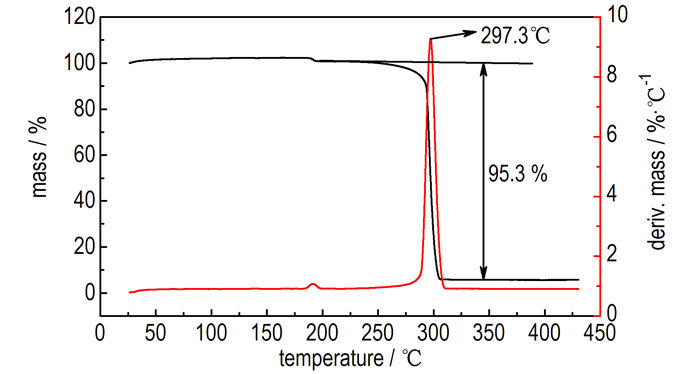
在N2气氛下, 升温速率10 K·min-1, 对HMX-d8进行了TG和DSC测试(图 17和图 18)。图 17中, 281.3 ℃处为HMX-d8的熔融吸热峰, 286.0 ℃处为其放热分解峰。从TG-DTG来看, HMX-d8只有一个失重阶段(232~336 ℃), 失重率为95.3%, 在279.3 ℃处达到最大分解速率(图 18)。

|
图 17 HMX-d8的DSC曲线(10 K·min-1, N2气氛) Fig.17 DSC curve of HMX-d8at 10 K·min-1 and N2 atmosphere |
|
图 18 HMX-d8的TG-DTG曲线(10 K·min -1, N2气氛) Fig.18 TG-DTG curve of HMX-d8 at 10 K·min -1 and N2 atmosphere |
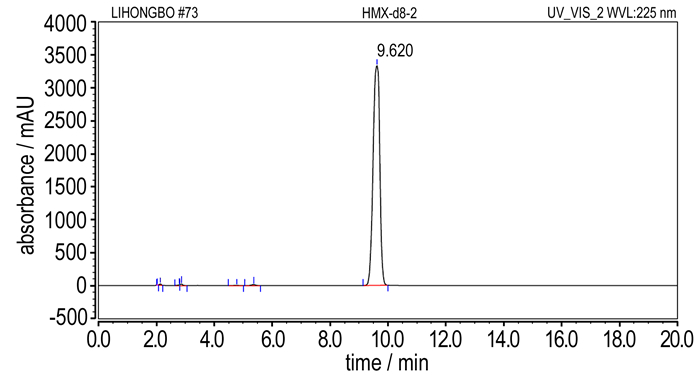
参考文献方法[23-24], 选取流动相甲醇:水=55:45(体积比), 流速1 mL·min-1, 检测波长230 nm, 进样量10 μL, C18液相色谱柱(4.6 μL, 4 mm×250 mm), 对HMX-d8进行了HPLC测试(图 19)。从图 19来看, 所合成的HMX-d8中没有RDX等副产物, 面积归一法计算得到HMX-d8的纯度为99.27%。
|
图 19 HMX-d8高效液相色谱图 Fig.19 HPLC spectrum of HMX-d8 |
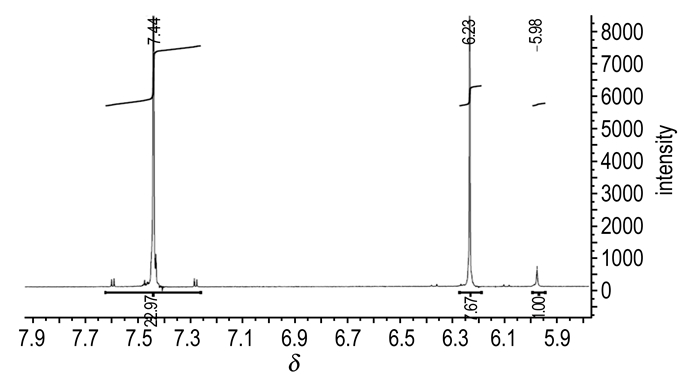
以马来酸酐为内标, 采用核磁法, 对HMX-d8的氘代率进行了测定。精确称量HMX-d8 (20.49 mg)和马来酸酐(2.04 mg), 溶于DMSO-d6, 测试所得1H NMR图谱见图 20。图 20中, 5.98处为HMX-d8分子中未氘代的氢质子信号, 7.44处为马来酸酐的氢质子信号, 而6.23处为马来酸的氢质子信号。
|
图 20 马来酸酐和HMX-d8混合物核磁共振氢谱 Fig.20 1H NMR spectrum of the mixture of HMX-d8 and maleic anhydride |
参考文献[25], 采用公式(2)计算氘代率:
| $ D = 1 - \frac{{{S_2}{m_1}{n_1}{M_2}}}{{{S_1}{M_1}{m_2}{n_2}}} $ | (2) |
式中, D为氘代率; S1为内标物质积分面积; m1为内标物质质量, g; n1为内标物质氢的个数; M1为内标物质相对分子质量, g·mol-1; S2为样品物质积分面积; m2为样品物质质量, g; n2为样品物质氢的个数; M2为样品物质相对分子质量, g·mol-1。
以HMX-d8分子中的氢质子信号峰面积积分为1.00, 得到顺丁烯二酸酐氢质子信号峰的积分面积为22.97, 计算HMX-d8的氘代率为99.75%, 说明了在反应中几乎没有发生H/D交换。
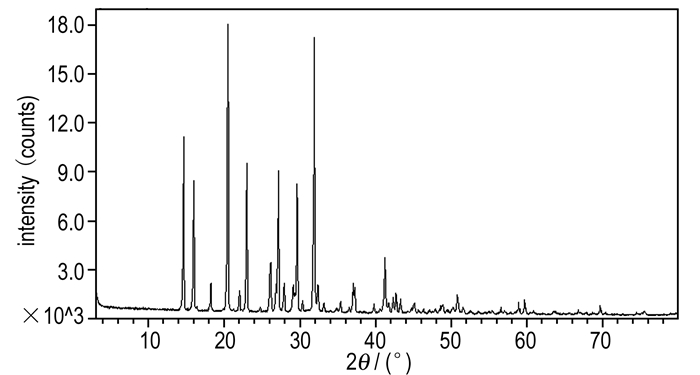
3.4 β-HMX-d8晶型表征通过丙酮转晶后, 所得到HMX-d8产品的XRD图谱见图 21, 与标准卡JCPDS 42-1768一致。经与标准卡片对比, 确认所得HMX-d8产品为纯β-晶相。
|
图 21 β-HMX-d8的XRD谱图 Fig.21 XRD pattern of β-HMX-d8 |
(1) 以氘代多聚甲醛为原料, 通过DADN-d8中间体, 成功合成得到氘代的HMX-d8产品, 总产率58.5%, 并采用丙酮重结晶法即可得到纯β-晶相的HMX-d8产品。
(2) 在HMTA-d12的合成中, 采用叔丁醇为带水剂, 可以减少HMTA-d12的分解, HMTA-d12最高产率达96.0%。
(3) DSC/TG测定HMX-d8的分解温度为286.0 ℃, HPLC测定HMX-d8的纯度达99.27%, 核磁内标法测定HMX-d8的氘代率高达99.75%。
(4) HMX-d8合成中, 除氘代多聚甲醛外, 均采用非氘代溶剂和试剂, 说明在选定的合成条件下H/D交换反应发生几率低。
| [1] |
吕连营, 欧育湘, 王建龙. 超酸硝化法合成六硝基六氮杂异伍烷[J].
精细化工, 2004, 21(5): 321-323. LÜ Lian-ying, OU Yu-xiang, WANG Jian-long. Synthesis of hexanitrohexaazaisowurtzitane by nitration with super acids[J]. Chinese Journal of Fine Chemicals, 2004, 21(5): 321-323. |
| [2] |
赵信岐, 方涛, 孙成辉. 六硝基六氮杂异伍兹烷制备工艺研究开发新进展[J].
兵工学报, 2004, 25(3): 354-357. ZHAO Xin-qi, FANG Tao, SUN Cheng-hui. Researche and development of HNIW synthesis[J]. Acta Armamentarii, 2004, 25(3): 354-357. |
| [3] |
欧育湘, 刘进全, 王才. 三级胺及酰胺硝解研究进展[J].
化学通报, 2004, 67(8): 560-565. OU Yu-xiang, LIU Jin-quan, WANG Cai. Recent development of nitrolysis of tertiary amines and amides[J]. Chinese Journal of Chemistry, 2004, 67(8): 560-565. |
| [4] |
王才, 欧育湘, 陈博仁, 等. 2, 14-二氧代-5, 5, 11, 11-四硝基-3, 7, 9, 13-四氧杂十五烷的合成与性能研究[J].
火炸药学报, 1998, 21(3): 27-28. WANG Cai, OU Yu-xiang, CHEN Bo-ren, et al. Synthesis and properties of 2, 14-dioxo-5, 5, 11, 11-tetranitro-3, 7, 9, 13-tetraoxapentadecane[J]. Chinese Journal of Explosives & Propellants, 1998, 21(3): 27-28. |
| [5] |
Dick J J. Stress-time profiles in low density HMX[J].
Combustion and Flame, 1987, 69(3): 257-262. DOI:10.1016/0010-2180(87)90119-2 |
| [6] |
William L. Process of making impacting-sensitive explosive alpha-HMX: US 5268469[P], 1993.
|
| [7] |
Yadollah B, Mohammad M A M. Silca sulfuric acid/HNO3 as novel Heterogeneous system for the nitrolysis of DADN to HMX under mild conditions[J].
The Bulletin of the Korean Chemical Society, 2012, 33(11): 3551-3553. DOI:10.5012/bkcs.2012.33.11.3551 |
| [8] |
William L. Manufacture of high-purity HMX in high yield: US 5124493[P], 1992.
|
| [9] |
Chen Ju, Wang Shao-Fang. Use of NMR spectrometry for studying the acetolysis of hexamethylenetetramine. Ⅰ. the reation of TAT formation form DAPT[J].
Propellants, Explosives, Pyrotechnics, 1984, 9(2): 58-63. DOI:10.1002/(ISSN)1521-4087 |
| [10] |
李全良. 奥克托今合成工艺研究[D]. 太原: 中北大学, 2007.
LI Quan-liang. Study on the technology of synthesis of HMX[D]. Taiyuan: North University of China, 2007. |
| [11] |
朱家瑄, 程玉芬, 沈今川. 单晶中子衍射法确定重晶石中氧的位置[J].
科学通报, 1965, 10(8): 738-740. ZHU Jia-xuan, CHENG Yu-fen, SHEN Jin-chuan. Single crystal neutron diffraction method to determine the position of the oxygen in the barite[J]. Cinese Science Bulletin, 1965, 10(8): 738-740. |
| [12] |
徐尧, 王虹, 李建, 等. 中子衍射法测量TATB基PBX单轴压缩的内应力研究[J].
含能材料, 2017, 25(10): 860-865. XU Yao, WANG Hong, LI Jian, et al. Internal stress measurement during uniaxial compression for TATB base PBX by neutron diffraction[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2017, 25(10): 860-865. DOI:10.11943/j.issn.1006-9941.2017.10.012 |
| [13] |
曾贵玉, 李长智. 小角散射(SAS)技术在含能材料结构表征中的应用[J].
含能材料, 2005, 13(2): 128-131. ZENG Gui-yu, LI Chang-zhi. Applications of small angel scattering(SAS) technique in the structure measuring of energetials[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2005, 13(2): 128-131. |
| [14] |
陈东风, 刘蕴韬, 韩松柏. 中国先进研究堆中子散射谱仪建设现状和展望[J].
中国材料进展, 2009, 28(12): 1-5. CHEN Dong-feng, LIU Yun-tao, HAN Song-bai. Progress of neution scattering project on CARR[J]. Chinese Journal of Materials china, 2009, 28(12): 1-5. |
| [15] |
王彰九, 成志远. 乌洛托品酰化反应的热动力学研究[J].
化学通报, 1988, 35(5): 35-38. WANG Zhang-jiu, CHENG Zhi-yuan. Thermokinetic study of urotropine acylation[J]. Chinese Journal of Chemistry, 1988, 35(5): 35-38. |
| [16] |
杨永惠. 乌洛托品合成方法及其探讨[J].
中国药学杂志, 1960, 8(1): 24-26. YANG Yong-hui. Synthetic methods and explore methenamine[J]. Chinese Pharmaceutical Journal, 1960, 8(1): 24-26. |
| [17] |
张林, 高文德, 肖淑兴, 等. 新法氘代溴苯-d5的合成表征[J].
化学世界, 2000, 41(2): 68-70. ZHANG Lin, GAO Wen-de, XIAO Shu-xing, et al. A novel method for synthesis and characterization of deuterated bromobenzene-d5[J]. Chemical World, 2000, 41(2): 68-70. |
| [18] |
Coburn M D, Ott D G. A convenient synthesic of nitrogen-15 and deuterium labelled octahydro-1, 3, 5, 7-tetranitro-1, 3, 5, 7-tetrazocine(HMX)[J].
Jounal of Labelled Compounds and Radiopharmaceuticals, 1981, 18(10): 1423-1427. DOI:10.1002/jlcr.v18:10 |
| [19] |
Suryanarayana B, David I W, Joseph R A, et al. Deuterium kinetic isotope effect in the thermal decomposition of 1, 3, 5-trlnitro-l, 3, 5-triazacyciohexane and 1, 3, 5, 7-tetranltro-l, 3, 5, 7-tetraazacyclooctane: Its use as an experimental probe for their shock-induced chemistry[J].
Journal of Physical Chemistry, 1986, 90(17): 4126-4131. DOI:10.1021/j100408a058 |
| [20] |
李伟明. 酸酐法生产HMX工艺研究[D]. 太原: 中北大学, 2009.
LI Wei-ming. Study on process of HMX by acetic anhydride method[D]. Taiyuan : North University of China, 2009. |
| [21] |
曹宇. 基于N2O5合成HMX工艺研究[D]. 南京: 南京理工大学, 2013.
CAO Yu. Study on thesynthesis of HMX with N2O5[D]. Nanjing: Nanjing University of Science & Technology, 2013. |
| [22] |
Suryanarayana B, Theodore A, Joseph R A. Application of 13C and 15N NMR spectrosopy to structural studies on nitramines[J].
Magnetic Resonance in Chemistry, 1981, 16(1): 52-56. |
| [23] |
王秀菊, 赵文深, 任特生. 综合法生产奥克托今/黑索今新工艺产品成分的高效液相色谱分析[J].
北京化工学院学报, 1988, 8(2): 110-116. WANG Xiu-ju, ZAHO Wen-shen, REN Te-sheng. Composition determination of HMX/RDX mixture obtained from the new combination process by HPLC[J]. Journal of Beijing Institute of Technology, 1988, 8(2): 110-116. |
| [24] |
张敏. RDX和HMX的大气压电喷雾电离质谱分析[J].
火炸药学报, 2006, 29(1): 77-80. ZHANG Min. Analysis of the mixture of RDX and HMX by the HPLC-ESI-MS[J]. Chinese Journal of Explosives & Propellants, 2006, 29(1): 77-80. |
| [25] |
胡睿, 熊晓玲, 阚文涛. 氘代有机物的表征技术[J].
化学试剂, 2013, 35(4): 329-332. HU Rui, XIONG Xiao-ling, KAN Wen-tao. Characterization techniques of deuterated organic compounds[J]. Chemical Reagents, 2013, 35(4): 329-332. |
Based on the synthesis technology of non-deuterated HMX using paraformaldehyde as raw material, β-deuterated octagon (β-HMX-d8) was successfully synthesized.




