2. 可靠性与环境工程技术重点实验室北京卫星环境工程研究所,北京 100094
含能离子化合物是一类分子结构中含有N—N和C—N键的离子型含能材料,它具有生成焓高[1]、密度较高、极性强、不挥发,毒害性小,对环境较友好等优点[2]。一般来说材料的能量和安全性能是对立的,随着材料的高能化,其安全性能有所降低。含能离子化合物能够有效地解决含能材料在高能量和安全性方面不协调的问题,通过阴阳离子的合理组合制备出综合性能优良的含能离子化合物,满足先进武器装备对含能材料的要求。近年来,含能离子化合物作为一类独特的高能材料受到了广泛的关注。
胍基含能离子化合物是一类含有胍基结构阳离子的含能离子化合物。胍基阳离子主要为胍、氨基胍、二氨基胍和三氨基胍,阴离子主要为含氮量较高的三唑、四唑环和四嗪环。胍基离子化合物燃烧产气量大,残渣少,主要气体产物为无毒的氮气、水、二氧化碳等,可以调节燃速,降低火焰温度,在火炸药[3]、推进剂[4]、气体发生剂[5]等方面具有良好的发展和应用前景。
本文主要对近年来胍基含能离子化合物的合成方法、性能及其应用情况进行综述。
2 胍基含能离子化合物的合成方法胍基含能离子化合物的合成方法与一般离子化合物的合成方法[6]类似,主要包括一步合成法和两步合成法。
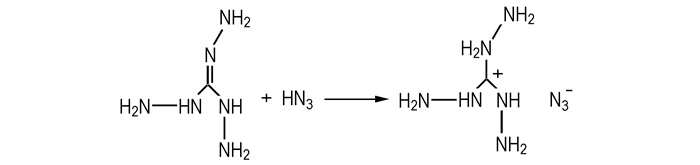
2.1 一步合成法一步合成法就是通过酸碱中和反应一步合成胍基含能离子化合物,此方法操作经济简便,没有副产物,产品易纯化。胍(氨基胍,二氨基胍,三氨基胍)为有机碱,他们能够直接和质子酸反应生成胍基含能盐。余天祥[7]等利用一步合成法,在非水条件下,将三氨基胍与叠氮酸直接反应制备了叠氮酸三氨基胍(TAZ),合成方法见Scheme 1。
|
Scheme 1 Synthetic route of TAZ |
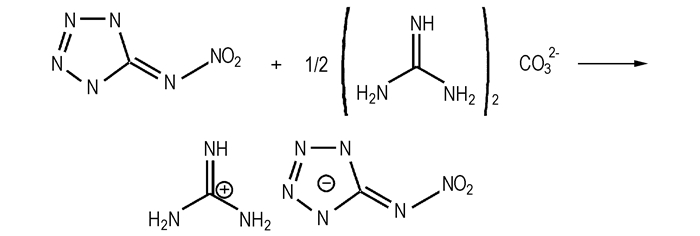
碳酸胍(碳酸氢胍)也能和质子酸反应生成胍基含能盐。如5-硝亚氨基四唑胍[8]的合成:将等物质的量的5-硝亚氨基四唑和碳酸胍(碳酸氨基胍)加入到热水中,发生中和反应,反应完全后,冷却至室温,过滤,烘干得到目标产物,见Scheme 2。
|
Scheme 2 Synthetic route of 5-nitroiminotetrazolate guanidine |
多数胍基含能盐的都是通过两步法合成的。首先分别合成胍卤盐GX(X=Cl、Br)和阴离子的金属盐MY(或铵盐NH4Y),然后GX与MY(NH4Y)发生离子交换反应生成胍基含能离子化合物GY(或NH4Y),见Scheme 3。常用的金属盐MY主要有AgY、BaY等,反应产生的金属卤化物沉淀或NH4、HX气体很容易除去。

|
Scheme 3 Synthesis of guanidine enegertic salts by ion-exchange method |
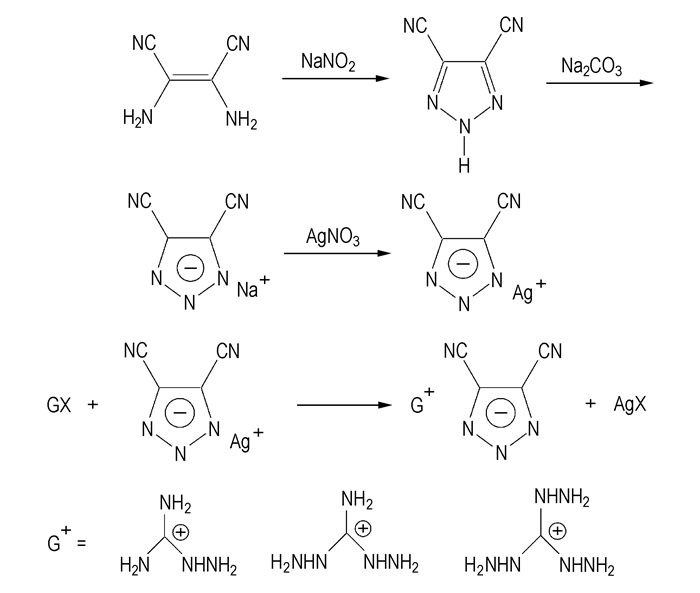
Margaret[9]等以2, 3-二氨基-2-丁烯二腈为原料,先合成4, 5-二氰基-1, 2, 3-三唑银盐,然后银盐分别与胍(氨基胍,二氨基胍,三氨基胍)卤盐反应合成出了相应的胍盐,具体路线间见Scheme 4。此外,硝基氨基胍、二氰胺胍、3-硝基-1, 2, 4-三唑-5-酮胍等[10-12]都是通过两步合成法合成的。
|
Scheme 4 Synthetic route of 4, 5-dicyano-1, 2, 4-triazole salt |
本课题组合成的六烷基胍含能离子化合物也是通过两步合成法合成的,首先对胍基阳离子进行功能化,在三个氮原子上引入烷基形成六烷基胍溴盐,然后六烷基胍溴盐与3-硝基1, 2, 4-三唑-5-铜、4, 5-二氰基-1, 2, 4-三唑和二氰胺的银盐反应生成六烷基胍含能离子化合物,并对它们进行了结构表征和性能测试。
3 胍基含能离子化合物的性能 3.1 熔点熔点是评价胍基含能离子化合物特性的一个关键参数,它是离子化合物内部阴阳离子微观结构及阴阳离子相互作用强弱的外在表现,是决定含能离子化合物实际应用进程的主要因素之一。研究离子化合物的组成与其熔点的关系具有重要意义。
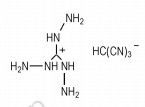
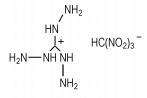
胍基含能离子化合物的熔点受离子键强弱、离子半径大小等因素的影响。化合物离子键越强,破坏离子键需要的能量越大,熔点越高。三氨基胍三氰基甲烷(Scheme 5)的熔点(182 ℃)比三氨基胍三硝基甲烷(Scheme 6)的熔点(84 ℃)高[13-14]。这是因为硝基和氰基为吸电子基团,它们作用于阴离子上使阴离子电荷中心向外偏移,与阳离子的离子键强度变小,而硝基的吸电子效应大于氰基,电荷偏移位移更大,因此含硝基的胍盐熔点低于含氰基的胍盐的熔点。
|
Scheme 5 |
|
Scheme 6 |
离子半径对熔点也有影响,当阴离子固定时,随着胍基中N原子上取代氨基的增加,阳离子半径变大,阴阳离子间距离变大,相互作用力减弱,熔点降低,见表 1,随着胍基中取代氨基的增加,2-甲基-5-硝氨基四唑胍盐(G_2MNAT、AG_2MNAT、DAG_2MNAT、TAG_2MNAT)的熔点逐渐降低。
3.2 密度密度是衡量高能化合物的一个重要指标。文献[7, 9, 13, 14, 16, 20, 21]报道的胍基含能离子化合物的密度普遍为1.5~1.8 g·cm-3。含能离子化合物的密度与阴阳离子的结构有很大关系,主要受离子的对称性和分子间作用力的影响,结构上微小的变化会引起密度的改变。
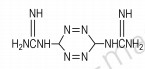
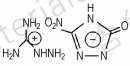
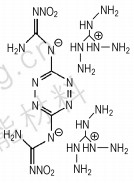
具有对称结构的化合物往往有着较高的密度,如Scheme 7[15],密度高达1.90 g·cm-3,这是由于它具有对称结构并且是单体分子,因此密度较高。分子间氢键作用可以增加胍基含能离子化合物的密度,杨利等[16]合成的三硝基1,2,4-三唑-5酮氨基胍(Scheme 8)密度为1.69 g·cm-3,在分子中引入—NO2基团后,—NO2和其他分子上氢形成氢键,密度较高。王伯周等[15]合成的3,6-双胍基-1,2,4,5-四嗪三氨基胍(Scheme 9)整个分子结构对称,并且分子间存在氢键,密度达到1.76 g·cm-3。
|
Scheme 7 |
|
Scheme 8 |
|
Scheme 9 |
胍基含能离子化合物的密度也与阴阳离子有关,见表 1,随着胍基中N原子上取代氨基的增加,化合物的密度逐渐降低,这是由于随着阳离子体积变大导致分子间作用力变小,密度逐渐变小。
3.3 能量性能表征化合物能量特征的参数主要有标准摩尔生成焓、爆速、爆压、产气量和产气的平均分子质量。胍基含能离子化合物分子结构中N含量高,C、H的含量低,容易达到氧平衡,燃烧爆炸时放气量大,产物主要为氮气、水、二氧化碳等小分子气体。
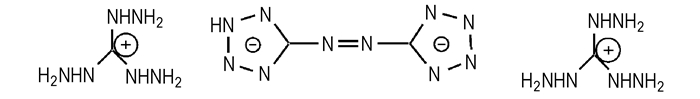
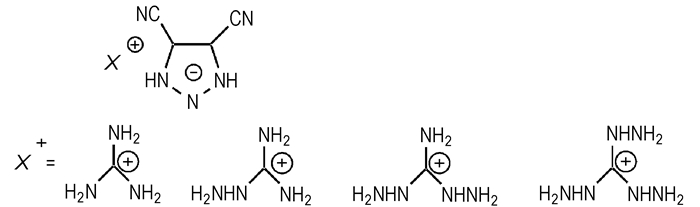
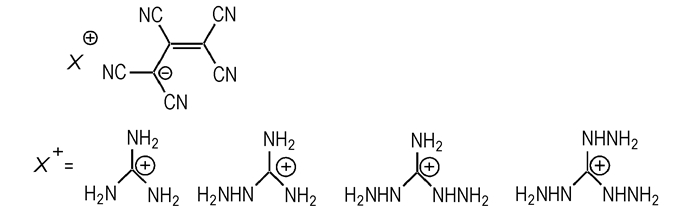
文献[17]报道的生成焓最高的胍基含能盐为偶氮四唑三氨基胍TAGZT(Scheme 10),生成焓为1074 kJ·mol-1,爆速为9050 m·s-1(RDX为8882 m·s-1),标准状况下单位质量成气量为981 mL·g-1 [18],具有很高的能量。在阴离子中引入氰基、叠氮基等基团可以显著提高化合物的标准摩尔生成焓,见Scheme 11,其标准摩尔生成焓在400~ 820 kJ·mol-1之间;多氰基胍基含能盐[19](Scheme 12)标准摩尔生成焓在600~920 kJ·mol-1之间。Michael等[13]合成的三氨基胍三硝基甲烷(Scheme 6)密度为1.689 g·cm-3,生成焓247.04 kJ·mol-1,爆压33 GPa,爆速8982 m·s-1。之所以会有如此高的能量,是因为当烷烃带有多个强吸电子基团时,形成了活泼氢而显酸性,与三氨基胍结合成高能量高稳定性的强氧化性盐;并且分子中三个硝基可以使化合物更容易达到氧平衡,燃烧放热量更大。
|
Scheme 10 |
|
Scheme 11 |
|
Scheme 12 |
胍基阳离子对化合物的能量性能也有影响,从表 1可以看出,随着胍基中N原子上取代氨基的增加,化合物含氮量增加,其生成焓、爆压、爆速也有所增加。
4 胍基含能离子化合物的应用 4.1 气体发生剂气体发生剂主要分为叠氮化物型气体发生剂和非叠氮化物型气体发生剂。叠氮化物型气体发生剂具有燃烧温度低、气体产物为无毒的氮气等优点,但制备叠氮化合物的重要原料叠氮化钠毒性较大,限制了其生产能力和用途,开发环保、廉价、实用和多品种的气体发生剂具有重要意义。
胍基含能离子化合物具有热稳定性好、产气量大、燃烧产物无渣或少渣、原料易得并且对环境友好等优点,在气体发生剂领域具有很好的应用。这类气体发生剂主要包括硝基胍(NQ)、硝酸胍(GN)、硝酸三氨基胍(TAGN)、二硝酰胺胍(GDN)和偶氮四唑二胍(GZT)和偶氮四唑二氨基胍(AGAT)等。
表 2列举的几类该气体发生剂的配方及性能可以看出,几种气体发生剂配方的燃烧产物均为H2O、N2、CO2等无毒无害气体,爆温大多都在2000 K以上。在TAGN配方中,燃速高达38.9 mm·s-1,TAGN (Scheme 13a)不吸湿、热安定性好,另外它还有冷却剂的作用,适合用于燃气推动作功、缓冲着陆等场合。偶氮类气体发生剂GZT含氮量高,燃速较慢、燃烧温度也在2000 K以上,但其产气量大,可以达到4 mol/100 g,在高温下体积更大,作功能力强,可以用于航天等要求气体量大,允许温度较高的场合。GDN(Scheme 13b)可以应用于燃气发生剂配方中,具有产气量大、无残渣、燃温低、燃速足够快,产生的气体无毒等优点。
| 表 2 胍类气体发生剂配方及性能[22] Tab.2 Formulations and properties of guanidine derivatives gas generating compositions |
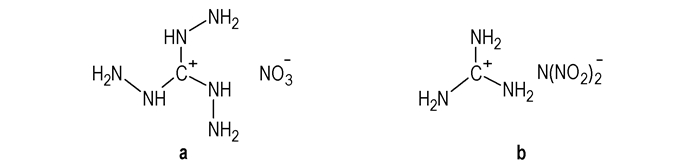
|
Scheme 13 |
目前航天推进剂的主要组分是肼类化合物及它们的甲基化衍生物,这些化合物是强致癌物,吸入或皮肤接触都会对人体产生危害。随着航天事业的发展,对新型推进剂的研制提出了较高的环保需求[23]。另外,低特征信号、燃速可调节也是新型推进剂系统所要满足的性能要求。
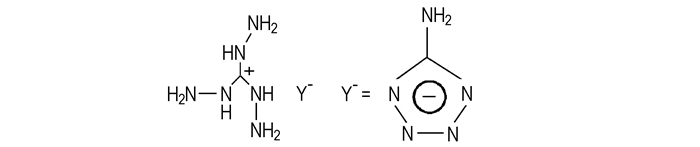
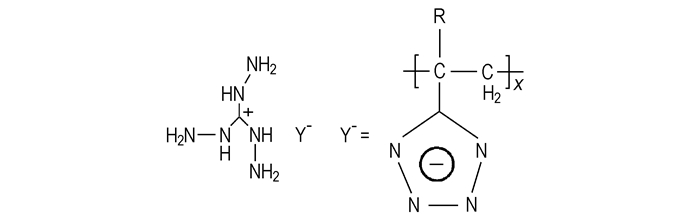
胍基含能离子化合物密度高、热稳定、不挥发、物性(密度、黏度)可通过调节它们的阴阳离子的组成来调节;它的强极性也可用于推进剂的燃速调节及弹道调节技术,特征信号也较低。因此,胍基含能离子化合物是一种有良好应用前景的推进剂材料。如5-氨基四唑三氨基胍(Scheme 14)[24]和5-聚乙烯基四唑三氨基胍(Scheme 15)[25],它们含氮量高,产气量大,是推进剂的主要组分,常用的配方为:可燃剂主要为5-氨基四唑三氨基胍、5-聚乙烯基四唑三氨基胍,氧化剂可选择高氯酸钠、高氯酸钾、硝酸铵等,粘合剂可选择聚丁二烯酸、硝化纤维、聚酯等。
|
Scheme 14 |
|
Scheme 15 |
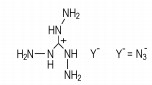
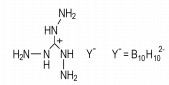
叠氮酸三氨基胍(TAZ)(Scheme 16)[26]氮含量高达85.7%,分子结构N3-在250 ℃迅速分解,放出367 kJ·mol-1键能,而且放出大量的氮气,燃烧温度为2935 ℃,是提高比冲、降低燃烧温度的理想组分之一。硼氢三氨基胍(Scheme 17) [27]为白色晶体,是无氧高能含能化合物,密度1.22 g·cm-3,5 s爆发点252 ℃,热稳定性好。撞击感度测试:2 kg落锤在3 cm处连续10次落下,未发生爆炸,感度低于叠氮化铅(2 cm),爆热为5700 kJ·kg-1,接近叠氮化铅爆热值(1500 kJ·kg-1)的四倍。硼氢三氨基胍通过释放自身的内能无需添加任何氧化剂而燃烧,有正的生成焓,可直接作推进剂,也可与氧化剂如高氯酸钾、高氯酸铵、硝酸三氨基胍作为混合推进剂使用。
|
Scheme 16 |
|
Scheme 17 |
目前常用的一些炸药感度高,安全性差。如果要把胍基含能离子化合物用作炸药就要求它们具有更高的能量和较好的稳定性,利用离子化合物可设计的特点,选择适当的阴阳离子,使得含能化合物具有更好的热稳定性、低挥发性以及更高的密度等特点。例如, 要使含能离子化合物具有更高的能量,可以用含有更多氮原子的环取代咪唑(三唑、四唑、四嗪、偶氮四唑等)以增加其能量,还可以用含能量高的基团—CN,—NH2,—N3,—NO2取代氢或烷基侧链。
偶氮四唑类胍盐具有生成焓高、不吸湿、爆压低、产气量大等特点,在高性能炸药方面具有潜在优势。徐松林[28]和Hiske[29]对偶氮四唑类胍盐的爆炸性能进行了研究,结果见表 3。
偶氮四唑类含能化合物的爆压较低、成气量大;在密度较低的情况下,部分化合物的爆速仍很高,如TAGZT密度为1.602 g·cm-3, 其计算爆速高达9678 m·s-1,在不含氧或硝基的情况下,却具有爆炸性能。其中GZT感度较低,与钝感炸药TATB相当(撞击感度大于320 cm,摩擦感度为零[28]),有望作为高能钝感炸药;TAGZT生成焓和爆速都很高,但感度较差。因此,偶氮四唑类高氮含能化合物是一类新型炸药—有机无氧炸药的典型代表。
5 展望从国内外研究可以看出,胍基含能离子化合物热稳定性好,密度较高,同一系列推进剂组分兼容性良好;离子化合物的强极性可用于推进剂的燃速调节及弹道调节技术[30];其生成焓高,产气量大,燃烧无残渣和气体产物无毒害等特点使它们在高性能炸药和无烟烟火技术方面具有潜在优势[28]。
目前胍基含能离子化合物的合成研究主要是通过分子设计和修饰,分别对阴阳离子进行功能化,引入不同的取代基,然后将功能化的阴阳离子结合形成新的胍基含能离子化合物。如在阴离子中引入氨基提高化合物的稳定性,引入硝氨基提高化合物的能量,引入氧、甲基等改善化合物的氧平衡。但是对胍基阳进行功能化的研究却很少,在该方向上还有待于进一步研究。
| [1] |
HuynhM H V, HiskeyM, Pollard C J, et al. 4, 4′, 6, 6′-Tetra-substituted hydrazo-and azo-1, 3, 5-triazines[J].
Journal of Energetic Materials, 2004, 22(4): 217-29. DOI:10.1080/07370650490893054 |
| [2] |
Singh R P, Verma R D, Shreeve J M, et al. Energetic nitrogen-rich salts and ionic liquids[J].
Angew Chem Int Ed, 2006, 37(34): 3585-3601. |
| [3] |
Hiskey M, Chavez D. Insensitive high-nitrogen compounds: DE220012776133[R]. 2001.
|
| [4] |
Son S F, Berghout H L, Bolme C A, et al. Burn rate measurements of HMX, TATB, DHT, DAAF and BTATz[C]//Proceedings of the Combustion Institute, Edinburgh, 2000, 28: 919-924.
|
| [5] |
Khandhadia P S, Burns S P, Williams G K. High gas yield nonazidegas generants: US6201505[P], 2001.
|
| [6] |
石家华, 孙逊, 杨春和, 等. 离子液体研究进展[J].
化学通报, 2002, 65(4): 243-250. SHI Jia-hua, SUN Xun, YANG Chun-he, et al. Progress in the studies on ionic liquids[J]. Chemistry, 2002, 65(4): 243-250. |
| [7] |
余天祥, 杨发福, 杨海鸥. 三氨基胍叠氮酸盐的非水相研究[J].
含能材料, 2000, 8(2): 52-55. YU Tian-xiang, YANG Fa-fu, YANG Hai-ou. Synthesis of triaminoguanidinum azide in non-aquious medium[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2000, 8(2): 52-55. |
| [8] |
GAO Hai-xiang, HUANG Yan-gen, YE Cheng-feng. The synthesis of di(aminoguanidine) 5-nitroiminote trazolate: some diprotic or monoprotic acids as precursors of energetic salts[J].
Chem Eur J, 2008, 14(18): 5596-5603. DOI:10.1002/(ISSN)1521-3765 |
| [9] |
Margaret J C, Konstantin K, Thomas M K. Synthesis and characterization of 4, 5-dicyano-2H-1, 2, 3-triazole and its sodium, ammonium, and guanidinium salts[J].
Inorg Chem, 2009, 48(4): 1731-1743. DOI:10.1021/ic801793p |
| [10] |
HE Ling, TAO Guo-Ling, Damon A Parrish, et al. Nitrocyanamide-based ionic liquids and their potential applications as hypergolic fuels[J].
Chemistry, Eur J, 2010, 16(19): 5736-5743. DOI:10.1002/chem.200902651 |
| [11] |
Carvalho D A. Triaminoguanidinum dicyanamide: USP3405175[P], 1968.
|
| [12] |
徐抗震, 赵凤起, 杨冉, 等. GNTO的热分解动力学和比热容及绝热至爆时间研究[J].
固体火箭技术, 2009, 32(1): 74-78. XU Kang-zhen, ZHAO Feng-qi, YANG Ran, et al. Non-isothermal decompositi on kinetics, specific heat capacity and adiabatic time-to-explosion of GNTO[J]. Journal of Solid Rocket Technology, 2009, 32(1): 74-78. |
| [13] |
Michael G, Thomas M. Potassium-, ammonium-, hydrazinium-, guanidinium-, aminoguanidinium-, diaminoguanidinium-, triaminoguanidinium-and melaminiumnitroformate-synthesis, characterization and energetic properties[J].
Zeitschrift fuer Anorganische und Allgemeine Chemie, 2007, 633(7): 1006-1017. DOI:10.1002/(ISSN)1521-3749 |
| [14] |
Frankel, Milt on B D, Li onel A. Triaminoguanidine cyanoformate: USP 3981899[P], 1976.
|
| [15] |
王伯周, 廉鹏, 刘愆, 等. 3, 6-双胍基-1, 2, 4, 5-四嗪及其盐的合成工艺改进[J].
含能材料, 2006, 14(5): 352-254. WANG Bo-zhou, LIAN Peng, LIU qian, et al. Synthesis improvement of 3, 6-diguanidino-1, 2, 4, 5-tetrazine and its salts[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2006, 14(5): 352-254. |
| [16] |
杨利, 张同来, 冯长根. AGNTO的制备和分子结构[J].
物理化学学报, 2001, 17(5): 438-442. YANG Li, ZHANG Tong-lai, FENG Chang-gen. Preparation and molecular structure of agnto[J]. Acta Phys-Chim Sin, 2001, 17(5): 438-442. |
| [17] |
徐松林, 阳世清. 偶氮四唑非金属盐类含能材料的合成与性能研究[J].
含能材料, 2006, 14(5): 377-380. XU Song-lin, YANG Shi-qing. Synthesis and properties of high-nitrogen energetic compounds based on azotetrazolate nonmetallic salts[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2006, 14(5): 377-380. |
| [18] |
Hiskey M A, Nir G, James S R, et al. High-nitrogen energetic materials dervied from azotetrazolate[J].
Journal of Energetic Materials, 1998, 16(2): 119-127. |
| [19] |
GAO Hai-xiang, ZENG Zhuo, Twamley B. Polycyano-anion-based energetic salts[J].
Chem Eur J, 2008, 14(4): 1282-1290. DOI:10.1002/(ISSN)1521-3765 |
| [20] |
Michael G, Konstantin K, Thomas M K. Nitrotetrazolate-2N-oxides and the strategy of N-oxide introduction[J].
Articles, 2010, 132(48): 17216-17226. |
| [21] |
Tobias F, Niko F, Thomas M K. N-rich salts of 2-methyl-5-nitraminotetrazole: Secondary explosives with low sensitivities[J].
Inorg Chem, 2011, 50(4): 1447-1458. DOI:10.1021/ic1019923 |
| [22] |
王宏社, 杜志明. 烟火气体发生剂研究进展[J].
含能材料, 2004, 12(6): 376-380. WANG Hong-she, DU Zhi-ming. Progress in gas generating pyrotechnie composition[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2004, 12(6): 376-380. |
| [23] |
黄海丰, 孟子晖, 周智明, 等. 含能盐与含能离子液体[J].
化学进展, 2009, 21(1): 152-163. HUANG Hai-feng, MENG Zi-hui, ZHOU Zhi-ming, et al. Energetic salts and energetic ionic liquids[J]. Progress in Chemistry, 2009, 21(1): 152-163. |
| [24] |
Takaes E A, Nor walk. Triaminoguanidinium 5-aminotetrazolate and its preparation: USP 3354172[P], 1967.
|
| [25] |
Torley R E, Wilton. Triaminoguanidinium salts of 5-vinyltetrazole polymers and a method for their preparation: USP 3397186[P], 1968.
|
| [26] |
余天祥, 杨海鸥, 李常青. 离子交换法合成三氨基胍叠氮酸盐[J].
含能材料, 1998, 6(2): 82-86. YU Tian-xiang, YANG Hai-ou, LI Chang-qing. Synthesis of triaminoguanidine azide by ion-exchange[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 1998, 6(2): 82-86. |
| [27] |
Goddard T P. Bis-triaminoguanidine dechydrodecaborate process: USP 4130585[P], 1978.
|
| [28] |
徐松林, 阳世清. 偶氮四唑非金属盐类含能材料的合成与性能研究[J].
含能材料, 2006, 14(5): 377-380. XU Song-lin, YANG Shi-qing. Synthesis and properties of high-nitrogen energetic compounds based on azotetrazolate nonmetallic salts[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2006, 14(5): 377-380. |
| [29] |
Hiskey M A, Nir G, James S R, et al. High-nitrogen energetic materials dervied from azotetrazolate[J].
Journal of Energetic Materials, 1998, 16(2): 119-127. |
| [30] |
Katritzky A R, Singh S, Kirichenko K, et al. In search of ionic liquids incorporating azolate anions[J].
Chem Eur, 2006, 12: 4630-4641. DOI:10.1002/(ISSN)1521-3765 |
Recent progress in synthesis and applications of energetic guanidine ionic compounds was introduced and reviewed with 30 references.




