2. 中国工程物理研究院化工材料研究所, 四川 绵阳 621900
2. Institute of Chemical Materials, China Academy of Engineering Physics, Mianyang 621900, China
精确打击和高破坏力是现代武器所追求的目标,随着现代高性能武器弹药的发展,对含能材料的综合性能(高能量密度、能量释放的高度可控性、低易损性和环境适应性等)要求越来越高[1]。
纳米铝热剂是当今含能材料领域的一个研究热点。传统铝热反应中各组分都是在微米状态下发生反应,由于受控于组分间最大传质速率的影响,能量释放速率较慢。与传统铝热剂相比,纳米铝热剂中氧化剂或燃料至少有一组尺寸为纳米级[2],比表面积的增大,使得反应组分间具有更大的反应接触面积,从而获得更大的传质速率,使反应快速进行,提高了传热率,并减少了热损失[3]。同时,由于纳米铝热剂对点火温度比较稳定,只有达到某一点火温度才会发生自持高温反应,具有不同于传统铝热剂的燃烧特性,因此也被称为“亚稳态分子间复合物”(metastable intermolecular composites)或超级铝热剂[4-5]。
美国利弗莫尔实验室(Lawrence Livermore National Laboratory)采用溶胶-凝胶法首次成功制备了Al/Fe2O3纳米铝热剂,并将该材料试用于点火器和传爆药[6]。洛斯阿拉莫斯(LosAlamos National Laboratory)国家实验室[7]也展开了大量研究,制备了多种纳米铝热剂,并进行了性能表征及点火性能测试,表明该体系具有高的能量密度和高于1 km·s-1的能量释放速率。目前,国际上研究较多的纳米铝热剂有Al/MoO3,Al/CuO,Al/Fe2O3[8]等。与国外相比,国内对纳米铝热剂的研究尚处于起步阶段,薛艳等[9]对纳米铝热剂Al/MoO3进行了初步的性能研究。王毅等[10]用溶胶-凝胶法制备的Al/Fe2O3具有优越的点火和能量特性。张松林等[11]对微米Al/Fe2O3点火温度与铝热剂球的体积关系进行了研究,认为二者没有明显关系。安亭等[12]通过溶胶-凝胶法制备了Al/CuO超级铝热剂,并深入研究了其前驱体热分解机理及非等温分解反应动力学。但上述制备过程中易产生静电,制备安全性能较差,一些方法易带入杂质,反应组分间结合程度低。
本研究以纳米铝粉为还原剂,与溶胶-凝胶法制备的CuO气凝胶在超声振荡条件下进行充分混合,制备了纳米铝热剂Al/CuO,并对其热反应性能以及点火性能进行了分析。研究成果可为研制新型的高能量密度、无铅污染的新型火工药剂提供技术支撑。
2 实验部分 2.1 材料与仪器Cu(NO3)2·3H2O,分析纯,成都市科龙化工试剂厂;无水乙醇,分析纯,成都市联合化工试剂研究所;聚丙烯酸,分析纯,天津市科密欧化学试剂有限公司;环氧丙烷,分析纯,成都市科龙化工试剂厂;纳米铝粉,纯度99.8%,徐州市宏武纳米材料有限公司。
FS-1200超声波处理器,上海生析超声仪器有限公司;CO2超临界干燥器,非标;日立TM-1000扫描电子显微镜,日立高新技术公司;X'Pert PRO型多功能X射线衍射仪,荷兰帕纳科公司;SDTQ600型同步热分析仪,美国TA仪器公司;比表面及孔径分析仪,JW-BK 112型,北京精微高博科学技术有限公司;GM-1导爆管起爆器,湖南湘西奇博矿山仪器厂。
2.2 实验过程 2.2.1 CuO气凝胶的制备在室温条件下,将9.69 g(7.8 mmoL)的Cu(NO3)2·3H2O和126 mL无水乙醇配成浅绿色的Cu(NO3)2醇溶液,再加入15 mL聚丙烯酸,充分搅拌均匀。将11 mL 1,2-环氧丙烷缓慢滴入上述溶液,搅拌均匀后静置数分钟,产生蓝绿色凝胶,即制得铜基醇凝胶。
将上述制得的铜基醇凝胶置于恒温箱中,45 ℃下老化数小时后,将样品用无水乙醇在45 ℃环境中浸泡5天,24 h更换一次无水乙醇。最后将浸泡后的样品进行CO2超临界流体干燥。在超临界干燥容器内在-4 ℃后进行液态CO2替换2天,然后升温至36 ℃使CO2压力达到7.5 MPa以上的超临界状态2天,然后开阀放气减压至常压。干燥完全后得到浅蓝绿色块状铜基气凝胶样品。
将上述铜基气凝胶样品置于马弗炉中缓慢加热至350 ℃,保持3 h,自然降温后获得黑色块状氧化铜气凝胶样品。
2.2.2 纳米铝热剂Al/CuO的制备将CuO气凝胶用玛瑙研钵研磨20 min后,按铝热反应化学计量比与粒径为40 nm的Al粉(过量30%)在环己烷中于超声振荡条件下混合,然后45 ℃下真空干燥,得到纳米铝热剂Al/CuO。
2.2.3 测试及表征将制备的样品CuO气凝胶和纳米铝热剂Al/CuO通过SEM,EDS,BET,XRD进行表征,比表面(BET)采用氮气吸附法进行测试。为验证Al/CuO的反应传播情况,进行了点火测试:称取205 mg纳米铝热剂Al/CuO的样品,放入截面边长为3 mm,长度10 cm的有机玻璃槽中,然后通过GM-1导爆管起爆器在敞开环境下进行点火测试。纳米铝热剂Al/CuO的热反应特性通过DTA/DSC测试进行表征。测试在纯度大于99.999%的氩气气氛下进行,气流量为100 mL·min-1,以20 ℃·min-1的速率从室温升至1000 ℃。
3 结果和讨论 3.1 CuO气凝胶的SEM表征图 1a和图 1b分别为CuO气凝胶热处理前和热处理后的SEM图片。由图 1a可观察到,经CO2超临界流体干燥后的初始样品为一种典型的气凝胶形貌,由平均直径约为30~50 nm左右的纳米级球形颗粒均匀地垒成三维网络结构,孔分布均匀、完整。由图 1b可知,热处理后的样品形貌为典型的多孔结构,CuO由粒径为几十纳米的颗粒组成蓬松的网状结构,其孔径约为30~60 nm。

|
图 1 CuO气凝胶的SEM图片 Fig.1 SEM photos of CuO aerogel |
纳米铝热剂Al/CuO反应式为:
| $ {\rm{Al}}\left( {\rm{g}} \right) + {\rm{CuO}}\left( {\rm{g}} \right) \to {\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}\left( {\rm{g}} \right) + {\rm{Cu}}\left( {\rm{g}} \right) $ |
图 2a为反应前Al/CuO的SEM图片,纳米Al和纳米CuO混合较为均匀,纳米CuO分散在Al颗粒表面,局部地方出现尺寸在150~200 nm左右的团聚体,可能为纳米Al的团聚,没有看到光滑表面的Al颗粒,说明表面覆盖纳米CuO颗粒。图 2b为Al/CuO反应后的SEM图片,可以看到形貌不同于反应前,说明组分发生了反应,反应产物由纳米颗粒组成,且均匀分散,为了验证混合均匀性,进一步进行了EDS能谱测试。

|
图 2 纳米铝热剂Al/CuO的SEM照片 Fig.2 SEM photos of Al/CuO nanothermite |
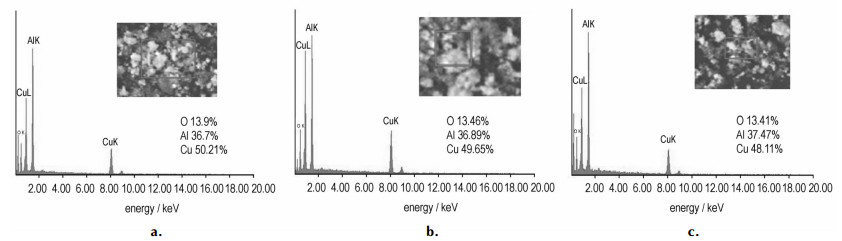
图 3为不同部位Al/CuO的EDS图谱,由图 3可见, 不同部位Al、O、Cu三种元素同时出现,说明复合的均匀性较好;能谱分析结果表明, Cu和O元素质量比接近于CuO化学式中质量比,多余的O元素可能是纳米铝粉在操作过程或受环境因素影响有部分被氧化所致。
|
图 3 纳米铝热剂Al/CuO不同处EDS图谱 Fig.3 EDS photos of the different parts of Al/CuO nanothermite |
经BET测试,CuO气凝胶的比表面约为170~200 m2·g-1,认为CuO气凝胶具有多孔结构,使其具有较大比表面积。Al/CuO的比表面积约为40 m2·g-1。复合后比表面积减小,可能是由于真空干燥后,纳米Al和CuO粉体出现了团聚,且二者紧密接触使表面积减小; 同时测试过程纳米Al粉暴露在空气中与氧气反应使质量增加以致比表面积减小。同时由于纳米Al粉和CuO的比表面积不同以及复合后所占比例不同,也使得最终复合产物比表面积减小。
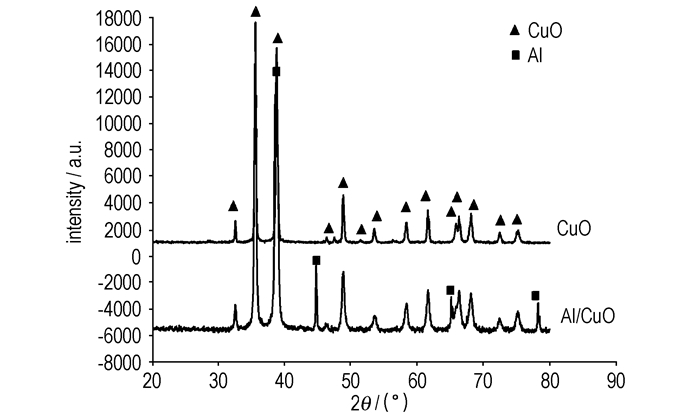
3.4 纳米铝热剂Al/CuO的XRD表征图 4是经过热处理后的CuO气凝胶和纳米铝热剂Al/CuO的XRD衍射图。由图 4可见,CuO衍射峰非常尖锐,表明所得CuO气凝胶具有良好的结晶性。350 ℃下热处理以后,吸附水、结晶水、氯元素以及有机物成分都被完全灼烧掉,只剩下铜和氧元素。在空气中热处理得到纯CuO的结晶,并由这些晶态CuO构成样品的骨架。在纳米铝热剂Al/CuO的XRD衍射图中可以看到, 除了CuO的衍射峰外,还增加了4个衍射峰,由软件分析其为Al的特征衍射峰。
|
图 4 CuO气凝胶和纳米铝热剂Al/CuO的XRD图谱 Fig.4 XRD spectra of CuO aerogel and Al/CuO nanthermite |
点火测试结果表明通过溶胶-凝胶法制备的纳米铝热剂Al/CuO容易用电火花或加热源点燃。采用GM-1导爆管起爆器对纳米铝热剂Al/CuO进行点火测试,点火现象如图 5所示。由图 5可见,Al/CuO剧烈反应释放能量并伴随明亮火焰,说明点火后反应快速传播,能够快速释放能量。这可能是由于CuO气凝胶比表面积增大,增加了Al和CuO的接触面,使得反应快速进行,并快速释放能量。为了进一步获得反应的定量信息,进行了热分析表征。

|
图 5 纳米铝热剂Al/CuO的点火 Fig.5 Ignition of Al/CuO nanothermite |
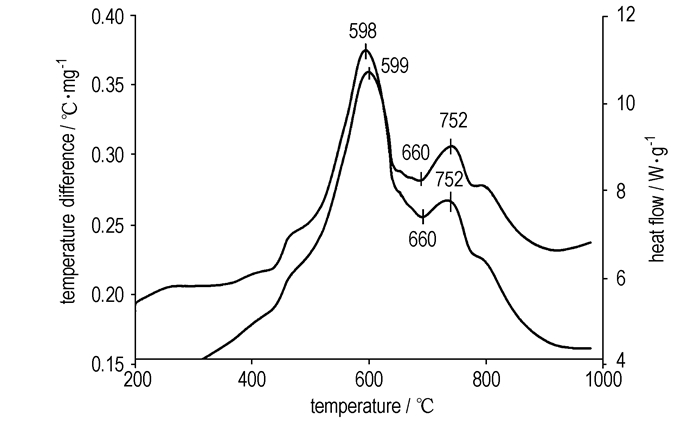
热分析测试是在惰性气体氩气气氛下进行的。在氩气气氛下,单独纳米Al粉除了达到熔点熔化时会有一个吸热峰,不会和氩气反应,也不会有放热现象。单独CuO气凝胶在实验温度范围内的氩气气氛下不会有放热反应。所以在氩气气氛下得到的热分析图谱,没有其它放热来源,可以确定是纳米Al和CuO反应的放热峰。图 6为Al/CuO放热反应的DTA/DSC曲线。由图 6可见,DTA和DSC曲线均出现两个放热峰,第一个放热峰在598 ℃左右,该反应起始温度在550 ℃左右,这说明该材料的反应温度低于Al的熔点(660 ℃),表明第一个放热峰是由纳米Al和纳米CuO的铝热反应所引起,属于固-固相扩散传播反应[10]。第二个放热峰在752 ℃左右,该峰是由熔化后的Al与CuO发生反应所引起,属于液-固相反应[10]。由图可知,660 ℃出现的小吸热峰是Al粉熔化引起的,此时熔化的Al继续与未反应的CuO反应。固-固相反应放热峰面积明显大于液-固相反应,说明热反应主要以固-固相反应为主。
|
图 6 纳米铝热剂Al/CuO的DTA/DSC曲线 Fig.6 DTA/DSC curves of Al/CuO nanothermite |
将溶胶-凝胶法与超临界干燥技术相结合,制备了比表面约为170~200 m2·g-1的多孔网状结构CuO气凝胶。通过超声波振荡搅拌将40 nm的Al粉和制备的CuO气凝胶混合,得到纳米铝热剂Al/CuO。通过GM-1导爆管起爆器点燃可以看到伴随火花的剧烈反应,热分析可知分别在598 ℃和752 ℃左右出现两个放热峰,分别对应Al和CuO的固-固相和液-固相反应,反应温度低于Al的熔化温度(660 ℃),其反应机制较传统铝热剂更加优越,这一优异性能说明Al/CuO铝热剂在枪炮发射药和火箭推进剂等方面具有潜在的应用前景。
| [1] |
黄辉, 王泽山, 黄亨建, 等. 新型含能材料的研究进展[J].
火炸药学报, 2005, 28(4): 9-13. HUANG Hui, WANG Ze-shan, HUANG Heng-Jian, et al. Researches and progresses of novel energetic materials[J]. Chinese Journal of Explosives & Propellants, 2005, 28(4): 9-13. |
| [2] |
Cheng J L, Hng H H, Ng H Y, et al. Synthesis and characterization of self-assembled nanoenergetic Al-Fe2O3 thermite system[J].
Journal of physics and Chemistry of Solids, 2010, 71(2): 90-94. DOI:10.1016/j.jpcs.2009.08.017 |
| [3] |
Son S F, Asay B W, Foley T J, et al. Combustion of nanoscale Al/MoO3 thermite in microchannels[J].
Journal of Propulsion and Power, 2007, 23(4): 715-721. DOI:10.2514/1.26090 |
| [4] |
PIERCEY Davin G, ÖTKE Thomas M KLAP. Nanoscale aluminum-metal oxide(thermite) reactions for application in energetic materials[J].
Central European Journal of Energetic Materials, 2010, 7(2): 115-129. |
| [5] |
Rossi C, Zhang K, Estève D, et al. Nanoenergetic materials for MEMS: A review[J].
Journal of Microelectromechanical Sysrems, 2007, 16(4): 919-931. DOI:10.1109/JMEMS.2007.893519 |
| [6] |
Tillotson T M, Gash A E, Simpson R L, et al. Nanostructured energetic materials using sol-gel methodologies[J].
Journal of Nano-Crystalline Solids, 2001, 285(1-3): 338-345. DOI:10.1016/S0022-3093(01)00477-X |
| [7] |
Sanders V E, Asay B W, Foley T J, et al. Combustion and reaction propagation of metastable intermolecular composites(MIC)[C]//Thirty-There International Pyrotechnics Seminar, FortColins, Colorado, USA, 2006, 7: 113-115.
|
| [8] |
Stenen F S, Blaine W. Burn rate measurements of nanocomposite thermites[R]. 41rd AIAA, Aerospace Sciences Meeting and Exhibit, AIAA-2003-241, 2003, 1.
|
| [9] |
薛艳, 张蕊, 杨伯伦, 等. 亚稳态分子间复合物Al/MoO3的制备与性能研究[J].
火工品, 2005(4): 33-36. XUE Yan, ZHANG Rui, YANG Bo-lun, et al. Preparation and characterization of metastable intermolecular composite Al/MoO3[J]. Initiators & Pyrotechnics, 2005(4): 33-36. |
| [10] |
王毅, 李凤生, 姜炜, 等. A1/Fe2O3纳米复合铝热剂的制备及其反应特性研究[J].
火工品, 2008(4): 11-14. WANG Yi, LI Feng-sheng, JIANG Wei, et al. Synthesis of Al/Fe2O3 nanocomposite and research on its thermite reaction[J]. Initiators & Pyrotechnics, 2008(4): 11-14. |
| [11] |
张松林, 武斌, 秦志桂, 等. 2Al/Fe2O3铝热剂的点火温度[J].
含能材料, 2010, 18(2): 162-166. ZHANG Song-lin, WU Bin, QIN Zhi-gui, et al. Ignition temperature of 2Al/Fe2O3 thermite[J]. Chniese Journal of Energetic Materials(Hanneng Cailiao), 2010, 18(2): 162-166. |
| [12] |
安亭, 赵风起, 仪建华, 等. 超级铝热剂Al/CuO前驱体的制备、表征、热分解机理及菲等温分解反应动力学[J].
物理化学学报, 2011, 27(2): 281-288. AN Ting, ZHAO Feng-qi, YI Jian-hua, et al. Preraration, characterization, decomposition mechanism and non-isothermal decomposition reaction kinetics of the super thermite Al/CuO precuesor[J]. Chinese Journal of Chemical Physics, 2011, 27(2): 281-288. |
The thermal behavior of the reaction of Al/CuO nanothermite was studied by means of DTA /DSC.




