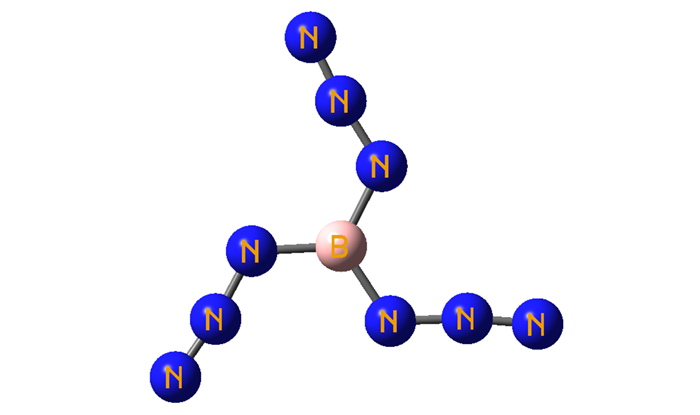
发射药和推进剂中引入叠氮基, 既可增加能量, 又可降低火焰温度, 因此叠氮基化合物, 如叠氮硝胺、叠氮烷烃、叠氮基胺和叠氮基醚等, 在含能增塑剂、含能粘合剂、氧化剂和其它添加剂的研制方面有着独特的作用[1-2]。近年来, 多叠氮化合物(Polyazides)[3]的合成使叠氮基化合物的研究焕发出新的活力, 多达18种元素形成的多叠氮化合物已成功合成[3-11]。其中三叠氮化硼(B(N3)3)含氮量高达91.97%, 有很强的能量储备能力。其最稳定构型为平面三角形, 如图 1所示, 具有C3h对称性, 分子中B原子表现出强烈的缺电子性, 极易和胺、醚等形成配合物[12], 有望应用于一系列含能添加剂中。
|
图 1 B(N3)3的稳定构型 Fig.1 Optimized geometrical structure of boron triazide B(N3)3 |
然而, B(N3)3的合成一般通过气相法进行, 如Julanna V.Gilbert等将氩气稀释后的三氯化硼(BCl3:Ar =1:100)和叠氮酸(HN3: Ar=1:100)按1:3混合, 经常温反应后在氩气氛中生成B(N3)3[4]; Foo-tim Chau等将稀薄的三溴化硼气体通过新制备的叠氮化银粉末, 经异相反应生成气相B(N3)3, 并用光电子能谱对其进行了表征[13]。然而, 气相合成法一般需要特殊的实验设备, 操作工序多, 少量产物存在于其它气体介质中, 给应用研究带来不便。
为此, 本研究选择三溴化硼和三甲基叠氮硅烷(TMSA)为起始原料, 在液相中合成了B(N3)3, 克服现有气相合成法的不足, 提供了一种B(N3)3的简便合成方法。
2 实验部分 2.1 试剂与仪器试剂:三甲基叠氮硅烷, 三溴化硼, 三氟化硼乙醚络合物, 乙腈均为市售分析纯级。
仪器:上海精密科学仪器有限公司JA 5003B型分析天平; Nicocet 5700 FT-IR型傅里叶变换红外光谱仪, 红外光谱由溴化钾夹片法测定; Bruker 400 MHz核磁共振仪。
2.2 实验过程氩气保护下, 将2.0 mL三甲基叠氮硅烷加入含5.0 mL无水乙腈的反应瓶中, 冰浴冷却, 在搅拌下快速注入1.26 g三溴化硼, 然后缓慢升至室温继续反应。用红外光谱监测反应液, 直到三甲基叠氮硅烷反应完全。常压蒸馏反应液, 收集42~45 ℃馏分, 得到淡黄色液体。
3 结果与讨论 3.1 原料选择与在稀薄的气相介质中合成B(N3)3相比, 液相合成更常规更实用。经实验筛选, BBr3具有非常高的反应活性, 比另一种商品化试剂三氟化硼乙醚更适合作为B(N3)3的合成原料。无机叠氮试剂在有机溶剂中溶解性很差, 而叠氮酸剧毒且易爆, 因此, 兼具溶解性和反应活性的三甲基叠氮硅烷(TMSA)是该实验的理想原料。二者在室温下即可反应, 合成路线如下:
BBr3+3(CH3)3SiN3→ B(N3)3+3(CH3)3SiBr
B(N3)3在溶液中比较稳定。利用B(N3)3和溶剂沸点的差异, 可通过蒸馏得到B(N3)3纯品, 为淡黄色液体。要注意的是, B(N3)3极易爆炸, 尤其是纯品, 转移等操作宜在溶液中进行。实验过程中要严格控制剂量, 并佩戴好防护措施。
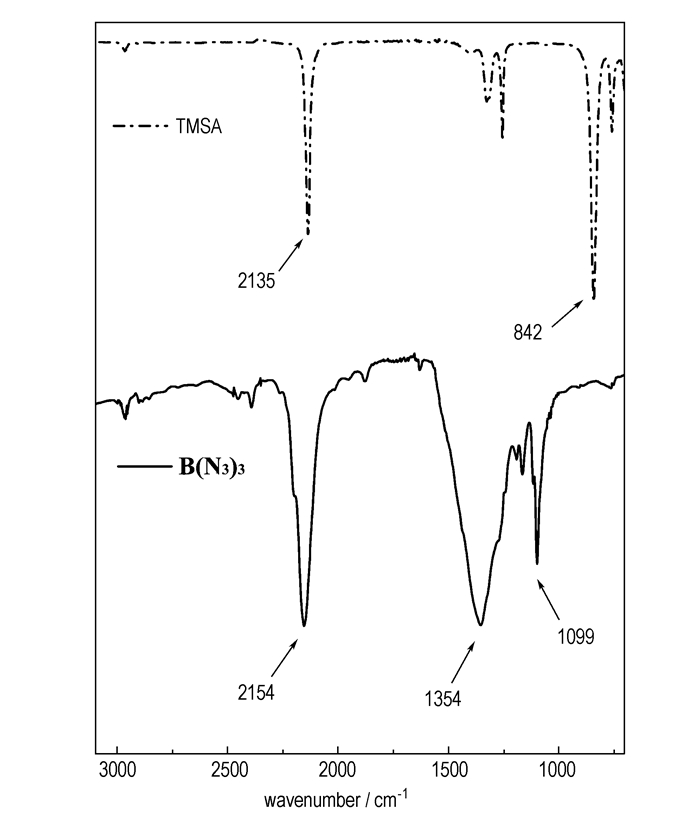
3.2 B(N3)3的表征由于B(N3)3纯品极易爆炸, 本课题组曾尝试用液质联用分析B(N3)3的乙腈溶液, 但即使选用软电离方式, 除了获得m/z=28(N2)信号外, 未发现对鉴定结构有用的其它信息, 因此本研究中未提供质谱数据。但是B(N3)3在红外光谱上有极其明显的特征吸收峰, 尤其是叠氮基, 在反应过程中, 可以明显监测到原料消失, 产物生成的过程。如图 2所示, 原料三甲基叠氮硅烷(TMSA)的主要红外峰在2135, 842 cm-1, 随着反应的进行, 这组峰强度逐渐减小, 最终被产物的特征峰替代:2154 cm-1处的强峰为叠氮基不对称伸缩振动的特征峰; 1354, 1099 cm-1处的一组强峰是叠氮基对称伸缩振动的特征峰。该组数据和Al-Jihad等[4]报道的气相B(N3)3的红外峰(2163, 1360, 1100 cm-1)吻合较好, 细微差别是由产物相态不同引起的。
|
图 2 B(N3)3和TMSA的红外光谱图 Fig.2 IR spectrum of B(N3)3 and trimethylsilylazide(TMSA) |
同时, 本研究尝试对B(N3)3进行室温14N NMR表征。样品在氘代乙腈中的核磁共振谱有三个清晰可辨的N信号, 化学位移分别位于-257, -139, -170, 依次归属为叠氮基上的Nα, Nβ, Nγ(M-Nα-Nβ-Nγ)。
4 结论以三溴化硼和三甲基叠氮硅烷为起始原料, 在乙腈中经低温反应合成出B(N3)3, 并通过蒸馏分离出样品。该方法所需设备简单, 操作工序少, 实验条件温和, 实现了B(N3)3的简便合成。
| [1] |
施明达. 一种新型含能材料-叠氮有机化合物[J].
火炸药, 1992(4): 24-30. |
| [2] |
周明川. 国外叠氮有机化合物的研究[J].
固体火箭技术, 1990(1): 59-63. ZHOU Ming-chuan. Study on organic azide compounds in abroad[J]. Journal of Solid Rocket Technology, 1990(1): 59-63. |
| [3] |
丁可伟, 李陶琦, 葛忠学, 等. 多叠氮类化合物的合成研究进展[J].
含能材料, 2013, 21(1): 116-120. DING Ke-wei, LI Tao-qi, GE Zhong-xue, et al. Review on synthesis of polyazides[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2013, 21(1): 116-120. |
| [4] |
Al-Jihad I A, Liu B, Linnen C J, et al. Generation of NNBN via photolysis of B(N3)3 in low-temperature argon matrices:IR spectra and ab initio calculations[J].
J Phys Chem A, 1998, 102: 6220-6226. DOI:10.1021/jp9812684 |
| [5] |
Haiges R, Boatz J A, Williams J M, et al. Preparation and characterization of the binary group 13 azides M(N3)3 and M(N3)3·CH3CN(M=Ga, In, Tl), [Ga(N3)5]2-, and[M(N3)6]3-(M=In, Tl)[J].
Angew Chem Int Ed, 2011, 50: 8828-8833. DOI:10.1002/anie.v50.38 |
| [6] |
Banert K, Joo Y H, Rffer T, et al. The exciting chemistry of tetraazidomethane[J].
Angew Chem Int Ed, 2007, 46: 1168-1171. DOI:10.1002/(ISSN)1521-3773 |
| [7] |
Haiges R, Boatz J A, Vij A, et al. Polyazide chemistry:preparation and characterization of Te(N3)4 and[P(C6H5)4]2[Te(N3)6] and evidence for[N(CH3)4][Te(N3)5][J].
Angew Chem Int Ed, 2003, 42: 5847-5851. DOI:10.1002/(ISSN)1521-3773 |
| [8] |
Haiges R, Boatz J A, Christe K O. The Syntheses and structure of the vanadium(Ⅳ) and vanadium(Ⅴ) binary azides V(N3)4, [V(N3)6]2-, and[V(N3)6]-[J].
Angew Chem Int Ed, 2010, 49: 8008-8012. DOI:10.1002/anie.v49:43 |
| [9] |
Haiges R, Vij A, Boatz J A, et al. First structural characterization of binary As and Sb azides[J].
Chem Eur J, 2004, 10: 508-517. DOI:10.1002/(ISSN)1521-3765 |
| [10] |
Haiges R, Boatz J A, Schneider S, et al. The binary group 4 azides[Ti(N3)4], [P(C6H5)4][Ti(N3)5], and[P(C6H5)4]2[Ti(N3)6] and on linear Ti-N-NN coordination[J].
Angew Chem Int Ed, 2004, 43: 3148-3152. DOI:10.1002/(ISSN)1521-3773 |
| [11] |
Haiges R, Boatz J A, Bau R, et al. Polyazide chemistry:The first binary group 6 azides, Mo(N3)6, W(N3)6, [Mo(N3)7], and[W(N3)7], and the[NW(N3)4] and[NMo(N3)4] Ions[J].
Angew Chem Int Ed, 2005, 44: 1860-1865. DOI:10.1002/(ISSN)1521-3773 |
| [12] |
Fraenk W, Habereder T, Hammerl A. Highly energetic tetraazidoborate anion and boron triazide adducts[J].
Inorg Chem, 2001, 40: 1334-1340. DOI:10.1021/ic001119b |
| [13] |
Fengyi L, Xiaoqing Z, Jianping Z, et al. A simple method to generate B(N3)3[J].
Chem Phys Lett, 2006, 419: 213-216. DOI:10.1016/j.cplett.2005.11.082 |

Boron triazide(B(N3)3)was synthesized via low-temperature reaction in acetonitrile with trimethylsilylazide and boron tribromide as starting materials.




