1, 1′-二羟基-5, 5′-联四唑二羟胺盐(HATO)的晶体密度为1.877 g·cm-3, 生成焓为446.6 kJ·mol-1, 爆压大于HMX, 稍低于CL-20, 爆速大于CL-20, 理论比冲高于RDX、HMX和CL-20, 具有较高的能量水平[1]。HATO同时具有热稳定性好、机械感度低等优点, 是一种综合性能优良的高能不敏感含能材料, 目前受到含能材料领域的广泛关注[2]。通常, 1, 1′-二羟基-5, 5′-联四唑的碱金属盐是利用复分解反应制备HATO的原料, 同时1, 1′-二羟基-5, 5′-联四唑的碱金属盐也可用于气体发生剂, 其中1, 1′-二羟基-5, 5′-联四唑二钾盐也是一种潜在的消焰剂。作为一类新型含能材料, 不同1, 1′-二羟基-5, 5′-联四唑的碱金属盐与HATO溶解度及溶解热力学参数是应用研究的基础热力学数据。因此, 1, 1′-二羟基-5, 5′-联四唑的碱金属盐与HATO的溶解度及溶解热力学对其应用研究具有重要的意义。
本研究合成了1, 1′-二羟基-5, 5′-联四唑的四种盐, 并利用激光监测技术、采用动态法测定了不同温度下, HATO、1, 1′-二羟基-5, 5′-联四唑二锂盐(Li2DHBT)、1, 1′-二羟基-5, 5′-联四唑二钠盐(Na2DHBT)、1, 1′-二羟基-5, 5′-联四唑二钾盐(K2DHBT)在水中的溶解度(s), 利用理想溶液模型[3]、Apelblat方程[4-6]对实验数据进行了关联, 并对结果进行了分析。
2 实验部分 2.1 试剂与仪器试剂:实验所用1, 1′-二羟基-5, 5′-联四唑(H2DHBT)为实验室根据文献[1, 7]方法制得; LiOH、NaOH、KOH、盐酸羟胺、乙醇为分析纯; 实验用水为去离子二次蒸馏水。
仪器:德国Elementar公司Vario EL Ⅲ型元素分析仪; 美国Nicolet公司FTIR型红外光谱仪; 瑞士Bruker公司AV500型(500 MHz)超导核磁共振仪; 优莱博公司F12型恒温器; 西安赛朴林激光技术研究所TLX-B型激光仪、JD-1激光二极管组件参数测量仪。
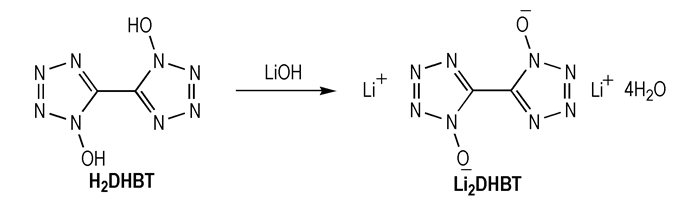
2.2 合成实验 2.2.1 Li2DHBT的合成合成路线见Scheme 1。
|
Scheme 1 |
向圆底烧瓶中加入206 mg H2DHBT和5 mL水, 室温条件下搅拌, 分批加入88 mg氢氧化锂, 搅拌反应2 h后, 经浓缩、过滤、乙醇洗涤、干燥得230 mg白色晶体, 产率90.6%。13C NMR(125 MHz, DMSO-d6, δ):134.69;IR(KBr, ν/cm-1):3538, 3311, 1670, 1434, 1368, 1243, 1181, 1064, 1009, 748, 705, 617, 509, 470;元素分析C2H8Li2N8O6(%):理论值:C 9.46, H 3.17, N 44.11;实测值:C 9.13, H 3.13, N 44.27。
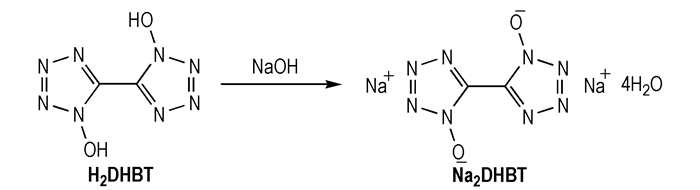
2.2.2 Na2DHBT的合成合成路线见Scheme 2。
|
Scheme 2 |
向圆底烧瓶中加入206 mg H2DHBT和5 mL水, 室温条件下搅拌, 分批加入84 mg氢氧化钠, 搅拌反应2 h后, 经浓缩、过滤、乙醇洗涤、干燥得263 mg白色晶体, 产率91.9%。13C NMR(125 MHz, DMSO-d6, δ):134.19;IR(KBr, ν/cm-1):3496, 3404, 3311, 1673, 1424, 1359, 1240, 1178, 1149, 1067, 1007, 755, 718, 687, 658, 623, 544, 502。元素分析C2H8Na2N8O6(%):理论值:C 8.40, H 2.82, N 39.16;实测值:C 8.38, H 2.79, N 39.24。
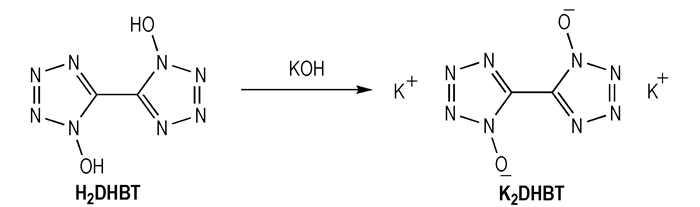
2.2.3 K2DHBT的合成合成路线见Scheme 3。
|
Scheme 3 |
向圆底烧瓶中加入206 mg H2DHBT和5 mL水, 室温条件下搅拌, 分批加入132 mg氢氧化钾, 搅拌反应2 h后, 经浓缩、过滤、乙醇洗涤、干燥得222 mg白色晶体, 产率90.2%。13C NMR(125 MHz, DMSO-d6, δ):135.36;IR(KBr, ν/cm-1):1638, 1510, 1408, 1356, 1286, 1233, 1164, 1058, 998, 805, 732, 715, 502;元素分析C2K2N8O2(%):理论值:C 9.75, N 45.50;实测值:C 9.71, N 46.10。
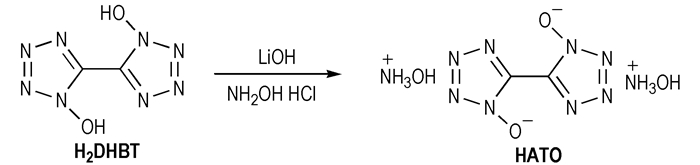
2.2.4 HATO的合成合成路线见Scheme 4。
|
Scheme 4 |
向圆底烧瓶中加入206 mg H2DHBT和5 mL水, 升至70 ℃, 分批加入88 mg氢氧化锂, 搅拌反应30 min, 滴加含139 mg盐酸羟胺的水溶液5 mL, 经浓缩、洗涤、过滤、干燥得223 mg白色晶体, 产率94.1%。1H NMR(DMSO-d6, 500 MHz):10.18(brs, 8H); 13C NMR(DMSO-d6, 125 MHz):134.98;IR(KBr, ν/cm-1):3221, 3084, 2913, 2682, 2504, 1578, 1526, 1427, 1413, 1351, 1236, 1172, 1045, 1011, 997, 814, 716, 674, 499。元素分析C2H8N10O4(%), 计算值:C 10.17, H 3.41, N 59.31;实测值:C 10.05, H 3.39, N 59.56。
2.3 溶解度测定采用动态法对HATO、Li2DHBT、Na2DHBT、K2DHBT的溶解度进行测定, 利用激光监测技术代替人眼观察固体的溶解情况, 提高了测量的精度。具体实验装置及过程参照文献[8-9]方法进行。
为保证实验数据的准确, 同样操作重复3次, 取平均值。溶质在某温度下纯溶剂中的摩尔溶解度(x)可表示为:
| $ x = \frac{{{m_{\rm{A}}}/{M_{\rm{A}}}}}{{{m_{\rm{A}}}/{M_{\rm{A}}} + {m_{\rm{B}}}/{M_{\rm{B}}}}} $ | (1) |
式中, mA、mB分别表示溶质和溶剂的质量, g; MA、MB分别表示溶质和溶剂的分子量。
2.4 关联模型为了更好地描述HATO、Li2DHBT、Na2DHBT、K2DHBT溶解度的变化规律, 选用理想溶液模型[3]和Apelblat方程[4-6]对实验数据进行了关联。
(1) 理想溶液模型
对于固液平衡体系, 依据热力学原理[10], 溶解度方程可表示为:
| $ {\rm{ln}}\left( {\frac{1}{{x\gamma }}} \right) = \frac{{\Delta {H_{{\rm{tp}}}}}}{R}\left( {\frac{1}{{{T_{{\rm{tp}}}}}} - \frac{1}{T}} \right) - \frac{{\Delta {C_{\rm{P}}}}}{R}\left( {{\rm{ln}}\frac{{{T_{{\rm{tp}}}}}}{T} - \frac{{{T_{{\rm{tp}}}}}}{T} + 1} \right) - \frac{{\Delta V}}{{RT}}(p - {p_{{\rm{tp}}}}) $ | (2) |
式中, γ为溶液中溶质的活度系数; R表示气体常数, 8.3145 J·mol-1·K-1; ΔHtp为三相点时的熔化焓, J·mol-1; Ttp为三相点温度, K; Cp为定压摩尔热熔, J·mol-1·K-1; ΔV为体积差, m-3; p为体系的压力, Pa; ptp为三相点压力, Pa。
忽略影响较小的压力相和热容差相, 并用熔点代替三相点温度, 可得简化方程为:
| $ {\rm{ln}}\left( {\frac{1}{{x\gamma }}} \right) = \frac{{\Delta {H_{\rm{m}}}}}{R}\left( {\frac{1}{{{T_{\rm{m}}}}} - \frac{1}{T}} \right) $ | (3) |
式中, ΔHm为熔化焓, J·mol-1; Tm为熔点, K。
在远离临界区域的有限温度范围内真实溶液中组分的活度因子γ对温度的依赖程度较小, 即γ对温度不敏感, 近似为1。因此方程可以写为以下形式:
| $ {\rm{ln}}x = a + b/T $ | (4) |
(2) Apelblat方程
| $ {\rm{ln}}x = A + \frac{B}{T} + C{\rm{ln}}T $ | (5) |
式中, A, B和C为3个无因次参数。
其中, 相对误差σ为:
| $ \sigma = \frac{{{x_{{\rm{exp}}}} - {x_{cal}}}}{{{x_{{\rm{exp}}}}}} \times 100\% $ | (6) |
平均相对误差ε为:
| $ \varepsilon = \frac{1}{n}\sum\limits_{i = 1}^n {\left| {{\sigma _i}} \right|} $ | (7) |
式中, n为实验点数。
(3) 溶解热力学数据的计算方法[11]
根据Van′t Hoff方程[12]可知溶解度的对数值与温度呈线型关系:
| $ {\rm{ln}}x = - \frac{{\Delta {H_{\rm{m}}}}}{{RT}} + \frac{{\Delta {S_{\rm{m}}}}}{R} $ | (8) |
式中, ΔHm为熔融焓, kJ·mol-1; ΔSm为熔融熵, kJ·mol-1·K-1; T表示绝对温度, K; R表示气体常数。
在实际应用中, 常用混合热力学数据代替熔融热力学数据。用ΔHd代替ΔHm, 用ΔSd代替ΔSm, 所以方程可写为
| $ {\rm{ln}}x = - \frac{{\Delta {H_{\rm{d}}}}}{{RT}} + \frac{{\Delta {S_{\rm{d}}}}}{R} $ | (9) |
此方程形式与理想溶液模型相同, 因此可以利用理想溶液模型的拟合结果求得ΔHd和ΔSd。
3 结果与讨论 3.1 溶解度实验数据的测定结果HATO、Li2DHBT、Na2DHBT、K2DHBT在水中的溶解度如表 1所示。
| 表 1 四种1, 1′-二羟基-5, 5′-联四唑盐的溶解度 Tab.1 Solubilities of four kinds salts of 5, 5′-bistetrazole-1, 1′-diolate |
由表 1数据可知, HATO、Li2DHBT、Na2DHBT、K2DHBT在水中的溶解度均随着温度的升高而增加。在25~60 ℃范围内, HATO、Li2DHBT、Na2DHBT、K2DHBT的溶解度对温度的依赖程度不相同, Li2DHBT的溶解度对温度依赖性较高, 即随温度变化, 其溶解度变化最大, HATO的溶解度随温度的变化最小。
3.2 实验数据拟合结果将HATO、Li2DHBT、Na2DHBT、K2DHBT理想溶液模型和Apelblat方程拟合参数及平均相对误差(ε)列于表 2和表 3中。
| 表 2 理想溶液模型拟合结果 Tab.2 Parameters of the ideal solution model for four kinds of salts of 5, 5′-bistetrazole-1, 1′-diolate |
| 表 3 Apelblat方程拟合结果 Tab.3 Parameters of the Apelblat equation for four kinds of salts of 5, 5′-bistetrazole-1, 1′-diolate |
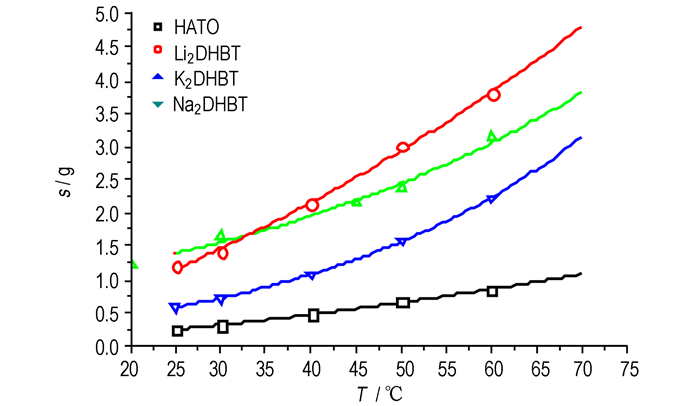
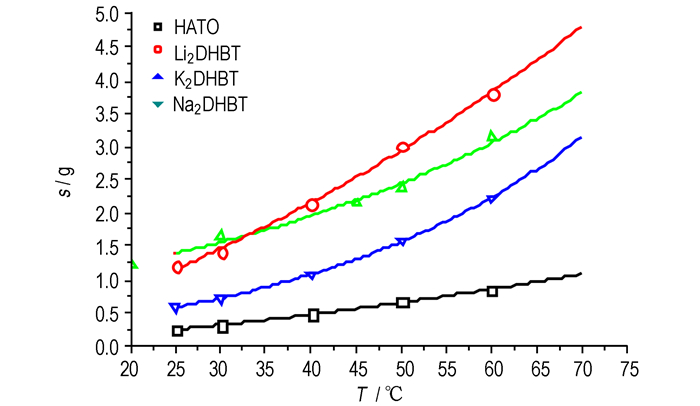
从表 2和表 3的数据可知, 选用理想溶液模型和Apelblat方程均能得到较好的拟合数据, 相关系数均在0.97以上, 平均相对误差在3.5%以内。但Apelblat方程的拟合精度要优于理想溶液模型, 可用作处理及回归。根据Apelblat方程的拟合结果得到的溶解度曲线如图 1所示。图 1中曲线为Apelblat方程的拟合曲线, 点为实验数据。
|
图 1 四种1, 1′-二羟基-5, 5′-联四唑盐的溶解度曲线 Fig.1 Solubility curves of four kinds salts of 5, 5′-bistetrazole-1, 1′-diolate |
由图 1可以看出, Apelblat方程的拟合结果与实验数据具有较好的一致性。从溶解度曲线可以看出, 当温度为33.2 ℃时, K2DHBT和Li2DHBT的溶解度相等。当温度小于33.2 ℃时, 溶解度大小顺序为:K2DHBT>Li2DHBT>Na2DHBT>HATO; 当温度大于33.2 ℃时, 溶解度大小顺序为:Li2DHBT>K2DHBT>Na2DHBT>HATO。
当温度为70 ℃时, 由溶解度曲线可计算得到这三种碱金属溶液的摩尔溶解度分别为:xLi2DHBT=4.7×10-3, xNa2DHBT =2.6×10-3, xK2DHBT =2.8×10-3, Li2DHBT的摩尔溶解度最大。因此, 当利用1, 1′-二羟基-5, 5′-联四唑的碱金属盐来制备HATO时, 1, 1′-二羟基-5, 5′-联四唑二锂盐是最佳反应原料。
3.3 溶解热力学计算结果溶解焓及溶解熵是化合物基本溶解热力学数据, 本文根据理想方程拟合结果对HATO、Li2DHBT、Na2DHBT、K2DHBT的溶解焓与溶解熵进行了计算, 计算结果如表 4所示。
| 表 4 溶解热力学计算结果 Tab.4 Thermodynamic parameters for dissolution of four kinds of salts of 5, 5′-bistetrazole-1, 1′-diolate |
从表 4中数据可以看出, HATO、Li2DHBT、Na2DHBT、K2DHBT在溶解过程中ΔHd均为正值, 表明这四类盐的溶解过程需要消耗能量, 为吸热过程, ΔSd为正值, 表明这四类盐的溶解过程为不可逆过程。
4 结论(1) 以H2DHBT为原料, 分别与氢氧化锂、氢氧化钠、氢氧化钾反应得到Li2DHBT、Na2DHBT、K2DHBT, 收率均大于90%。以Li2DHBT为原料, 通过与盐酸羟胺的复分解反应制备得到1, 1′-二羟基-5, 5′-联四唑二羟胺盐(HATO), 收率为94.1%。
(2) 采用动态法激光监测技术分别测定了HATO、Li2DHBT、Na2DHBT、K2DHBT的在不同温度下的溶解度。实验结果表明, 这四种盐的溶解度均随温度的升高而增加。
(3) 理想溶液模型和Apelblat方程均能较好的关联实验数据, 其拟合值与实验值的平均相对误差在3.5%以内, 但Apelblat方程的溶解度数据的关联结果优于理想溶液模型。
(4) 通过van′t Hoff方程求得实验的溶解焓和溶解熵均为正值, 表明HATO、Li2 DHBT、Na2 DHBT、K2DHBT在水中的溶解过程均为不可逆吸热过程。
| [1] |
毕福强, 肖川, 许诚, 等. 1, 1'-二羟基-5, 5'-联四唑羟胺盐的合成及性能[J].
含能材料, 2014, 22(2): 272-273. Bi Fu-qiang, XIAO Chuan, XU Cheng, et al. Synthesis and properties of dihydroxylammonium 5, 5'-bistetrazole-1, 1'-diolate[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2014, 22(2): 272-273. |
| [2] |
Niko Fischer, Dennis Fischer, Thomas M.Klapötke, et al. Pushing the limits of energetic materials-the synthesis and characterization of dihydroxylammonium 5, 5'-bistetrazole-1, 1'-diolate[J].
J Mater Chem, 2012, 22: 20418-20422. DOI:10.1039/c2jm33646d |
| [3] |
韩佳宾, 王静康. 咖啡因在水和乙醇中的溶解度及其关联[J].
化工学报, 2004, 55(1): 125-128. HAN Jia-bin, WANG Jing-kang. Measurement and correlation of the solubility of caffeine in water and ethanol[J]. Journal of chemical industry and engineering, 2004, 55(1): 125-128. |
| [4] |
Apelblat A, Manzurola E. Solubilities of o-acetylsalicylic, 4-aminosalicylic, 3, 5-dinitrosalicylic and, p-toluic acid, and magnesium-dl-aspartate in water from T=(278 to 348)K[J].
J Chem Therm, 1999, 31(1): 85-91. DOI:10.1006/jcht.1998.0424 |
| [5] |
Apelblat A, Manzurola E. Solubilities of L-aspartic, dl-aspartic, dl-hydroxybenzoic, o-anisic, p-anisicm, and itaconic acids in water from T=278K to T=345K[J].
J Chem Therm, 1997, 29(12): 1527-1533. DOI:10.1006/jcht.1997.0267 |
| [6] |
Manzurola E, Apelblat A. Solubilities of l-gluatamic acid, 3-nitrobenzoic acid, p-toluic acid, calcium-l-lactate, calcium gluconate, magnesium-dl-aspartate, and magnesium-l-lactate in water[J].
J Chem Therm, 2002, 34(7): 1127-1136. DOI:10.1006/jcht.2002.0975 |
| [7] |
毕福强, 樊学忠, 许诚, 等. 1, 1'-二羟基-5, 5'-联四唑的合成及理论研究[J].
火炸药学报, 2013, 36(4): 22-25. BI Fu-qiang, FAN Xue-zhong, XU Cheng, et al. Synthesis and theoretical study of 1, 1'-diolate-5, 5'-bistetrazole[J]. Chinese Journal of Explosives & Propellants, 2013, 36(4): 22-25. |
| [8] |
李群生, 冯召东, 赵宇, 等. 激光动态法测定DL-酒石酸有机溶剂中的溶解度[J].
北京化工大学学报(自然科学版), 2012, 39(5): 6-10. LI Qun-sheng, FENG Zhao-dong, ZHAO Yu, et al. Measurement and correlation of the solubility of DL-tartaric acid in selected solvents using a laser monitoring technique[J]. Journal of Beijing University of Chemical Technology(Natural Science), 2012, 39(5): 6-10. |
| [9] |
朱勇, 葛忠学, 王伯周, 等. RDX溶液固液平衡数据测定及模型研究[J].
含能材料, 2010, 18(4): 393-396. ZHU Yong, GE Zhong-xue, WANG Bo-zhou, et al. Measurement of solid-Liquid equilibrium and its model for RDX solution[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2010, 18(4): 393-396. |
| [10] |
Walas S M. 化工相平衡[M]. (韩世钧)译. 北京: 中国石化出版社, 1991.
Walas S M. Phase Equilibrium in Chemical Engineering[M]. Translated by HAN Shi-jun. Beijing: Chinese Petrochemical Press, 1991. |
| [11] |
李群生, 赵宇, 秦小勇, 等. 乌洛托品在有机溶剂中溶解度的测定与关联[J].
北京化工大学学报(自然科学版), 2012, 39(3): 24-28. LI Qun-sheng, ZHAO Yu, QIN Xiao-yong, et al. Measurement and correlation of the solubility of hexamethylenetetramine in organic solvents[J]. Journal of Beijing University of Chemical Technology(Natural Science), 2012, 39(3): 24-28. |
| [12] |
Bennema P, van Eupen J, Van der Wolf B M, et al. Solubility of molecular crystals:Polymorphism in the light of solubility theory[J].
International Journal of Pharmaceutics, 2008, 351(1/2): 74-91. |
Dihydroxylammonium 5, 5′-bistetrazole-1, 1′-diolate, dilithium 5, 5′-bistetrazole-1, 1′-diolate, disodium 5, 5′-bistetrazole-1, 1′-diolate and dipotassium 5, 5′-bistetrazole-1, 1′-diolate were synthesized.Their solubilities were measured and analyzed.




