二硝酰胺盐不含卤素, 可作为环境友好高能低特征征信号推进剂的氧化剂, 是目前推进剂研究的热点。N-脒基脲二硝酰胺盐(FOX-12)具有燃烧产物环境友好、产气量大、燃烧稳定、燃速对温度和压力的依赖性小等诸多优点, 已在安全气囊气体发生器领域得到应用, 也可作为低特征信号推进剂组分[1-2]。二硝酰胺钾(KDN)是在推进剂和烟火剂领域中有潜力的无机氧化剂, 可以作为硝酸铵(AN)的相稳定剂[3], 可替代硝酸钾作为含能烟火剂[4], 也可作为制备其他二硝酰胺金属盐或非金属盐的中间体[5-6]。二硝酰胺铵(ADN), 作为氧化剂取代推进剂配方中的AP, 预估航天运载火箭的运载能力将会提升约8%, 实现燃烧的低特征信号; 超纯的ADN制备技术推动了ADN基液体推进剂的研制, 瑞典已成功应用于近地轨道PRISMA卫星导航推进器[7-8]。
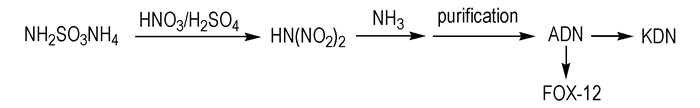
早期文献[9]报道的合成二硝酰胺盐的方法主要是以二硝酰胺铵(ADN)为前体, 通过离子交换反应得到KDN或FOX-12, 见Scheme 1。而ADN制备方法中最受关注是混酸硝化法, 即将氨基磺酸铵混酸硝化后将中间体二硝酰胺酸HN(NO2)2与硝硫混酸的混合物倒入冰水中后用氨水中和, 造成氨中和反应后的混合物(包括ADN、硝酸铵、硫酸铵)溶解在同一溶剂中而成为溶液, 使分离提纯ADN过程十分繁琐, 不利于工业放大, 因此一直以来ADN的合成规模及成本制约着其他二硝酰胺盐的制备及应用。
|
Scheme 1 Synthetic route of dinitramide salt[9] |
瑞典专利[10]报道了一种新型的合成二硝酰胺盐的方法, 即将氨基磺酸铵混酸硝化后倒入双氰胺水溶液或脒基脲悬浮液中, 过滤即得二硝酰胺盐。该方法制备的缺点是放热量非常大, 温度会升至70 ℃以上甚至达到水的沸点, 试验危险性增大; 部分脒基脲没有完全溶解使得水解后所得产品杂质含量较高。本研究针对该缺点改进了文献[10]的工艺路线, 将脒基脲溶解于惰性溶剂中, 将完成硝化反应后的硝化液倒入配制好的惰性溶液中以期平稳、高效的制备二硝酰胺盐产品。
2 实验部分 2.1 试剂脒基脲溶液:自制; 发烟硝酸、发烟硫酸:分析纯, 国药集团; 氨基磺酸铵:分析纯, 天津基准试剂公司; 氢氧化钾、硫酸铵、N, N-二甲基甲酰胺、丙酮、异丙醇、石油醚:分析纯, 广东汕头西陇化工厂。
2.2 仪器及实验条件红外测试采用德国Bruker公司EQU INOX 55型傅里叶变换红外光谱仪。纯度测试采用美国waters 2695型高效液相色谱仪。元素分析测试采用Elementar公司Vario EL Ⅲ型元素分析仪。热分析测试采用美国TA公司SDT Q600差热-热重联用仪, 测试条件:氮气气氛, 流速30 mL·min-1, 升温速率10 ℃·min-1。密度测试依据GB/T4472-2011, 测试条件:25 ℃。
撞击感度测试依据GJB5891.22-2006, 采用WL-1型落锤撞击感度仪测试, 测试条件:药量20 mg, 锤重98.00 N。摩擦感度测试依据GJB5891.24-2006, 采用WM-1型摩擦感度仪测试, 测试条件:药量20 mg, 摆角90°, 压强3.92 MPa。静电感度测试依据GJB5891.27-2006, 采用WJ-1型静电感度仪测试, 测试条件:药量20 mg, 电容3×3900 pF, 针距0.5 mm。
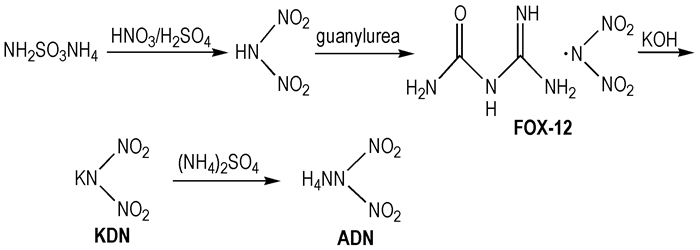
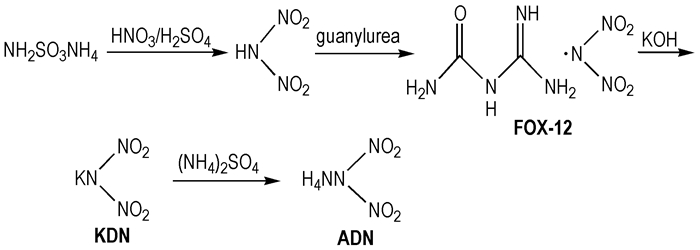
2.3 合成路线以氨基磺酸铵为前体经过混酸硝化后, 倒入含脒基脲的惰性溶剂中, 沉淀出N-脒基脲二硝酰胺盐(FOX-12), 再经过离子交换反应得到二硝酰胺钾(KDN)、二硝酰胺胺(ADN)。具体见Scheme 2。该路线的水解过程温度能够保持在30~45 ℃, 安全性及可操作性强, 所得产品纯度较高, 并实现了三种二硝酰胺盐的公斤级放大, 为二硝酰胺盐类化合物的应用奠定了基础。
|
Scheme 2 Synthetic route of dinitramide salts(this work) |
在100 L双层反应釜内分别加入38 L发烟硝酸、20 L发烟硫酸, 冷却至-40 ℃时, 分批加入10 kg研磨细化的氨基磺酸铵。在-35~-40 ℃反应50~70 min, 将该硝化液用氮气缓慢压至预先冷却的一定浓度的20 L含有脒基脲的惰性溶剂中进行水解反应, 温度最高升至45 ℃。待冷却后过滤、水洗即得8 kg FOX-12白色粗品, 产率为45.94%, 纯度为98.6%。
FOX-12精制:将所得到的FOX-12溶解在N, N-二甲基甲酰胺中, 加入丙酮, 即得到纯净的FOX-12产品, 精制后产品纯度为99.0%, 收率为93.96%。
2.3.2 KDN的制备在50 L双层反应釜内配置9.4 kg水、20 kg乙醇的混合溶液, 加热至50 ℃, 投入3.2 kg KOH、10.2 kg FOX-12, 溶液呈透明状后继续搅拌1 h, 冷却, 析出大量固体, 过滤即得白色KDN粗品约5.66 kg, 产率为80.52%, 纯度为98.3%。
KDN精制:将所得到的KDN溶解在丙酮中, 过滤, 滤液中加入异丙醇, 析出白色固体, 得到纯净的KDN产品, 精制后纯度达99.3%, 收率为88.72%。
2.3.3 ADN的制备配制5 kg KDN/10 L去离子水溶液, 此为溶液A; 配制2.3 kg硫酸铵/5 L水溶液, 此为溶液B; 将溶液A与溶液B混合, 搅拌均匀后加入50 L异丙醇, 析出大量白色硫酸钾沉淀。过滤后将滤液在45~60 ℃减压蒸馏至出现少量固体, 加入异丙醇使固体溶解, 溶液倒入石油醚中即得到白色ADN粗品3.45 kg, 产率80.86%, 纯度为99.2%, 精制后纯度达到99.8%, 收率为90.75%。
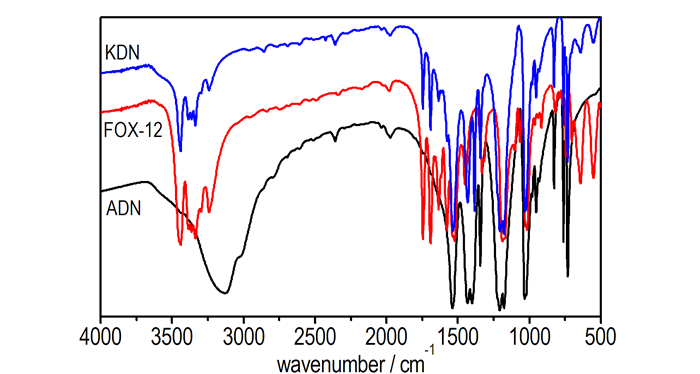
3 结果与讨论 3.1 红外图 1给出了三种二硝酰胺盐的红外谱图。谱图显示FOX-12的特征吸收峰位于3439、3336(—NH伸缩振动)、1745(—C—N伸缩振动)、1691(—C—N伸缩振动)、1538、1523(—NO2伸缩振动)、1331(—C—N伸缩振动)、1189、1026(—N3对称伸缩振动)、960(—N3不对称伸缩振动)cm-1处, 含有脒基脲、二硝酰胺根离子的特征峰。KDN的特征吸收峰位于1536、1432(—NO2伸缩振动)、1344、1224、1178(—NO2伸缩振动)、1031(—N3对称伸缩振动)、952(—N3不对称伸缩振动)cm-1处, 含有二硝酰胺根离子的特征峰。ADN的特征吸收峰位于3128(—NH4+伸缩振动)、1539、1433(—NO2伸缩振动)、1344、1208、1177(—NO2对称伸缩振动)、1033(—N3对称伸缩振动)、953(—N3不对称伸缩振动)、827、762、732(—NO2弯曲振动) cm-1处, 含有铵根离子、二硝酰胺根离子的特征峰。三种二硝酰胺盐在1030~1210 cm-1处都具有二硝酰铵根的特征吸收峰。
|
图 1 二硝酰胺盐的红外谱图 Fig.1 IR spectra of dinitramide salts |
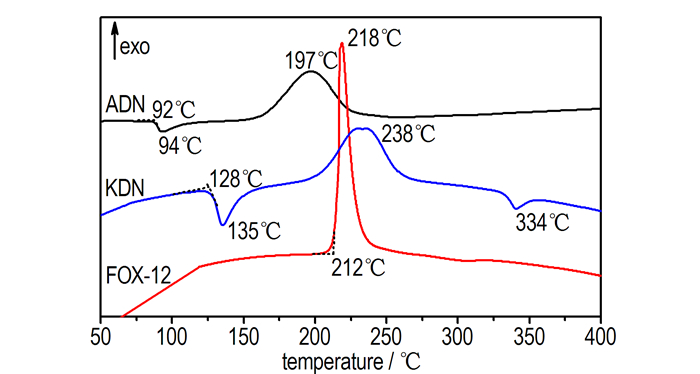
制备的三种二硝酰胺盐的DSC谱图如图 2所示。图 2显示FOX-12的熔点为212 ℃, 与文献值214 ℃[11]相符, 接着出现尖锐的放热分解峰, 峰温为218 ℃。KDN的熔点为128 ℃, 熔化峰峰温在135 ℃, 在220~230 ℃存在宽的放热分解峰, 推测是KDN受热分解为KNO3和N2O, 在334 ℃出现的吸热峰, 即为KNO3的熔化吸热峰, 与文献[12-14]报道一致。ADN的熔点为92 ℃, 在94 ℃附近有一个明显的吸热峰, 此时ADN晶体由固相转变为液态, 约在150 ℃附近开始放热分解, 放热峰峰温197 ℃, 与文献[15]报道一致。
|
图 2 二硝酰胺盐的DSC谱图 Fig.2 DSC curves of dinitramide salts |
表 1给出了制备的三种二硝酰胺盐的元素分析理论值与实测值, 其中FOX-12的N、H、C实测含量与理论值是相符的; KDN中由于不含H、C, 实际测试中H、C含量小于0.1%, N含量与理论值相符; ADN的N、H含量也与理论值基本一致, C含量小于0.1%。因此, 制备的三种二硝酰胺盐的N、H、C元素分析与理论值是相符的。
| 表 1 二硝酰胺盐的元素分析实测值与计算值 Tab.1 Measured values and calculated ones for elemental analyses of dinitramide salts |
表 2给出了制备的三种二硝酰胺盐实测密度值, 与文献值完全吻合。
| 表 2 二硝酰胺盐的密度实测值与文献值 Tab.2 Measured values and literature ones for density of dinitramide salts |
按国军标方法测试了所制备的FOX-12、KDN和ADN的撞击、摩擦、静电感度, 为了便于比较, 同时测试了黑索今(RDX)的感度, 结果见表 3。表 3结果表明, FOX-12、KDN的感度低于RDX, ADN的感度与RDX相当。
| 表 3 二硝酰胺盐的感度结果 Tab.3 Sensitivity results of dinitramide salts |
(1) 以氨基磺酸铵为前体, 通过改进工艺实现了三种二硝酰胺盐(FOX-12、KDN、ADN)的工艺放大, 完成了结构鉴定及性能测试。所得粗品纯度均大于98%。三种二硝酰胺盐中FOX-12的熔点最高, KDN次之, ADN最低。FOX-12与KDN感度低于ADN。
(2) 该制备工艺增强了操作过程的安全性, 省去了原ADN制备工艺中繁琐的提纯过程, 缩短了二硝酰胺盐的合成周期; 以低感度、不吸湿的FOX-12、KDN作为ADN制备的上游产品, 便于储存, 是一种适合进行工业规模放大合成ADN的新方法。
| [1] |
雷永鹏, 阳世清, 徐松林, 等. 钝感高能材料N-脒基脲二硝酰胺盐的研究进展[J].
含能材料, 2007, 15(3): 289-293. LEI Yong-peng, YANG Shi-qing, XU Song-lin, et al. Progress in insensitive high energetic materials N-Guanylurea dinitramide[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2007, 15(3): 289-293. |
| [2] |
刘海洲, 许华新, 李青, 等. GUDN的合成与应用进展[J].
化学推进剂与高分子材料, 2009, 7(4): 14-16. LIU Hai-zhou, XU Hua-xin, LI Qing, et al. Synthesis and application progress of GUDN[J]. Chemical Propellants & Polymeric Materials, 2009, 7(4): 14-16. |
| [3] |
Thomas K H, Carol J H, Robert B W.Phase-Stabilized Ammonium Nitrate and Method of Making Same:US 5292387[P], 1994.
|
| [4] |
Weiser V, Lity A, Kelzenberg S, et al.Burning behavior of B/KDN-mixtures compared with B/KNO3[C]//45th International Annual Conference of ICT, Karlsruhe, Germany, 2014:1/111-6/111.
|
| [5] |
Golofit T, Maksimowski P, Biernacki A. Optimization of potassium dinitramide preparation[J].
Propellants, Explosives, Pyrotechnics, 2013, 38(2): 261-265. DOI:10.1002/prep.v38.2 |
| [6] |
How-Ghee A, Wolfgang F. Synthesis, characterization, and crystal structures of Cu, Ag, and Pd dinitramide salts[J].
Z Anorg Allg Chem, 2002, 628: 2894-2900. DOI:10.1002/1521-3749(200213)628:13<2894::AID-ZAAC2894>3.0.CO;2-R |
| [7] |
Anders L, Niklas W.Green propellants based on ammonium dinitramid(ADN)[M], Avances in Spacecraft Technologies, 2010:139-156.
|
| [8] |
Hiroki M, Hiroto H, Atsumi M. Thermal behavior of new oxidizer ammonium dinitramide[J].
Therm Anal Calorim, 2013, 111: 1183-1188. DOI:10.1007/s10973-012-2441-0 |
| [9] |
Bottaro J C.Method of forming dinitramide salts:US 5198204[P], 1993.
|
| [10] |
Voerde C, Skifs H.Method of producing salts of dinitramide acid.WO:2005070823[P], 2005.
|
| [11] |
Stmark H O, Bemm U, Bergman H, et al. N-guanylurea-dinitramide:a new energetic material with low sensitivity for propellants and explosives applications[J].
Thermochimica Acta, 2002, 384: 253-259. DOI:10.1016/S0040-6031(01)00800-0 |
| [12] |
Berger B, Bircher H, Studer M, et al. Alkali dinitramide salts.Part 1:synthesis andcharacterization[J].
Propellants, Explosives, Pyrotechnics, 2005, 30: 184-190. DOI:10.1002/(ISSN)1521-4087 |
| [13] |
Ming L, Zhi-Zhong Z, YANG Hui-kong, et al. The thermal behaviour of potassium dinitramide[J].
Thermochim Acta, 1999, 355: 105-112. |
| [14] |
Ming L, Zi-Ru L, Yang-Hui K. The thermal behaviour of potassium dinitramide Part 2.mechanism of thermal decomposition[J].
Thermochim Acta, 1999(355): 131-120. |
| [15] |
Oliveira J I S, Diniz M F, Azevedo M F P, et al.Synthesis and characterization of ADN (AQI/IAE)[C]//41th International Annual Conference of ICT, Karlsruhe, Germany, 2010:1/49-11/49.
|
Ammonium sulfamate was nitrated at low temperature with mixed acid, and the reacting solution was neutralized with N-guanylurea to form N-guanylurea dinitramide(FOX-12).Potassium dinitramide(KDN) was produced by reacting FOX-12 with KOH in an aqueous solution.Ammonium dinitramide(ADN) was prepared by an ion-exchange reaction of KDN and(NH4)2SO4.




